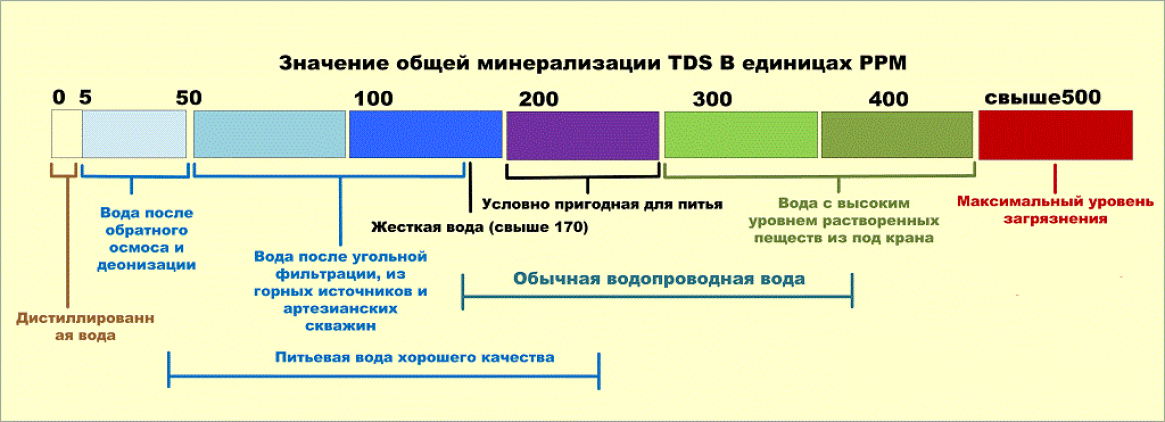
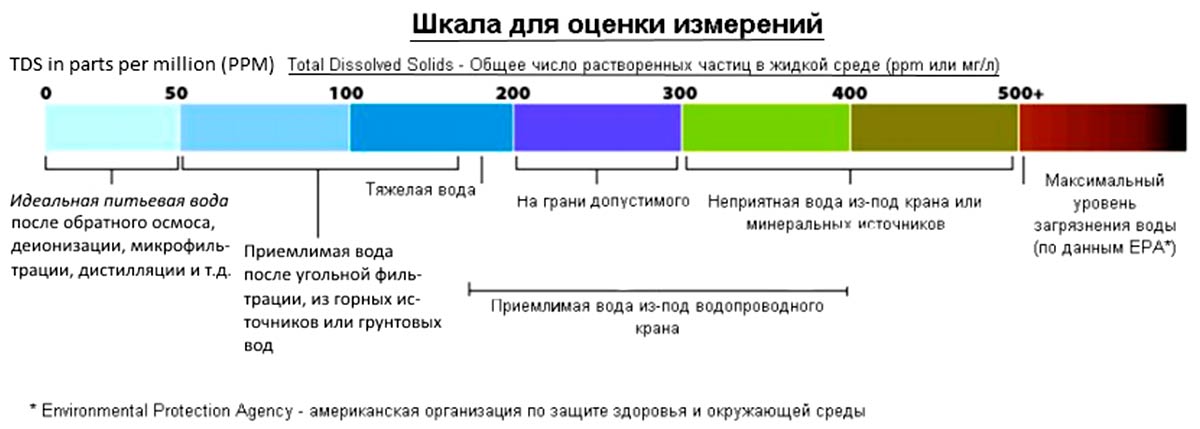
Что такое жесткая и мягкая вода
Мягкая вода характеризуется, в первую очередь, приятным вкусом и сохранением защитного слоя на коже и волосах даже после воздействия мыла. Жесткая же, напротив, отличается выраженным горьковатым неприятным привкусом и высушиванием кожи и волос.
Как определить вода жесткая или мягкая?
Чем отличается жесткая вода от мягкой и как без анализа отличить их и определить излишнюю жесткость воды? Существует ряд признаков, по которым можно сделать вывод о наличии избыточных солей жесткости, основываясь на собственных наблюдениях.
Признаки жесткой воды:
- приглушенный вкус напитков и воды,
- “моментальное” заваривание чая за пару секунд до черноты. Заваренный в мягкой воде, черный чай постепенно приобретает оранжево-красный цвет. Жесткая же вода “убивает” весь вкус напитка и эстетическое удовольствие. Если в чае есть какие-то добавки, например, барбарис, они почти не будут чувствоваться как на вкус, так и по запаху.
- плохое пенообразование у любых моющих средств.
- “скрип” у кожи и волос после умывания с мылом. Такой эффект означает смывание естественной защитной пленки.
- повышенная сухость кожи и волос после умывания.
Как узнать, жесткая ли у вас вода, если не с чем сравнивать и вы всегда жили на одном месте? В большинстве случаев наблюдаются средние показатели жесткости и люди не всегда догадываются, что с водой что-то не так, так как привыкли к определенному вкусу и запаху.
Конечно, организм приспосабливается ко многим вещам. Постепенно мы привыкаем скупать тоннами увлажняющий крем и пить бутилированную воду. Но даже в разных районах одного города может быть разная вода и придя в гости к друзьям и впервые попробовав действительно вкусный чай, можно задуматься, а что вообще с моей водой?
Какая вода лучше жесткая или мягкая?
Согласно СанПин, есть рекомендации только для общей жесткости воды. Что касается “настоящей” жесткости, которую не убрать кипячением, приходится полагаться на собственные ощущения. Если говорить о вкусе и уходе за кожей, жесткая вода однозначно проигрывает. У мягкой, впрочем, есть один нюанс: она может оказывать коррозионное воздействие на сантехнику и в ряде случаев даже требовать искусственной регуляции солевого баланса.
Польза воды для организма
Несмотря на то, что вода является неорганическим соединением, ее пользу для организма сложно переоценить. Жизнь когда-то зародилась в воде и развивается благодаря ей. Без воды не может существовать ни одно живое существо, в том числе и человек. Антуан де Сент-Экзюпери высказался о воде просто и исчерпывающе: «Ты – сама жизнь». В профессиональной среде биологов бытует шутка, что вода изобрела человек для своего передвижения. Каждому школьнику известно, что организм человека состоит из воды почти на 80%. Для чего же в организме столько воды, какова её биологическая роль?
Попадая в организм через рот, вода попадает в пищевод, затем в желудок и оттуда в кишечник. Там происходит её всасывание через стенки кишечника в кровь. Вместе с водой при этом всасываются не только те минералы, которые были в ней, но и органические и минеральные вещества, попавшие в организм с пищей. Это возможно благодаря тому, что вода является абсолютным растворителем. Она способна растворять буквально все попавшие в её среду вещества.
Кровеносная система является основным путём «доставки» жизненно необходимых питательных веществ, витаминов и микроэлементов к клеткам организма. Кровь состоит наполовину из кровяных телец, наполовину из плазмы. А плазма представляет собой именно воду с растворёнными в ней органическими и неорганическими веществами. Эти вещества питают каждую живую клетку.
В человеческом теле 60% жидкости содержится внутри клеток, 40% — это межклеточная жидкость.
Стоит отметить, что человеческие органы «потребляют» воду в разном количестве.
Для сравнения, рассмотрим содержание воды в разных внутренних органах и системах:
- мозг – 90%;
- сердце, лёгкие, почки – 80%;
- кожа – 70%;
- кости – 25%;
- зубы – 10%.
Удивительно, что самым «водянистым» органом оказывается мозг. Из этого можно сделать вывод, что при недостатке жидкости в организме страдают, в первую очередь, мыслительные процессы. Это подтверждается тем, что путешественники в пустыне, страдающие от жажды, отмечают спутанность мышления и испытываю галлюцинации.
Не менее удивительно, что такие, казалось бы, «сухие» части тела, как зубы и кости, тоже содержат жидкость, и немало.
После того, как вода обеспечила все органы и клетки питательными веществами, минералами и витаминами, она должна покинуть организм. Но при этом она выполняет еще одну важнейшую функцию.
В результате происходящих в тканях биохимических реакций (переработки белков и углеводов) в клетках появляются отработанные вещества – шлаки. Вода снова выступает в роли растворителя. Она растворяет и выводит все отходы жизнедеятельности сначала из каждой клетки, а затем из организма.
Покидает организм вода разными путями. Половина её выводится через мочевыделительную систему. Если принять условную норму потребления жидкости в день в объёме 2 литра, то почки выводят 1 литр ежедневно. Ещё 300 мл выводится через кишечник. Целых 400 мл (два стакана!) воды испаряется через кожу. И более 300 мл человек просто выдыхает.
Такое важное путешествие по всем системам человеческого тела вода совершает ежедневно. За одни сутки обновляется 6% всей жидкости в теле, а за 10 дней – половина
Можно с уверенностью утверждать, что за срок чуть более 20 дней вся вода полностью обновляется. Получается, что за такой период сам человек становится иным более чем на 70%.
Кроме основных функций (доставки питательных веществ и выведения шлаков) вода выполняет также следующие задачи:
- участвует в процессе терморегуляции, охлаждая организм потоотделением;
- улучшает состояние суставов, являясь основным компонентом межсуставной смазки;
- регулирует кровяное давление, нормализуя тонус сосудов и состояние крови;
- улучшает пищеварение, приводя в норму повышенную кислотность;
- поддерживает в хорошем состоянии кожу и волосы;
- помогает эффективно бороться с ожирением, выводя шлаки из организма и регулируя повышенный аппетит.
Методы устранения
Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи:
-
- Ca(HCO3)2→otCaCO3↓+CO2+H2O{\displaystyle {\mathsf {Ca(HCO_{3})_{2}{\xrightarrow{^{o}t}}CaCO_{3}\downarrow +CO_{2}+H_{2}O}}}
Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту.
Реагентное умягчение. Метод основан на добавлении в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат:
-
- Ca(HCO3)2+Ca(OH)2→2CaCO3↓+2H2O{\displaystyle {\mathsf {Ca(HCO_{3})_{2}+Ca(OH)_{2}\rightarrow 2CaCO_{3}\downarrow +2H_{2}O}}}
Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na3PO4, входящий в состав большинства препаратов бытового и промышленного назначения:
-
- 3Ca(HCO3)2+2Na3PO4→Ca3(PO4)2+6NaHCO3{\displaystyle {\mathsf {3Ca(HCO_{3})_{2}+2Na_{3}PO_{4}\rightarrow Ca_{3}(PO_{4})_{2}+6NaHCO_{3}}}}
- 3MgSO4+2Na3PO4→Mg3(PO4)2↓+3Na2SO4{\displaystyle {\mathsf {3MgSO_{4}+2Na_{3}PO_{4}\rightarrow Mg_{3}(PO_{4})_{2}\downarrow +3Na_{2}SO_{4}}}}
Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому легко отделяются механическим фильтрованием. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдаёт ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж.
В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %.
Различают нанофильтрацию (условный диаметр отверстий мембраны равен единицам нанометров) и пикофильтрацию (условный диаметр отверстий мембраны равен единицам пикометров). В качестве недостатков данного метода следует отметить:
-
- необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану;
- относительно высокая стоимость 1 л получаемой воды (дорогое оборудование, дорогие мембраны);
- низкую минерализацию получаемой воды (особенно при пикофильтрации). Вода становится практически дистиллированной.
Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Полностью очистить воду от солей жёсткости можно дистилляцией.
Жесткость воды. Соли жесткости
Жесткость воды — это совокупность химических и физических свойств воды, связанных с содержанием в ней растворенных солей щелочноземельных металлов, главным образом, кальция и магния (так называемых «солей жесткости»).
Соли жесткости имеют разные свойства. Так, при нагреве воды, некоторые из них выпадают в осадок в виде накипи, а некоторые — не выпадают. По этому признаку их и начали разделять.
Соли, выпадающие в осадок, стали называть солями временной (или устранимой) жесткости, а соли, которые не выпадают в осадок при нагреве воды, солями постоянной жесткости.
Сульфаты, хлориды и нитраты магния и кальция, растворенные в воде, образуют постоянную (или некарбонатную) жесткость. Они выпадают в осадок исключительно при полном испарении воды.
Временная жесткость характеризуется присутствием в воде наряду с катионами Ca2+, Mg2+ и Fe2+ гидрокарбонатных, или бикарбонатных анионов (HCO3-).
При кипячении воды гидрокарбонаты разлагаются, образуя очень плохо растворимый карбонат кальция, углекислый газ и воду:
Общая жесткость складывается из постоянной и временной.
В данной таблице приведены основные катионы металлов, вызывающие жесткость, и главные анионы, с которыми они ассоциируются.
| Катионы | Анионы |
| Кальций (Ca2+) | Гидрокарбонат (HCO3-) |
| Магний (Mg2+) | Сульфат (SO42-) |
| Стронций (Sr2+) | Хлорид (Cl-) |
| Железо (Fe2+) | Нитрат (NO3-) |
| Марганец (Mn2+) | Силикат (SiO32-) |
На практике стронций, железо и марганец оказывают на жесткость столь небольшое влияние, что ими, как правило, пренебрегают. Алюминий (Al3+) и трехвалентное железо (Fe3+) также влияют на жесткость, но при уровнях рН, встречающихся в природных водах, их растворимость и, соответственно, «вклад» в жесткость ничтожно малы. Аналогично, не учитывается и незначительное влияние бария (Ва2+).
Жёсткость воды — происхождение
Ионы кальция (Ca2+) и магния (Mg2+), а также других щелочноземельных металлов, обуславливающих жесткость, присутствуют во всех минерализованных водах. Их источником являются природные залежи известняков, гипса и доломитов.
Ионы кальция и магния поступают в воду в результате взаимодействия растворенного диоксида углерода с минералами и при других процессах растворения и химического выветривания горных пород.
Источником этих ионов могут служить также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий.
Обычно в маломинерализованных водах преобладает (до 70%-80%) жесткость, обусловленная ионами кальция (хотя в отдельных редких случаях магниевая жесткость может достигать 50-60%).
С увеличением степени минерализации воды содержание ионов кальция (Са2+) быстро падает и редко превышает 1 г/л.
В целом, жесткость поверхностных вод, как правило, меньше жесткости вод подземных. Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего в период половодья, когда обильно разбавляется мягкой дождевой и талой водой. Морская и океанская вода имеют очень высокую жесткость (десятки и сотни мг-экв/дм3).
Жесткость воды — единицы измерения
С 1 января 2014 года в России введен межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». По новому ГОСТу жесткость выражается в градусах жесткости (°Ж).
1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр (1 °Ж = 1 мг-экв/л). В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
За рубежом приняты другие единицы измерения жесткости воды, соотношение этих единиц представлено ниже:
1°Ж = 20,04 мг Ca2+ или 12,15 Mg2+ в 1 дм3 воды;
1°DH = 10 мг CaO в 1 дм3 воды;
1°Clark = 10 мг CaCO3 в 0,7 дм3 воды;
1°F = 10 мг CaCO3 в 1 дм3 воды;
1 ppm = 1 мг CaCO3 в 1 дм3 воды.
Численные значения жесткости измеренные в мг-экв/л, моль/м3, и °Ж, несмотря на различия в обозначении, равны между собой.
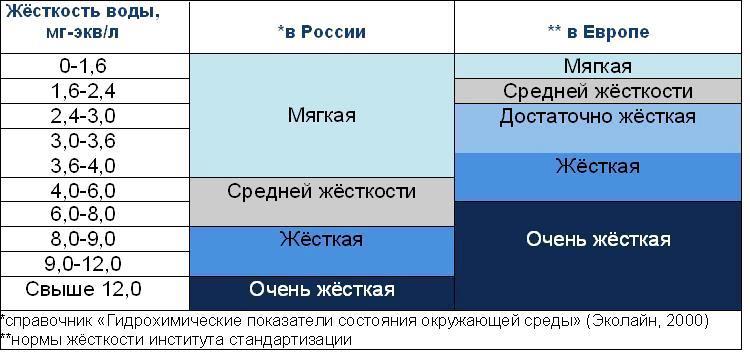
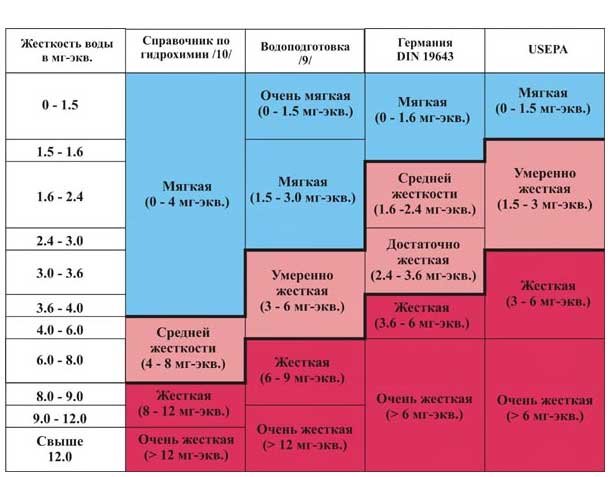
По значению общей жесткости природные воды делят на группы:
- очень мягкая вода (0–1,5 мг-экв/л)
- мягкая вода (1,5–4 мг-экв/л)
- вода средней жесткости (4–8 мг-экв/л)
- жесткая вода (8–12 мг-экв/л)
- очень жесткая вода (более 12 мг-экв/л).
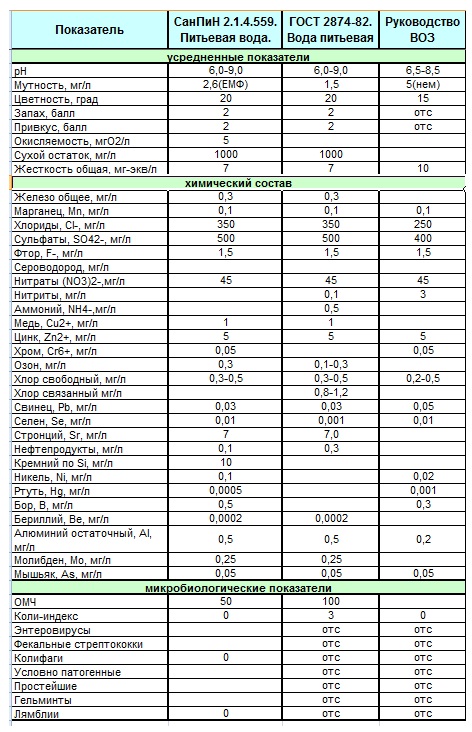
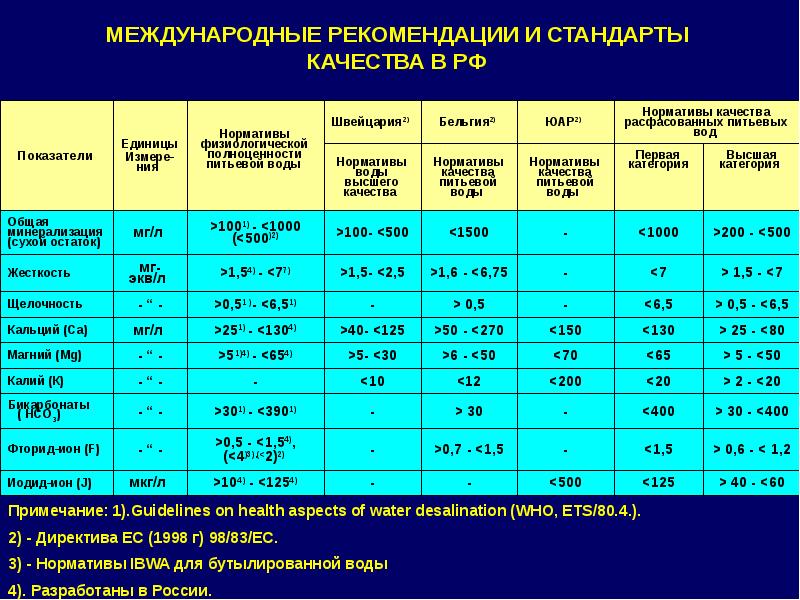
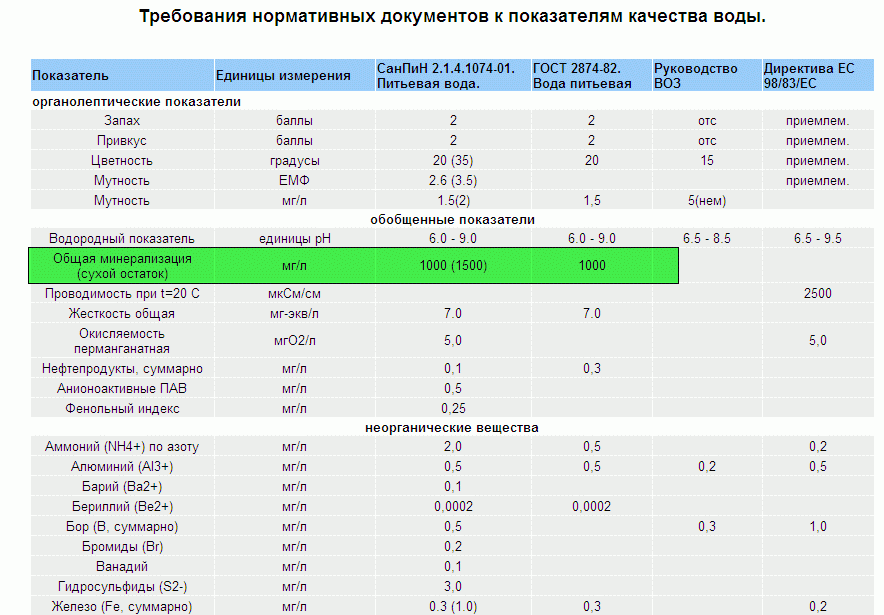
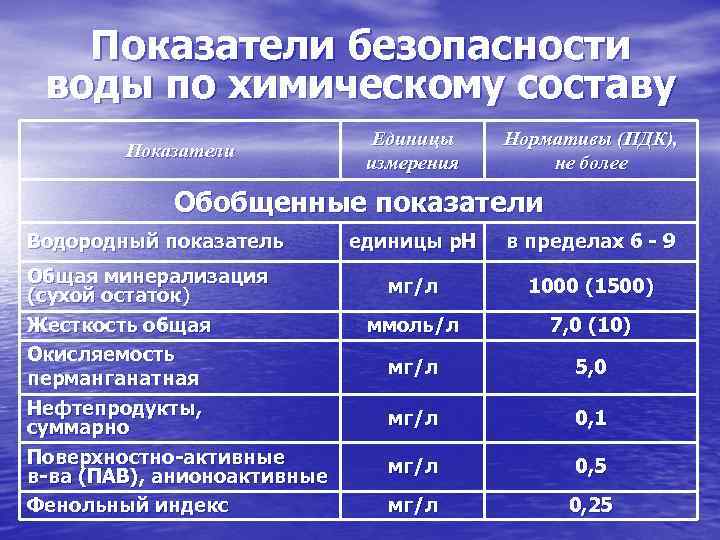
Нормативные требования и рекомендации
Рекомендации всемирной организации здравоохранения (ВОЗ) для питьевой воды:
кальций – 20-80 мг/л; магний – 10-30 мг/л. Для жесткости какой-либо рекомендуемой величины не предлагается.
Как измерить жёсткость
Существуют ситуации, когда необходимо узнать жесткость воды для посудомоечной машины или определить ее пригодность для разведения аквариумных рыбок. Существует несколько способов проверить воду в домашних условиях. Естественно, без лаборатории все тесты весьма условны и не каждый сможет ими воспользоваться, так как не сможет понять разницы.
- Проверить, как пенится мыло. Просто намыльте руки мылом, если оно хорошо пенится и легко смывается, значит, вода не очень жесткая и наоборот. Такой способ поможет определить лишь крайние показатели жесткости.
- Проверьте интенсивность образования накипи на стенках чайника или тэнах нагревательных приборов, чем слой толще, тем выше жесткость. Проблема заключается в том, что невозможно определить непродолжительные изменения состава, процесс образования накипи не быстрый и способен дать лишь общее представление и только о временной жесткости.
- Попробуйте воду на вкус, жесткая вода будет горьковатой. Способ также весьма приблизительный, не каждый человек сможет выступить в роли гурмана и понять разницу.
- Более точную картину дают индикаторы жесткости, продаются чаще в виде бумажек, пропитанных специальным составом, меняющим цвет в зависимости от состава жидкости.
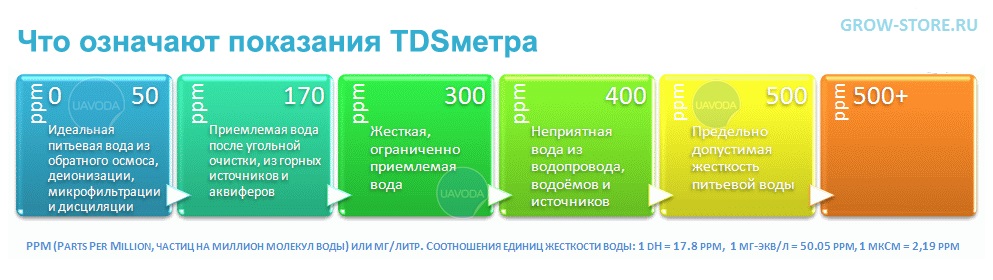
- Есть и технические средства для измерения состава воды. Их называют TDS-метрами, приборы определяют общее количество растворенных в воде веществ. Устройство компактное и подходит к использованию в домашних условиях.
Не стоит забывать, что вода способна навредить бытовой технике или аквариумным рыбкам. Вода участвует во всех обменных процессах нашего организма и способна вызвать неприятные последствия, особенно часто вода из-под крана вызывает раздражение или сухость кожи, но может и стать причиной камней в почках.
В каких единицах измеряется жесткость

В России и многих странах постсоветского пространства значение жесткости измеряется в градусах жесткости. Но может измеряться этот параметр также в массовом числе и объемной доле. Официально принятая единица измерения жесткости, которая используется в Международной системе единиц – моль на куб. метр. Но на практике измерение обычно производится в других единицах – в мг-экв/л (миллиэквивалент на литр).
Самостоятельно узнать, что жидкость в вашем кране течет слишком жесткая, не сложно. Признаками этого могут стать такие наблюдения и факторы:
- после выстирывания белье становится жестким, быстро линяет и теряет цвет;
- на поверхности чая, кофе и других напитков, требующих заливания кипятком, образуется мутная или белесая пленочка;
- мыло, порошки, шампуни плохо пенятся и слишком быстро расходуются;
- аромат блюд и напитков не яркий;
- фильтры быстро выходят из строя, ломается техника, использующая водонагревательные элементы;
- на стенках кастрюль и чайников после кипячения есть налет.
Вкус жесткая вода имеет немного горьковатый. Но заметить это можно только в случае, если вы долгое время пили лишь мягкую или очищенную водичку. Также измерить уровень жесткости можно с помощью экспресс-теста (купить можно в аптеке или в зоомагазине) или солемера (приобретается там, где продается все для аквариумов).
Как понизить?
Понизить жесткость немного сложнее. Нужно быть осторожным, в кислой среде погибает большинство видов рыб и растений.
Домашние рецепты
Применяют следующие народные методы, понижая количество солей:
- Сделать смесь из водопроводной и дистиллированной водой.
- Кипячение. Водопроводную воду кипятят на огне 1 час. В аквариум добавляют только верхние слои, так как на дно соли выпадают в осадок.
- Замораживание. В емкость добавляют воду, которую отправляют в морозильную камеру.
Дожидаются, когда она покроется толстой корочкой. В ней пробивают отверстие, выливая жидкое содержимое. Лед топят, наливая в аквариум.
Это самые простые способы, которые может применить любой человек. Не нужно покупать дополнительные ингредиенты.
Фильтры
Химические методы включают в себя систему фильтрации. Можно применить как разные вещества, так и электронные системы.
Применяют следующие виды фильтров:
- осмотический;
- деионизирующий;
- торфяной.
Первые 2 метода применяют с помощью готовой системы.
Если используют торфяной фильтр, воду предварительно кипятят. После фильтрации она приобретет желтый оттенок. Его убирают активированным углем.
Как определить жесткость воды в лаборатории
Бывают случаи, когда нужно как можно точнее определить жесткость воды.
Как уже говорилось выше, самый доступный, используемый повсеместно метод определения количества солей в воде, – титрование. Однако точность этого метода относительно невысока.
Один из самых точных приборов, помогающих определить концентрацию солей, по мнению сотрудников лабораторий, – АКМС-1. На экран прибора автоматически выводятся результаты сравнения разности электродных потенциалов и эталонных значений.
Резонансное поглощение фотонов атомами анализируемых элементов является основой метода атомной спектрометрии. Данный метод отличается высокой точностью, однако стоимость приборов, применяемых в нем, довольно высока.
Статьи, рекомендуемые к прочтению:
- Как удалить накипь в чайнике: методы и рекомендации
- Комплект очистки воды: для чего он необходим
- Очистка воды от запаха: устраняем не только запах, но и его причину
Как правильно пить воду
Чтобы вода приносила максимальную пользу, пить её нужно небольшими порциями на протяжении дня.
Первый стакан воды нужно выпить сразу после пробуждения, это запустит обменные процессы в организме и восполнит ночные потери жидкости
Далее нужно выпивать по одному стакану за полчаса до каждого приёма пищи. Это снизит ложное чувство голода и позволит избежать переедания.
После еды следует попить воды через 2-2,5 часа, чтобы пищеварительный процесс завершился поступлением необходимой жидкости.
Не стоит забывать пить воду за 30-40 минут до спортивной тренировки, а также за час до сна.
В остальное время питьевой режим должен быть основан на чувстве комфорта. Организм сам подскажет, когда и сколько нужно выпить воды, нужно только прислушаться к сигналам собственного тела.
Интересно, что иногда человек ощущает жажду, как голод. Можно попробовать заменить перекусы стаканом воды. Часто этого бывает достаточно, чтобы унять аппетит.
Важно, что чувство жажды, которое не проходит даже при обильном питье, может быть симптомом серьёзных заболеваний. В этих случаях следует обратиться к врачу как можно скорее
Тест на жесткость воды в аквариуме
Чаще всего применяют два вида тестов:
- Тест полоски
- Капельные тесты
Первые обходятся дешевле, но менее точны.
Впрочем, их точности вполне хватает для понимания того, что в аквариуме пошло не так.
Тест полоски

В основном распространены тест полоски, измеряющие сразу несколько основных параметров аквариумной воды.
Например.
Tetra Test 6 в 1 позволяет измерить общую жесткость, карбонатную жесткость, pH, уровень нитратов, нитритов и хлора за одно применение.
Тест полоска погружается в аквариум на несколько секунд, после чего она извлекается. Далее нанесенная цветная шкала тестовой полоски изменит свой цвет.
Получившиеся значения параметров воды вы сможете расшифровать по цветовой шкале на упаковке, сравнив ее с получившимся цветом на тест полоске.
Капельные тесты

Их применение не сложнее, чем тест полоски.
В мерный стаканчик набирают 5 мл аквариумной воды. После чего по капле добавляют реагент, постоянно встряхивая мерный стаканчик.
Количество капель нужно считать.
Цвет исследуемой воды изменяется с каждой каплей. Как только вода приобретет зеленую окраску, титрование прекращают.
Количество затраченных капель реагента будет соответствовать показаниям общей или карбонатной жесткости воды в зависимости от того, что вы измеряли.
Капельные тесты широко распространены и позволяют измерить практически любой параметр воды в аквариуме от жесткости до нитратов, аммиака, нитритов или концентрации железа.
Именно капельные тесты обладают наилучшей точностью, которая доступна аквариумистам в домашних условиях.
После измерения жесткости аквариумной воды и расшифровки результата, остается выяснить, что делать дальше. Понижать или повышать жесткость воды.
Признаки повышенной жесткости
Что такое жесткость воды? Это показатель, определяющий уровень магниевых и кальциевых солей, которые входят в химический состав жидкости. Единицы измерения — моль/куб.м и мг.экв./литр.
Жесткая вода — частое явление, которое обусловлено влиянием подземных вод, насыщенных солями химических элементов. Кроме того, подобная жидкость может содержать хлоридные и фосфатные соединения, а также различные органические загрязнители.

Чтобы определить жесткость воды своими руками, рекомендуется воспользоваться специальным устройством — кондуктометром, предназначенным для замера параметра электропроводимости жидкости. Высокий показатель указывает на повышенную концентрацию солей металлов в воде.
В процессе кипячения химические соли образуют осадочную массу, но большая часть соединений попадают в человеческий организм, оседают на стенках приборов, техники и оборудования.
Какая же вода будет считаеться жесткой? Основные признаки повышенной концентрации солей следующие:
- моющие средства плохо вспениваются;
- после кипячения образуется накипь и белый налет;
- после стирки вещей и мытья посуды остаются характерные разводы;
- жесткая жидкость приобретает неприятный горький привкус;
- вода оказывает негативное влияние на эксплуатационные характеристики тканей;
- повышенная концентрация солей приводит к заболеваниям выделительной системы, а также к дряблости и сухости кожи.
Норма потребления воды для человека
Упомянутые выше 2 литра потребляемой в день жидкости – весьма условная цифра. Норма потребления воды для человека индивидуальна и зависит как от самого организма, так и от внешних условий.
Правильным будет прислушиваться к самочувствию и соблюдать водный баланс: сколько воды покидает тело, столько и нужно выпить, чтобы восполнить потери влаги.
Человек, занимающийся физическим трудом, потеет и выдыхает много пара. Значит, он будет пить больше, чем сотрудник офиса, спокойно сидящий за столом.
Зимой организму требуется меньше жидкости, чем летом, ведь с потоотделением вода почти не выводится.
Жителям жарких стран приходится пить больше, чем северянам. Их норма потребления достигает 3,5 литров в день, а в очень экстремальных температурных условиях потребуется до 6 литров.
Почувствовать нехватку жидкости в организме очень легко, надо лишь быть внимательным к себе. Симптомами обезвоживания являются сухость слизистых рта и глаз, сильная жажда, учащённое дыхание, головокружение из-за пониженного кровяного давления, слабость, судороги, отсутствие выделения пота, проблемы с мочеиспусканием и запор, в тяжелых случаях обмороки.