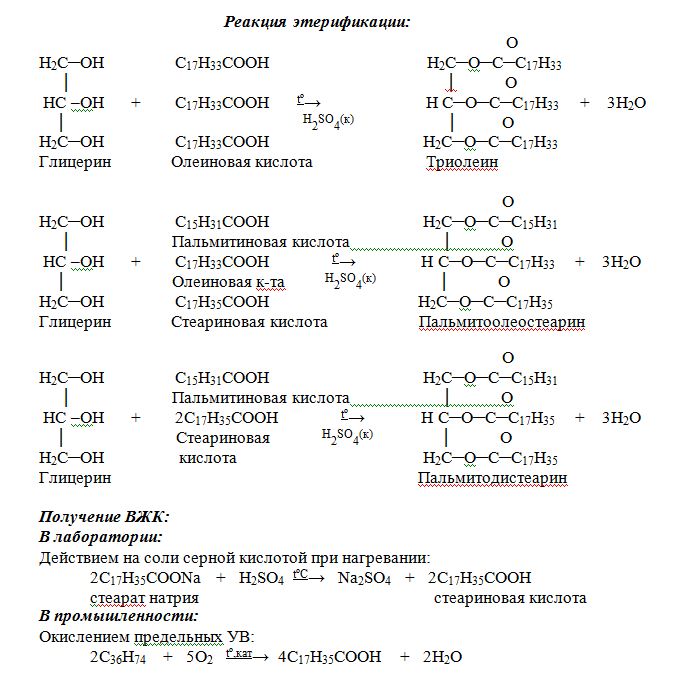
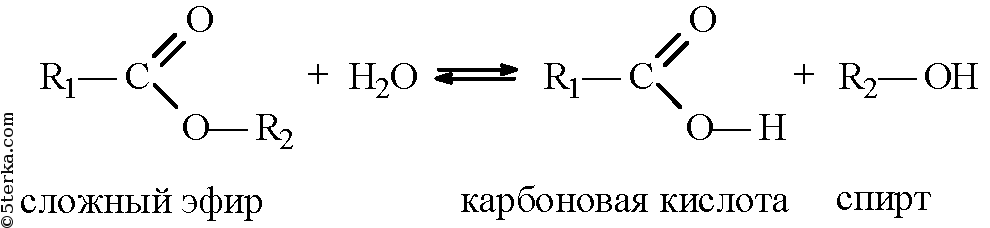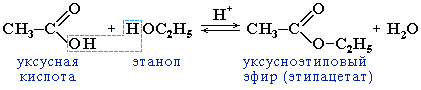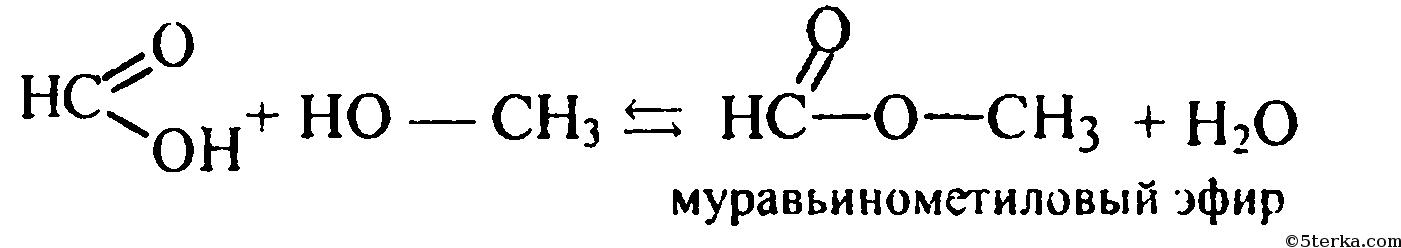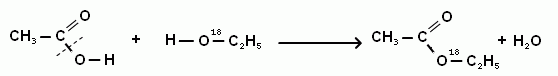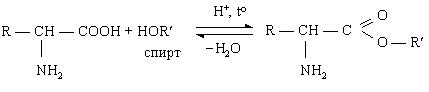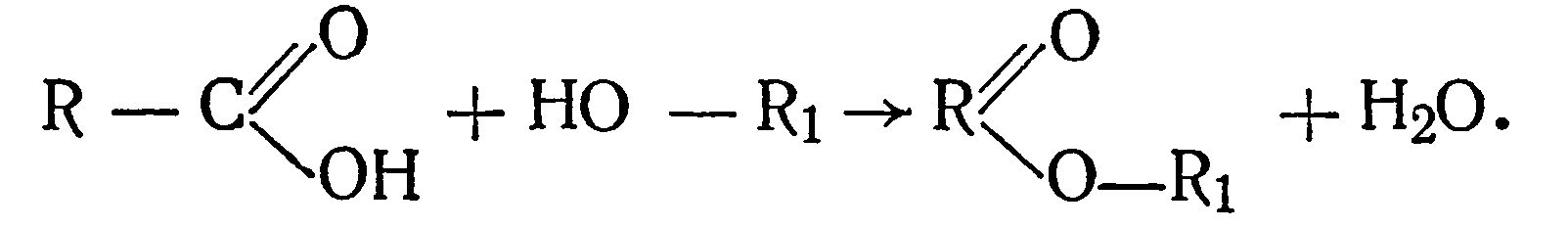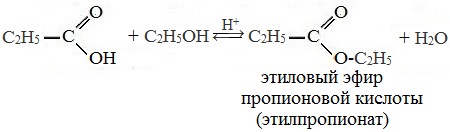Что такое этерификация
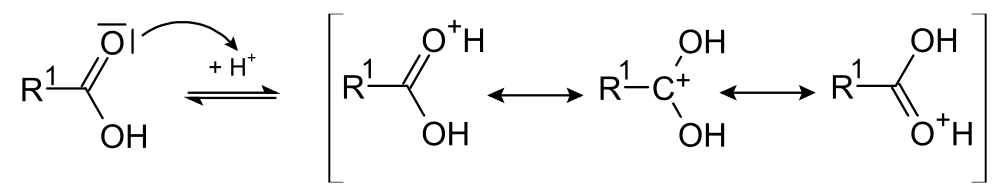
Этерификация — это процесс, в котором образуется сложный эфир. Чаще всего это делается с карбоновыми кислотами. Этерификация происходит, когда карбоновая кислота реагирует со спиртом. Эта реакция возможна только тогда, когда в реакционную смесь подается кислотный катализатор и тепло. В противном случае не будет никакой реакции, даже если карбоновая кислота и спирт смешаны вместе. Это потому, что этот процесс требует высокой энергии для удаления группы -ОН из карбоновой кислоты. Следовательно, для уменьшения энергии активации реакции необходим катализатор, а в качестве источника энергии требуется тепло.
Побочным продуктом, образующимся в этой реакции, является вода. Следовательно, в присутствии дегидратирующего агента мы можем получить чистый сложноэфирный продукт. Изменяя карбоновую кислоту или спирт, можно получить сложный эфир с требуемыми атомами углерода. Реакция этерификации является равновесной реакцией. Поэтому для получения высокого выхода сложного эфира мы можем использовать либо избыточное количество спирта, либо дегидратирующий агент для удаления воды из системы. Если нет, вода может быть удалена другим методом, таким как дистилляция.
Рисунок 01: Синтез метилацетата
На изображении выше показано производство метилацетата с использованием этановой кислоты и метанола в качестве реагентов. Побочным продуктом является молекула воды. Молекула воды образуется из Н+ исходит от алкоголя и тому –ОН карбоновой кислоты. Используемый здесь катализатор — серная кислота.
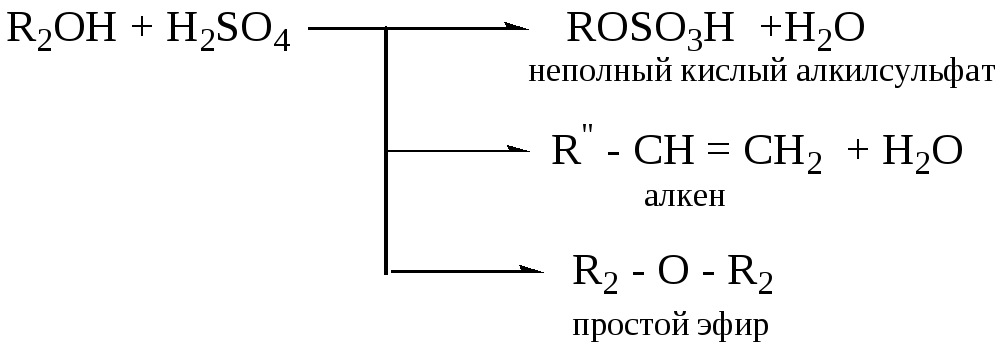
Скорость — реакция — этерификация
Скорость реакции этерификации зависит от природы кислоты и спирта, а именно — от того, с каким атомом углерода связана гидроксильная группа ( первичным, вторичным или третичным) и каково строение углеродной цепи, связанной с карбоксильной группой. Объемистые радикалы создают пространственные затруднения и мешают образованию промежуточных продуктов присоединения.
Скорость реакции этерификации зависит от строения и свойств как кислоты, так и спирта. Реакционная способность спиртов уменьшается в следующем ряду: СН3 — OHR — CH2 — OHR2CH — OHR3C — ОН.
Скорость реакции этерификации зависит от природы кислоты и спирта, а именно — от того, с каким атомом углерода связана гидроксильная группа ( первичным, вторичным или третичным) и каково строение углеродной цепи, связанной с карбоксильной группой. Объемистые радикалы создают пространственные затруднения и мешают образованию промежуточных продуктов присоединения.
Скорость реакции этерификации зависит от строения как спирта, так и кислоты.
|
Сложные эфиры гомологов муравьиной кислоты. |
Скорость реакции этерификации наибольшая для первичных спиртов.
Скорость реакции этерификации максимальна в начальный период, но по мере образования эфира снижается. Это происходит в результате омыления эфира водой. В тот момент, когда образовавшиеся компоненты и компоненты, вступившие в реакцию, эквивалентно равны, наступает химическое равновесие. При этом скорость прямой реакции равна скорости обратной реакции.
Скорость реакции этерификации зависит от строения как спирта, так и кислоты.
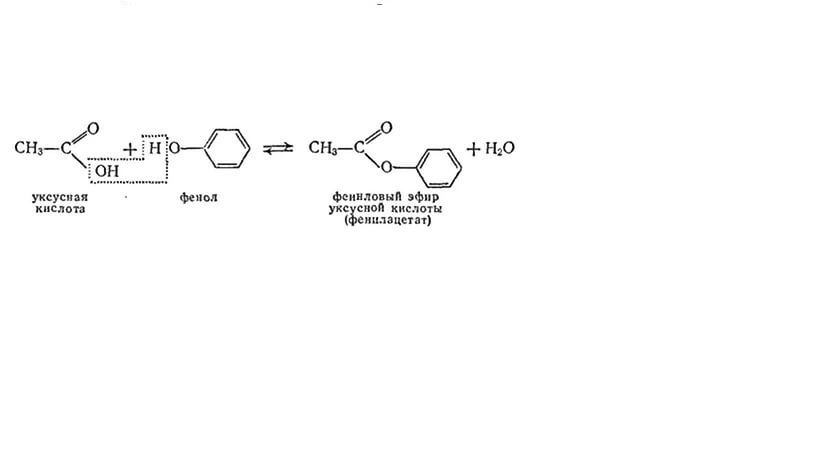
Скорость реакции этерификации четыреххлористого кремния фенолами значительно меньше, чем алифатическими спиртами, и для завершения процесса необходимо длительное нагревание при высокой температуре.
На скорость реакции этерификации влияет также объем группы R в карбоновой кислоте. Известно, что пивалиновая кислота ( 67), кислотность которой лишь немного меньше, чем кислотность уксусной кислоты, образует сложкые эфиры с большим трудом, так как метильные группы затрудняют нуклео-фильную атаку находящегося рядом атома углерода карбоксильной группы.
Увеличение скорости реакции этерификации до — Стигается применением катализаторов — минеральных кислот.
Определены константы скорости реакции этерификации, рассчитанные по уравнению второго порядка, для бутанола-1, гексанола-1, нонанола-1, 2-этилгек-санола — 1, гександиола-1 6, триметилолпропана, циклических спиртов циклогек-санола и циклогександиола-1 2 и нормальной валериановой кислоты.
Сильное влияние на скорость реакции этерификации оказывают также пространственные факторы. С увеличением объема связанных с карбоксилом углеводородных радикалов и с повышением объема этерифицируемых спиртов скорость этерификации уменьшается. Среди спиртов одного молекулярного веса быстрее всего взаимодействуют с кислотами первичные, медленнее — третичные спирты.
Для газообразных олефиновых углеводородов скорость реакции этерификации намного отличается при переходе от одного гомолога к другому.
При 100 С константа скорости реакции этерификации равна 4 76 X X 10 — 4 1 / г-мол мин, а для реакции гидролиза эфира она составляет 1.63 X X 10 — 41 / г-жол — мин.
Нитросоединения Нитросоединения алифатического ряда r — nо2
Нитросоединения
–производные углеводородов , в которых
один или несколько атомов водорода
замещены на одну или несколько нитрогрупп.
Нитросоединения
Первичные
Вторичные Третичные
При
рассмотрении строения нитрогруппы
необходимо обратить внимание на то, что
обе
связи в нитрогруппе (N
— О) имеют одинаковое межъядерное
расстояние.
Отрицательный
заряд равномерно распределен между
атомами кислорода. Схематически это
можно отразить следующим образом:
Схематически это
можно отразить следующим образом:
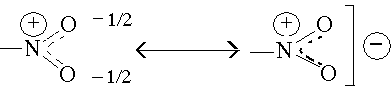
Нитрогруппа,
обладая сильным акцепторным свойством,
придаёт нитросоединениям особые
химические свойства.
Как в
альдегидах и кетонах, смещение электронной
плотности к группе
—NO2
приводит
к увеличению подвижности атомов водорода
в α положении. Подвижностью атомов
водорода обусловлено существование
двух
таутомерных форм
первичных и вторичных нитросоединений
(третичные не обладают этими свойствами,
так как нет подвижного атома Н в α
положении).

За
счёт подвижного атома водорода в α
положении могут идти реакции с азотистой
кислотой с образованием окрашенных
солей, что позволяет использовать эту
реакцию для качественного обнаружения
первичных и вторичных нитросоединений:

Псевдонитролы
в растворах и расплавах окрашены в синий
или зеленовато — синий цвет, соли —
бирюзового цвета.
Ароматические
нитросоединения
Нитрогруппа
в
ядре в
боковой цепи

Химические
свойства
Для
ароматических нитросоединений характерны
реакции восстановления и замещения.
Восстановление
Наиболее
важное свойство нитрогруппы:
В
зависимости от условий восстановления
(нейтральная, щелочная или слабокислая
среда) получается широкий спектр
ароматических аминов, применяемых при
производстве красителей, лекарств,
фото химикатов. (Этот материал следует
смотреть в учебнике Петрова А.А.)
Замещение
а)
Реакции
электрофильного замещения SЕ
.Нитрогруппа
— ориентант II
рода, затрудняет вступление нового
заместителя в ядро, ориентирует его
в мета — положение.

б)
Реакции нуклеофильного замещения SN.
Группа
—NO2
способствует вступлению заместителя
в ядро и направляет его в орто- и
пара-положение:
Нитрогруппа
оказывает значительное влияние на
свойства других функциональных групп:
1.
Увеличивает подвижность галогена в
ароматическом кольце (пособие кафедры:
Методы синтеза органических соединений,
тема 1, галогенирование стр.23)
2.
Влияет на кислые свойства фенолов.
3.
Влияет на основные свойства аминов.
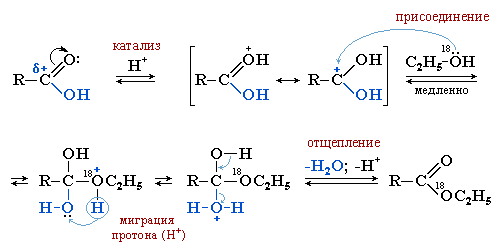
Реакция — этерификация
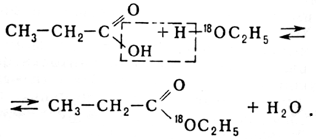
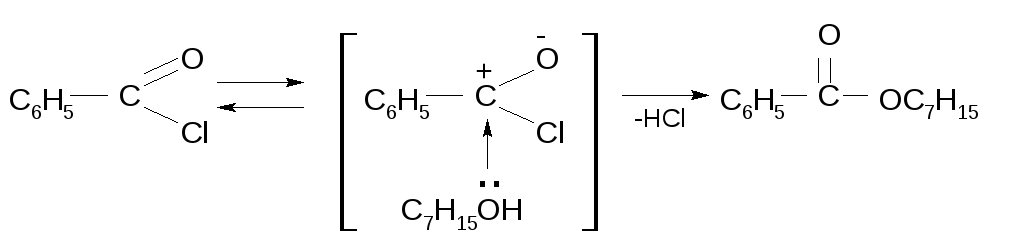
Реакция этерификации идет иным путем. Спирт в большинстве случаев реагирует, отдавая не гидроксил ( как щелочь при нейтрализации), а водород гидроксильной группы; кислоты ( органические и некоторые, по не все, минеральные) отдают свой гидроксил.
Реакции этерификации обратимы и, следовательно, ограничены состоянием равновесия. Превращение эквимолекулярных количеств кислоты и спирта в теоретически вычисленное количество сложного эфира по причине обратимости реакции невозможно. В результате реакции образуется некоторое максимальное количество эфира ( которое всегда ниже теоретического) и остаются непрореагировавшие спирт и кислота.
Реакция этерификации очень ускоряется в присутствии катализаторов — ионов водорода. Для этого через реакционную смесь пропускают газообразный хлористый водород ( 3 %), или, чаще, прибавляют концентрированную серную кислоту. Реакция получения уксусноэтилового эфира, которая без катализаторов идет несколько дней, в присутствии НС1 или H2SO4 требует лишь нескольких часов.
Реакция этерификации, а также образующиеся в результате ее сложные эфиры иыеют огромное значение и будут в дальнейшем предметом специального рассмотрения.
Реакция этерификации сильно ускоряется в присутствии катализаторов — ионов водорода. Практически для этого в реакционную смесь пропускают газообразный хлористый водород ( в количестве 3 %) или, чаще, прибавляют концентрированную серную кислоту. Упомянутая выше реакция получения уксусноэтилового эфира, которая без катализаторов идет несколько дней, в присутствии HG1 или H2S04 требует лишь нескольких часов.
Реакции этерификации, а также образующиеся в результате ее сложные эфиры имеют огромное значение и будут в дальнейшем предметом специального рассмотрения.
Реакция этерификации сильно ускоряется в присутствии катализаторов — водородных ионов. Практически для этого в реакционную смесь пропускают газообразный хлористый водород ( в количестве 3 %) или, чаще, прибавляют концентрированую серную кислоту. Реакция получения уксусноэтилового эфира требует без катализаторов несколько дней, в присутствии НС1 или H2SO4 — лишь несколько часов.
Реакция этерификации сильно ускоряется в присутствии катализаторов — водородных ионов. Практически для этого в реакционную смесь пропускают газообразный хлористый водород или, чаще, прибавляют концентрированную серную кислоту. Реакция получения уксусноэтило-вого эфира требует без катализаторов несколько дней, в присутствии НС1 или H2S04 — лишь несколько часов.
Реакция этерификации, а также образующиеся в результат ее эфиры имеют огромное значение, поэтому в дальнейшем эт-с реакция будет рассмотрена подробнее ( см. стр.
Реакции этерификации являются обратимыми реакциями.
Реакции этерификации характерны не только для карбоновых, но и для минеральных кислот.
Реакции этерификации являются обратимыми реакциями.
Реакция этерификации является обратимой.
Реакция этерификации играет важную роль в органической химии, и мы рассмотрим ее более подробно при изучении сложных эфиров.
Реакция этерификации для большинства гидро-ксильных групп протекает специфично и быстро, поэтому реагент можно определить легко и точно. Эта реакция обратима, провести ее количественно можно лишь в отсутствие воды. Поэтому вода извлекается из реакционной смеси с помощью ангидридов карбо-новых кислот, например уксусного или фталевого.
Что такое трансэтерификация
Переэтерификация представляет собой обмен алкильной группы, присоединенной к атому кислорода сложного эфира, на алкильную группу спирта. Эта реакция требует кислотных или основных катализаторов, чтобы уменьшить энергию активации реакции.
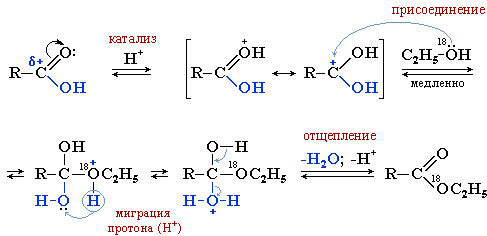
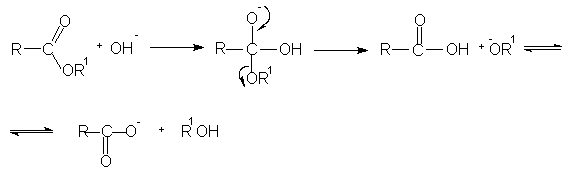
Механизм
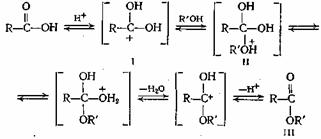
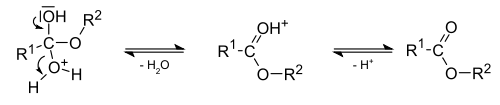
Переэтерификация эфира начинается с нуклеофильной атаки алкоголя. Спирт, удаляя протон, присоединенный к атому кислорода, становится нуклеофилом из-за наличия неподеленных электронных пар. Этот нуклеофил может атаковать атом углерода, который присоединен к двум атомам кислорода. Атом углерода получает частичный положительный заряд, потому что два атома кислорода притягивают электроны связи к себе, так как сродство к электрону у атомов кислорода выше, чем у атома углерода. Таким образом, этот углерод с частичным положительным зарядом является хорошим местом для атаки нуклеофилов.
Рисунок 02: Реакция переэтерификации
Это образует промежуточную молекулу, которая состоит из сложного эфира и спирта, связанных с атомом углерода (с частичным положительным зарядом) через его кислород. Поскольку этот промежуточный продукт нестабилен, происходит перегруппировка. Там группа -OR карбоновой кислоты удаляется. Но спиртовая группа остается связанной с углеродом. Теперь, новый эфир сформирован.
Этот механизм используется в производстве полиэстера.