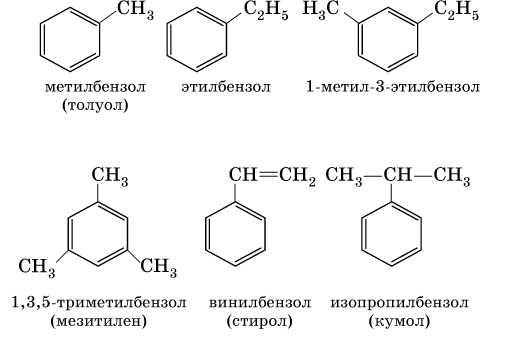
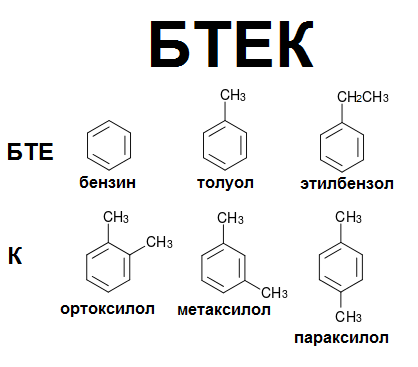
Токсикология и метаболизм
Экологические и токсикологические эффекты толуола широко изучены. В 2013 году мировые продажи толуола составили около 24,5 миллиардов долларов США. Вдыхание толуола в низких или умеренных количествах может вызвать усталость, спутанность сознания, слабость, действия в состоянии опьянения, потерю памяти, тошноту, потерю аппетита, потерю слуха и потерю цветового зрения. Некоторые из этих симптомов обычно исчезают при прекращении воздействия. Вдыхание большого количества толуола за короткое время может вызвать головокружение, тошноту или сонливость, потерю сознания и даже смерть . Толуол, однако, намного менее токсичен, чем бензол , и, как следствие, в значительной степени заменил его в качестве ароматического растворителя при химическом получении. Агентство США по охране окружающей среды (EPA) утверждает , что канцерогенный потенциал толуола не может быть оценена из — за недостатка информации.
Как и во многих других растворителях , таких как 1,1,1-трихлорэтан и некоторых алкильных бензолы , толуол было показано, действуют в качестве неконкурентного антагониста рецептора NMDA и ГАМК А рецептора положительного аллостерического модулятора . Кроме того, было показано, что толуол проявляет антидепрессантные эффекты у грызунов в тесте принудительного плавания (FST) и тесте подвешивания за хвост (TST), вероятно, из-за его свойств антагониста NMDA.
Толуол иногда используется как рекреационный ингалятор («нюхание клея»), вероятно, из-за его эйфорического и диссоциативного эффекта.
Толуол ингибирует возбуждающие ионные каналы, включая глутамат N-метил-D-аспартата (NMDA) и никотиновые ацетилхолиновые рецепторы (nAChR), и потенцирует функцию ингибирующих ионных каналов, таких как рецепторы гамма-аминомасляной кислоты типа A, рецепторы глицина и серотонина. Кроме того, толуол разрушает потенциал-управляемые кальциевые каналы и АТФ-управляемые ионные каналы.
Рекреационное использование
Толуол используется как опьяняющее средство для ингаляции способом, не предусмотренным производителями. Люди вдыхают продукты, содержащие толуол (например, разбавитель для краски , контактный цемент , клей для моделей и т. Д.) Из-за их опьяняющего действия . Владение и использование толуола и продуктов, содержащих его, регулируются во многих юрисдикциях по той причине, что якобы препятствует тому, чтобы несовершеннолетние могли получить эти продукты для употребления наркотиков . По состоянию на 2007 год в 24 штатах США действовали законы, предусматривающие наказание за использование, хранение с намерением использовать и / или распространение таких ингалянтов. В 2005 году Европейский Союз запретил общую продажу продуктов, содержащих более 0,5% толуола.
Биоремедиация
Несколько типов грибов, включая Cladophialophora , Exophiala , Leptodontium , Pseudeurotium zonatum и Cladosporium sphaerospermum , а также некоторые виды бактерий могут разлагать толуол, используя его в качестве источника углерода и энергии.
Толуол и бензол
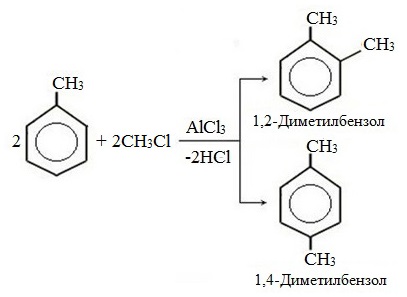
Поскольку эти два вещества похожи, стоит выполнить сравнение химических свойств. Бензол и толуол оба вступают в реакции замещения. Однако скорости их протекания отличаются. Поскольку в молекуле толуола метальная группа влияет на ароматическое кольцо, он реагирует быстрее.
Но бензол, в свою очередь, проявляет устойчивость к окислению. Так, например, когда на него воздействует перманганат калия, ничего не происходит. Зато толуол при такой реакции образует бензойную кислоту, о чем уже упоминалось ранее.
В то же время, известно, что предельные углеводороды не реагируют с раствором калиевого перманганата. Так что окисление толуола объясняется влиянием, оказываемым бензольным кольцом на метильную группу. Данное утверждение подтверждается теорией Бутлерова. В соответствии с ней атомы и их группы в молекулах оказывают взаимное влияние.
Использует
Прекурсор бензола и ксилола
Толуол в основном используется в качестве предшественника бензола путем :
- С 6 Н 5 СН 3 + Н 2 → С 6 Н 6 + СН 4
Вторая по значению заявка связана с его диспропорционированием до смеси бензола и ксилола .
Нитрация
Нитрование толуола дает моно-, ди- и тринитротолуол, все из которых широко используются. Динитротолуол является предшественником толуолдиизоцианата , который используется при производстве пенополиуретана . Тринитротолуол — это взрывчатое вещество, обычно сокращенно ТНТ.
Окисление
Бензойная кислота и бензальдегид производятся в промышленных масштабах путем частичного окисления толуола кислородом . Типичные катализаторы включают нафтенаты кобальта или марганца .
Растворитель
Толуол является обычным растворителем , например, для красок , разбавителей красок, силиконовых герметиков, многих химических реагентов , резины , типографской краски, клеев (клеев), лаков , средств для кожевенной обработки и дезинфицирующих средств .
Топливо
Толуол может быть использован в качестве октанового числа в бензине топлива для двигателей внутреннего сгорания , а также топливо для реактивных двигателей . Толуол в количестве 86% по объему заправлял все двигатели с турбонаддувом в Формуле-1 в 1980-х годах, впервые разработанные командой Honda . Остальные 14% был «наполнитель» из н — гептана , чтобы уменьшить октановое число , чтобы удовлетворить Формулы Один ограничений на топливо. 100% толуол можно использовать в качестве топлива как для двухтактных, так и для четырехтактных двигателей ; однако из-за плотности топлива и других факторов топливо не испаряется легко, если его предварительно не нагреть до 70 ° C (158 ° F). Honda решила эту проблему в своих автомобилях Формулы-1, пропустив топливопроводы через теплообменник , используя энергию воды в системе охлаждения для нагрева топлива.
В Австралии в 2003 году было обнаружено, что толуол незаконно смешивался с бензином в топливных точках для продажи в качестве стандартного автомобильного топлива. Толуол не облагается акцизным налогом на топливо, тогда как другие виды топлива облагаются налогом более 40%, что обеспечивает более высокую норму прибыли для поставщиков топлива. Степень замещения толуола не определена.
Нишевые приложения
В лаборатории толуол используется в качестве растворителя для углеродных наноматериалов, включая нанотрубки и фуллерены, а также его можно использовать в качестве индикатора фуллерена . Толуольный раствор C 60 имеет ярко-фиолетовый цвет. Толуол используется в качестве цемента для комплектов тонкого полистирола (путем растворения, а затем сплавления поверхностей), так как его можно очень точно наносить кистью и не содержит основной массы клея. Толуол можно использовать для разрушения красных кровяных телец с целью извлечения гемоглобина в биохимических экспериментах. Толуол также использовался в качестве хладагента из-за его хороших способностей к теплопередаче в натриевых холодных ловушках, используемых в контурах системы ядерных реакторов. Толуол также использовался в процессе удаления кокаина из листьев коки при производстве сиропа Coca-Cola.
Основные химические свойства
Толуол – это вещество, которому свойственны реакции электрофильного замещения. Они происходят в так называемом ароматическом кольце, проявляющим анормально высокую стабильность. Эти реакции идут, в основном, в пара- и орто-положениях относительно метильной группы -CH3.
Относятся к химическим свойствам толуола реакции озонолиза и присоединения (гидрирование). Под воздействием некоторых окислителей метильная группа становится карбоксильной. Чаще всего для этого используется щелочной раствор калийного перманганата или неконцентрированная азотная кислота.
Еще стоит отметить, что толуол способен самовоспламеняться. Для этого необходима температура в 535 °C. Вспышка происходит при 4 °C.

Химические свойства
Толуол реагирует как обычный ароматический углеводород при электрофильном ароматическом замещении . Поскольку метильная группа имеет более высокие свойства высвобождения электронов, чем атом водорода в том же положении, толуол более реактивен, чем бензол, по отношению к электрофилам. Она подвергается сульфирование с получением п — толуолсульфоновую кислоту , и хлорирование с помощью Cl 2 в присутствии FeCl 3 с получением орто- и пара — изомеров из хлортолуол .
Важно отметить, что боковая метильная цепь в толуоле подвержена окислению. Толуол реагирует с перманганатом калия с образованием бензойной кислоты и с хромилхлоридом с образованием бензальдегида ( реакция Этара ).. Метильная группа подвергается галогенированию в условиях свободных радикалов
Например, N- бромсукцинимид (NBS), нагретый с толуолом в присутствии AIBN, приводит к бензилбромиду. Такое же преобразование можно осуществить с элементарным бромом в присутствии ультрафиолетового света или даже солнечного света. Толуол также можно бромировать, обрабатывая его HBr и H 2 O 2 в присутствии света.
Метильная группа подвергается галогенированию в условиях свободных радикалов . Например, N- бромсукцинимид (NBS), нагретый с толуолом в присутствии AIBN, приводит к бензилбромиду . Такое же преобразование можно осуществить с элементарным бромом в присутствии ультрафиолетового света или даже солнечного света. Толуол также можно бромировать, обрабатывая его HBr и H 2 O 2 в присутствии света.
- C 6 H 5 CH 3 + Br 2 → C 6 H 5 CH (Br) 2 + HBr
- C 6 H 5 CH 2 Br + Br 2 → C 6 H 5 CHBr 2 + HBr
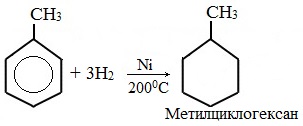
Метильная группа в толуоле подвергается депротонированию только очень сильными основаниями, ее pK a оценивается примерно 41. Полное гидрирование толуола дает метилциклогексан . Реакция требует высокого давления водорода и катализатора .
Профессиональные вредности
Толуол, как и другие ароматические углеводороды (см.), применяется в промышленности в качестве органического растворителя (см. Растворители). В организм контактирующих с ним он может попадать через органы дыхания, частично — через неповрежденную кожу. Высокая растворимость Т. в жирах и липидах способствует его накоплению в клетках ц. н. с., что определяет нек-рое наркотическое действие Т. Способность Т. изменять свойства биол. мембран (см. Мембраны биологические) также объясняется его высокой растворимостью в липидах. Это свойство Т. лежит в основе патогенеза проф. патологии, отмечаемой при интоксикациях Т.
Хрон. интоксикации Т. в производственных условиях наблюдают редко. При этом в клин, картине преобладают изменения системы крови с активацией процессов эритропоэза и тромбоцитопоэза. В крови отмечают тенденцию к эритроцитопении и ретикулоцитозу, связанную с сокращением продолжительности жизни эритроцитов, цитоплазматическая мембрана к-рых повреждается Т. У женщин при продолжительном (10—15 лет) контакте с Т. возможно развитие умеренной железодефицитной анемии, нередко сочетающейся с патологией половых органов. Прекращение контакта с Т. и своевременная терапия приводят к нормализации картины крови, что подтверждает роль профессионального фактора в ее патол. изменении. Наблюдаемые нарушения со стороны нервной системы характеризуются симптомами астеновегетативного или астеноневротического синдрома (см. Астенический синдром). Как правило, они мало выражены и сочетаются с другими проявлениями интоксикации. Изменения кожи при контакте с Т. чаще всего носят характер дерматита в виде сухости и трещин кожи. В редких случаях развивается контактная экзема (см.) или меланоз (см.).
Лечение при хрон. интоксикациях Т. симптоматическое.
Острые интоксикации Т. наблюдают лишь в аварийных ситуациях. Клин, проявлениями острого отравления Т. являются эйфория, головная боль, тошнота, рвота.
Первая помощь и неотложная терапия при остром отравлении Т. заключаются в немедленном прекращении контакта пострадавшего с Т.— пострадавшего необходимо вынести или вывести на свежий воздух, обеспечить ему покой, тепло, дать сердечные и успокаивающие средства (бромиды, препараты валерианы). Применение адреналина и адреномиметиков противопоказано. Дальнейшее лечение — симптоматическое. Госпитализация требуется редко.
Вопросы экспертизы трудоспособности, медицинской и трудовой реабилитации при интоксикациях Т. решаются с учетом выраженности клин, симптомов интоксикации и гиг. характеристики условий труда (см. Экспертиза).
Меры профилактики отравления Т.: обеспечение герметизации оборудования на соответствующих производствах и приточно-вытяжной вентиляции (см.) производственных помещений, контроль воздушной среды, использование противогазов (см.), спецодежды (см. Одежда специальная), соблюдение мер личной гигиены, проведение периодических мед. осмотров (см. Медицинский осмотр) 1 раз в 12 мес.
Предельно допустимая концентрация паров Т. 50 мг/м3.
Библиогр.: Вредные вещества в промышленности, под ред. Н. В. Лазарева и Э. Н. Левиной, т. 1, с. 98, Л., 1976; Грибова И. А. и др. Состояние системы крови у рабочих, имеющих контакт с толуолом, Гиг. труда и проф. заболев., JNS 10, с. 6, 1975; Каррер П. Курс органической химии, пер. с англ., Л., 1960; Руководство по профессиональным заболеваниям, под ред. Н. Ф. Измерова, т. 1, М., 1983; Соколов В. В. и др. Структурно-функциональные особенности мембран эритроцитов при воздействии толуола, Гиг. труда и проф. заболев., № 1, с. 27, 1981; Хаген И. Клиника профессиональных заболеваний, пер. с нем., Л., 1961.
Химические свойства толуола
Все реакции толуола (метилбензола) можно подразделить на два типа: реакции, затрагивающие бензольное кольцо и реакции, затрагивающие метильную группу.
Реакции замещения
1. Реакции с участием бензольного кольца
Метилбензол вступает во все реакции замещения, в которых участвует бензол, и проявляет при этом более высокую реакционную способность, реакции протекают с большой скоростью.
Метильный радикал, содержащийся в молекуле толуола, является ориентантом I рода, поэтому в результате реакций замещения в бензольном ядре получаются орто- и пара- производные толуола или при избытке реагента – трипроизводные общей формулы:
а) галогениерование
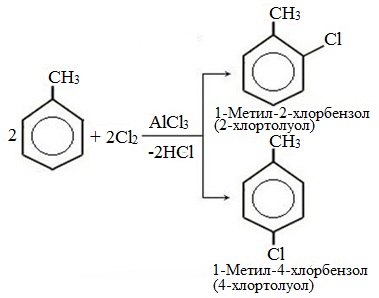
При избытке галогена можно получить ди- и три-замешенные производные в соответствии с правилами ориентации:
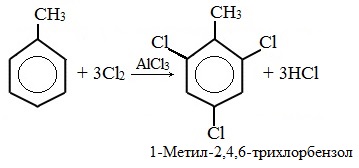
б) нитрование
Например, при нитровании толуола С6Н5CH3 (70°С) происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:

Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества. С одной стороны, метильная группа СH3 (за счет +I-эффекта) повышает электронную плотность в бензольном кольце в положениях 2, 4 и 6 и облегчает замещение именно в этих положениях:
С другой стороны, под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH4.
в) сульфирование
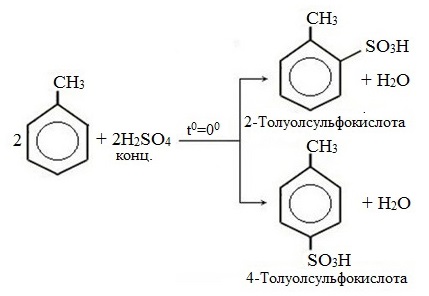
г) алкилирование

2. Реакции с участием боковой цепи
Метильная группа в метилбензоле может вступать в реакции, характерные для алканов:
Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуется радикал бензил ·CH2-C6H5. Он более стабилен, чем алкильные свободные радикалы (·СН3, ·СH2R), т.к. его неспаренный электрон делокализован за счет взаимодействия с π- электронной системой бензольного кольца:
а) гидрирование
Реакции окисления
а) горение
б) неполное окисление
В отличие от бензола его гомологи подвергаются окислению легче предельных углеводородов. При этом окислению подвергаются лишь радикалы, связанные с бензольным кольцом, в случае толуола — метильная группа. Мягкие окислите (MnО2) окисляют ее до альдегидной группы, более сильные окислители (KMnO4) вызывают дальнейшее окисление до кислоты:
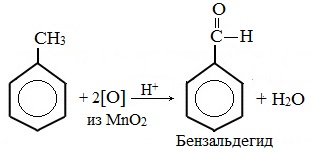

Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO4 при нагревании).
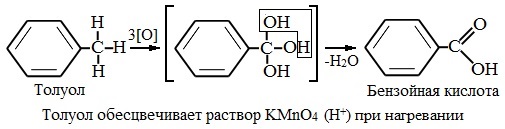
Любой гомолог бензола с одной боковой цепью окисляется KMnO4 и другим сильным окислителем в бензойную кислоту:
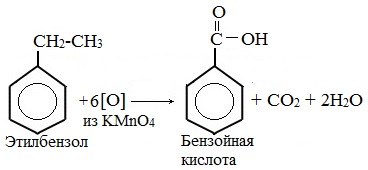
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:

Рубрики: Арены Теги: Толуол
Толуол — растворитель и разбавитель
Самым большим спросом толуол пользуется как растворитель и разбавитель разных химических веществ. Прежде всего, стоит понять, чем отличается разбавитель от растворителя. Разбавители снижают вязкость лакокрасочных материалов (ЛКМ), применяются для лаков, и красок. Сейчас этим терминов пользуются крайне редко, чаще можно услышать «растворитель». Растворители придают ЛКМ определенной консистенции, растворяют твердые вещества (засохший лак). Толуол растворяет полистирол, эфиры целлюлозы, а также виниловые и акрилатные полимеры. Полиэтилен он растворяет только в горячем виде. Он входит в состав таких растворителей: P4, 645, 647, 648.
Химическое вещество – толуол не столь токсичен, как бензол. Именно поэтому его сфера применения так обширна. Он используется в органическом синтезе, в парфюмерно – косметологической, военной, топливной, фармацевтической, лакокрасочной промышленности. Толуол есть в свободной продаже и его можно использовать в быту, как разбавитель.
Реакции присоединения
Бензол присоединяет хлор на свету и водород при нагревании в присутствии катализатора.
1.1. Гидрирование
Бензол присоединяет водород при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt и др.).
При гидрировании бензола образуется циклогексан:
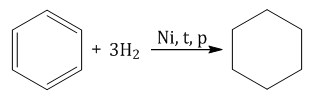
При гидрировании гомологов образуются производные циклоалканы. При нагревании толуола с водородом под давлением и в присутствии катализатора образуется метилциклогексан:
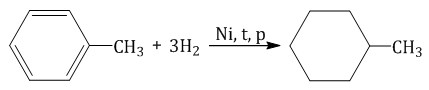
1.2. Хлорирование аренов
Присоединение хлора к бензолу протекает по радикальному механизму при высокой температуре, под действием ультрафиолетового излучения.
При хлорировании бензола на свету образуется 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран).
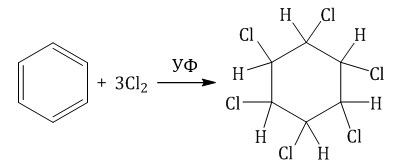
Гексахлоран – пестицид, использовался для борьбы с вредными насекомыми. В настоящее время использование гексахлорана запрещено.
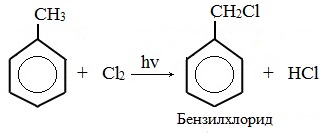
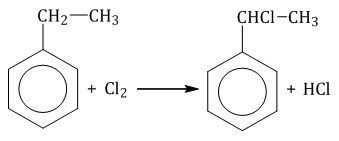
Гомологи бензола не присоединяют хлор. Если гомолог бензола реагирует с хлором или бромом на свету или при высокой температуре (300°C), то происходит замещение атомов водорода в боковом алкильном заместителе, а не в ароматическом кольце.
| Например, при хлорировании толуола на свету образуется бензилхлорид |

| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
| Например, этилбензол реагирует с хлором на свету |
Опасность для человека
Характеристики и химические свойства толуола определяют его токсичность. Как уже было сказано, его пары оказывают наркотическое воздействие. Оно особенно сильно в повышенных концентрациях. У человека, вдохнувшего пары, появляются сильные галлюцинации. Мало кто знает, но до 1998 года это вещество входило в состав клея «Момент». Именно поэтому он был так популярен среди токсикоманов.
Высокие концентрации данного вещества также отрицательно влияют на нервную систему, слизистые оболочки глаз, кожу. Нарушается функция кроветворения, поскольку толуол – это высокотоксичный яд. Из-за этого может возникнуть такие заболевания, как гипоксия и цианоз.
Существует даже понятие толуольной токсикомании. Она имеет и канцерогенное влияние. Ведь пару, попадая через кожу или органы дыхания в организм человека, поражают нервную систему. Порой, данные процессы обратить невозможно.
Кроме того, пары могут вызвать заторможенность и нарушить работу вестибулярного аппарата. Поэтому люди, работающие с данным веществом, трудятся в хорошо проветриваемых помещениях, обязательно под тягой, и используют специальные резиновые перчатки.

Пожарная опасность
Нельзя не упомянуть и о ней, рассказывая про химические и физические свойства толуола. Ведь это очень огнеопасное вещество.
Оно относится к классу 3,1 легковоспламеняющихся жидкостей. В эту же категорию входит дизельное топливо, газойль, десенсибилизированные взрывчатые соединения.
Нельзя допускать возникновения рядом с толуолом открытого огня, курения, искр. Даже смесь паров этого вещества с воздухом является взрывоопасной
Если выполняются сливно-наливные операции, то соблюдение правил защиты от статического электричества приобретает первостепенную важность
Производственные помещения, предназначенные для проведения работ, связанных с толуолом, обеспечиваются приточно-вытяжной вентиляцией, а техника – отсосами. Запрещен использование инструментов, которые могут при ударе дать искру. А если происходит возгорание вещества, то тушить его нужно лишь тонкораспыленной водой, воздушно-механической или химической пеной. Разлитый толуол обезвреживают песком.
Токсичность
Толуол — токсичное вещество, его ПДК в воздухе рабочей зоны в РФ составляет 50 мг/м3 (среднесменная, за 8 часов) и 150 мг/м3 (максимально-разовая). А порог восприятия запаха этого вещества может составлять (в среднем, в группе людей) ~ 260 мг/м3, и даже ~ 590 мг/м3; причём у отдельных людей он может быть значительно больше среднего значения. Поэтому можно ожидать, что использование широко распространённых в сочетании с «заменой по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками) приведёт к чрезмерному воздействию паров толуола на, по крайней мере, часть работников — из-за запоздалой замены противогазных фильтров. Поэтому для защиты от толуола следует использовать более эффективные технологии и средства коллективной защиты.
Толуол влияние на организм человека

Толуол – токсичный продукт (класс опасности – третий). Пары толуола при высоких концентрациях оказывают наркотическое воздействие на человека, вызывая сильные галлюцинации. До 1998 года толуол входил в состав популярного клея «Момент», из-за чего пользовался популярностью у токсикоманов.
Повышенные концетрации паров толуола также оказывают вредное влияние на нервную систему человека, раздражающе действуют на кожу, а также на слизистые оболочки глаз. Являясь сильно токсичным ядом, он влияет на функцию кроветворения организма.
Результатом нарушения кроветворения являются такие заболевания, как цианоз, гипоксия. Существует толуольная токсикомания, одновременно имеющая и канцерогенное влияние.
Пары проникают через органы дыхания или неповрежденную кожу, вызывают поражение нервной системы (наблюдается заторможенность и нарушения работы вестибулярного аппарата). Иногда эти процессы необратимые.
Пары толуола могут проникать через неповрежденную кожу и органы дыхания, вызывая поражение нервнойсистемы (заторможенность, нарушения в работе вестибулярного аппарата). Поэтому работать с толуолом и растворителями на его основе необходимо в стойких к их воздействию резиновых перчатках, обязательно под тягой и в хорошо проветриваемом помещении.
Молярная масса
92,14 г/моль
Плотность
0,86694 г/см³
Т. плав.
−95 ℃
Т. кип.
110,6 ℃
Кр. точка
320 °C (593 K), 4299 кПа
Удельная теплота испарения
364 кДж/кг
Растворимость в воде
14 мг/100 мл
Номер CAS
108-88-3
PubChem
1140
ChemSpider
1108
Номер EINECS
203-625-9
RTECS
XS5250000
ChEBI
17578
DrugBank
DB11558
Приводятся данные для стандартных условий (25 ℃, 100 кПа), если не указано иное.
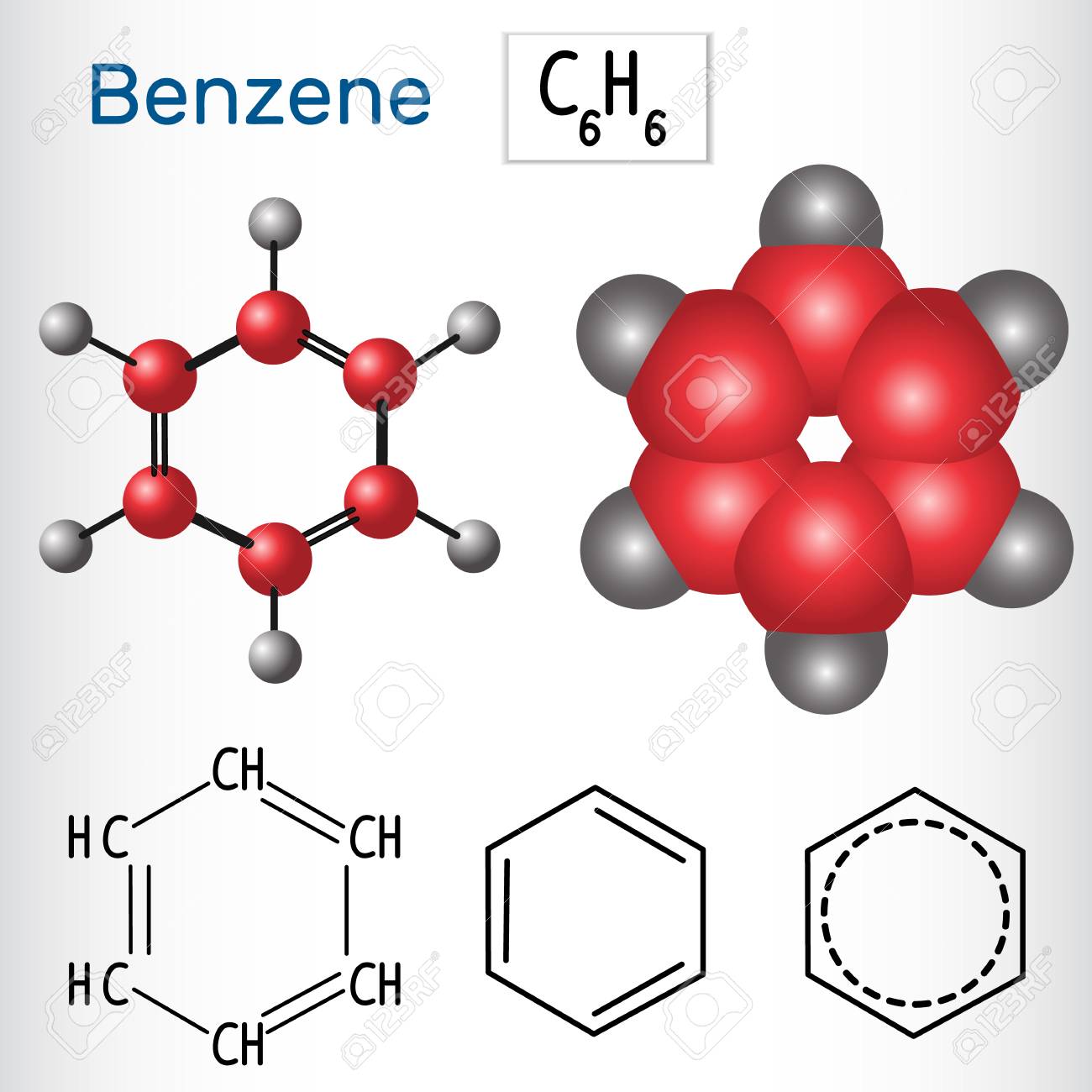
Толуо́л (от исп. Tolu , толуанский бальзам) — метилбензол, PhMe — бесцветная жидкость с характерным запахом, относится к аренам.
Толуол получен впервые П. Пеллетье в 1835 при перегонке сосновой смолы. В 1838 выделен А. Девилем из бальзама, привезенного из города Толу в Колумбии, в честь которого получил своё название .
Общая характеристика
Бесцветная подвижная летучая жидкость с резким запахом, проявляет слабое наркотическое действие. Смешивается в неограниченных количествах с углеводородами, многими спиртами, простыми и сложными эфирами, не смешивается с водой. Показатель преломления света 1,4969 при 20 °C. Горюч, сгорает коптящим пламенем.
Химические свойства
Для толуола характерны реакции электрофильного замещения в ароматическом кольце и замещения в метильной группе по радикальному механизму.
Электрофильное замещение в ароматическом кольце идёт преимущественно в орто- и пара-положениях относительно метильной группы.
Кроме реакций замещения, толуол вступает в реакции присоединения (гидрирование), озонолиза. Некоторые окислители (щелочной раствор перманганата калия, разбавленная азотная кислота) окисляют метильную группу до карбоксильной. Температура самовоспламенения 535 °C. Температура вспышки 4 °C.
При взаимодействии толуола с сильными окислителями образуется бензойная кислота:
Взаимодействие с перманганатом калия в кислой среде:
5 C 6 H 5 C H 3 + 6 K M n O 4 + 9 H 2 S O 4 → → 5 C 6 H 5 C O O H + 6 M n S O 4 + 3 K 2 S O 4 + 14 H 2 O .
Взаимодействие с перманганатом калия в нейтральной среде
C 6 H 5 C H 3 + 2 K M n O 4 → C 6 H 5 C O O K + 2 M n O 2 + K O H + H 2 O >
Взаимодействие с галогенами на свету
C 6 H 5 C H 3 + X 2 → h ν C 6 H 5 C H 2 X + H X >
Получение и очистка
Продукт каталитического риформинга бензиновых фракций нефти. Выделяется селективной экстракцией и последующей ректификацией.Также хорошие выходы достигаются при каталитическом дегидрировании гептана через метилциклогексан.
Очищают толуол аналогично бензолу, только в случае применения концентрированной серной кислоты следует учитывать, что толуол сульфируется легче бензола, а, значит, необходимо поддерживать более низкую температуру реакционной смеси (практически — менее 30 °C).
Толуол также образует с водой азеотропную смесь .
Толуол можно получить из бензола по реакции Фриделя — Крафтса с использованием трибромида железа в качестве катализатора:
C 6 H 6 + C H 3 B r → F e B r 3 C 6 H 5 C H 3 + H B r >>
Применение
Сырьё для производства бензола, бензойной кислоты, нитротолуолов (в том числе тринитротолуола), толуилендиизоцианатов (через динитротолуол и толуилендиамин) бензилхлорида и др. органических веществ.
Является растворителем для многих полимеров, входит в состав различных товарных растворителей для лаков и красок. Входит в состав растворителей: Р-40, Р-4, 645, 646, 647, 648. Применяется как растворитель в химическом синтезе.
Ориентирующее действие заместителей в бензольном кольце
Если в бензольном кольце имеются заместители, не только алкильные, но и содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции замещения атомов водорода в ароматической системе протекают строго определенным образом, в соответствии с характером влияния заместителя на ароматическую π-систему.
Типы заместителей в бензольном кольце
| Заместители первого рода | Заместители второго рода |
| Дальнейшее замещение происходит преимущественно в орто— и пара-положение | Дальнейшее замещение происходит преимущественно в мета-положение |
| Электронодонорные, повышают электронную плотность в бензольном кольце | Электроноакцепторные, снижают электронную плотность в сопряженной системе. |
|
|
| Например, толуол реагирует с хлором в присутствии катализатора с образованием смеси продуктов, в которой преимущественно содержатся орто-хлортолуол и пара-хлортолуол. Метильный радикал — заместитель первого рода. |

В уравнении реакции в качестве продукта записывается либо орто-толуол, либо пара-толуол.
| Например, при бромировании нитробензола в присутствии катализатора преимущественно образуется мета-хлортолуол. Нитро-группа — заместитель второго рода |

История
Впервые это соединение было выделено в 1837 году путем перегонки соснового масла польским химиком Филипом Вальтером , который назвал его ретиннафтом . В 1841 году французский химик Анри Этьен Сент-Клер Девиль выделил углеводород из бальзама Толу (ароматический экстракт тропического колумбийского дерева Myroxylon balsamum ), который Девиль признал сходным с ретиннафтом Вальтера и бензолом; отсюда он назвал новый углеводород бензоэном . В 1843 году Йенс Якоб Берцелиус рекомендовал название толуин . В 1850 году французский химик Огюст Каур выделил из древесного дистиллята углеводород, который он признал похожим на бензоен Девиля и который Каур назвал толуеном .
Что такое толуол?
Толуол (метилбензол) – это прозрачная жидкость с резким характерным запахом. Толуол не смешивается с водой, легко воспламеняется и горит коптящим пламенем, а также не вступает в реакции с кислотами и основаниями. Это продукт переработки нефти. Впервые был получен из толуанского бальзамала, который привезли из города Толу, отсюда и название – толуол. Пары толуола токсичны. Они несут опасность для человека в том случае, если длительно вдыхать вещества, содержащие толуол или если работать с такими веществами без надлежащей защиты. В остальных случаях толуол безопасен и имеет широкую сферу применения.
Токсичность толуола
Метилбензол является пожароопасным веществом. Паровоздушная смесь при определенных условиях взрывается. Легко воспламеняется жидкий толуол. Структурная формула дает представление о составе и строении, но не содержит информации о действии вещества на организм человека. Установлено, что толуол является токсичным, обладает канцерогенным действием. Пары метилбензола свободно проникают через кожу, органы дыхания, вызывают изменения в центральной нервной системе, раздражение покровных тканей, дерматит. При вдыхании испарений толуола у человека проявляется заторможенность, тремор, нарушается деятельность вестибулярного аппарата. Работать с толуолом, красками, растворителями нужно в резиновых перчатках, тщательно проветривать помещение либо использовать вытяжку. Метилбензол является слабым наркотическим веществом, вызывает толуольную токсикоманию. Другие формы негативного воздействия вещества:
- раздражение глаз и нарушение цветового зрения;
- длительное воздействие может привести к потере слуха;
- высокая концентрация в крови вызывает поражение печени, некроз почек;
- вдыхание большого количества паров приводит к головокружению, сонливости, головной боли.
Что такое толуол?
Один из важнейших аренов — толуол — представляет собой метильное производное бензола. Нерастворимая в воде бесцветная жидкость обладает сладковатым ароматом, напоминающим запах красок, лаков, растворителей.
Химическая формула толуола — C7H8 — может быть записана по-другому: C6H5–CH3. В этом случае количество атомов остается таким же, но заметно отличие от бензола, которое заключается в радикале — метиле.
Используя другие принципы номенклатуры, соединение называют метилбензолом и фенилметаном. Это тот же толуол, общая формула которого C7H8. Но в первом случае акцент делается на том, что один атом водорода из тех, что связаны с углеродом бензольного кольца, замещен на радикал метил. Для второго названия избран другой подход. Считается, что в метане один водород замещается на радикал фенил. Это частица, в которую превращается бензол, отдавая атом водорода.
Производство
Толуол в естественных условиях содержится в сырой нефти в небольших количествах и является побочным продуктом при производстве бензина на установке каталитического риформинга или крекинг- установке этилена . Это также побочный продукт производства кокса из угля . Окончательное разделение и очистка осуществляется с помощью любого из процессов дистилляции или экстракции растворителем, используемых для ароматических углеводородов БТК (бензол, толуол и изомеры ксилола).
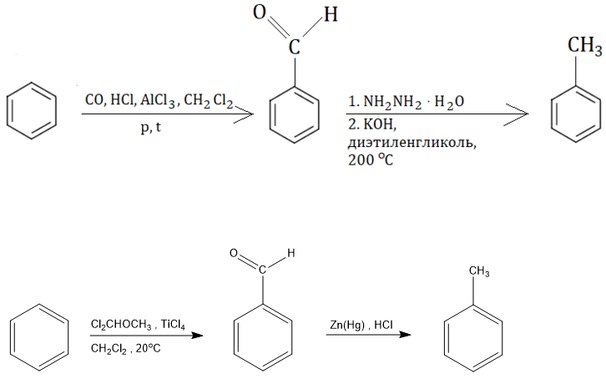
Лабораторная подготовка
Толуол дешево производится промышленным способом. В принципе, его можно приготовить разными способами. Например, хотя бензол представляет только дидактический интерес, он реагирует с метилхлоридом в присутствии кислоты Льюиса, такой как хлорид алюминия, с образованием толуола:
- C 6 H 5 H + CH 3 Cl → C 6 H 5 CH 3 + HCl
Такие реакции осложняются полиметилированием, поскольку толуол более подвержен алкилированию, чем бензол.
Заключение
Толуол в больших количествах производится на нефтехимических заводах или получается в качестве побочного продукта на коксовых предприятиях. Соединение является ценным сырьем для масштабного органического синтеза, используется в фармацевтической промышленности. Входит метилбензол в состав многих видов растворителей, которые применяются в работе с лакокрасочными материалами. Толуол относится в классификации ядовитых соединений к III классу опасности. При работе с веществом концентрация его паров в воздухе не должна превышать значений, которые определены санитарно-гигиеническими нормативами. Нельзя допускать при обращении с толуолом появления открытого огня, искр, это может привести к взрыву. Также существуют экологические проблемы, связанные с выделением толуола в атмосферу:
- при сжигании нефти, разных видов топлива;
- в действующих вулканах;
- в лесных пожарах;
- при использовании растворителей и красок.
Токсические свойства толуола, пожаро- и взрывоопасность требуют острожного обращения с жидким веществом и его парами.