Скрытая и ощущаемая теплота
Внутренняя энергия системы, в которой возможны фазовые переходы или химические реакции, может изменяться и без изменения температуры. Например, энергия, передаваемая в систему, где жидкая вода находится в равновесии со льдом при нуле градусов Цельсия, расходуется на плавление льда, но температура при этом остаётся постоянной, пока весь лёд не превратится в воду. Такой способ передачи энергии традиционно называется «скрытой» или изотермической теплотой (англ. latent heat), в отличие от «явной», «ощущаемой» или неизотермической теплоты (англ. sensible heat), под которой подразумевается процесс передачи энергии в систему, в результате которого изменяется лишь температура системы, но не её состав.
Определение
Количество теплоты входит в математическую формулировку первого начала термодинамики, которую можно записать как Q=A+ΔU{\displaystyle Q=A+\Delta U}. Здесь ΔU{\displaystyle \Delta U} — изменение внутренней энергии системы, Q{\displaystyle Q} — количество теплоты, переданное системе, а A{\displaystyle A} — работа, совершённая системой. Однако определение теплоты должно указывать способ её измерения безотносительно к первому началу. Так как теплота — это энергия переданная в ходе теплообмена, для измерения количества теплоты необходимо пробное калориметрическое тело. По изменению внутренней энергии пробного тела можно будет судить о количестве теплоты, переданном от системы пробному телу. Без использования пробного тела первое начало теряет смысл содержательного закона и превращается в бесполезное для расчётов определение количества теплоты.
Пусть в системе, состоящей из двух тел X{\displaystyle X} и Y{\displaystyle Y}, тело Y{\displaystyle Y} (пробное) заключено в жёсткую адиабатическую оболочку. Тогда оно не способно совершать макроскопическую работу, но может обмениваться энергией (то есть теплотой) с телом X{\displaystyle X}. Предположим, что тело X{\displaystyle X} также почти полностью заключено в адиабатическую, но не жёсткую оболочку, так что оно может совершать механическую работу, но обмениваться теплотой может лишь с Y{\displaystyle Y}. Количеством теплоты, переданным телу X{\displaystyle X} в некотором процессе, называется величина QX=−ΔUY{\displaystyle Q_{X}=-\Delta U_{Y}}, где ΔUY{\displaystyle \Delta U_{Y}} — изменение внутренней энергии тела Y{\displaystyle Y}. Согласно закону сохранения энергии, полная работа, выполненная системой, равна убыли полной внутренней энергии системы двух тел: A=−ΔUx−ΔUy{\displaystyle A=-\Delta U_{x}-\Delta U_{y}}, где A{\displaystyle A} — макроскопическая работа, совершенная телом X{\displaystyle X}, что позволяет записать это соотношение в форме первого начала термодинамики:Q=A+ΔUx{\displaystyle Q=A+\Delta U_{x}}.
| Виды энергии: | ||
|---|---|---|
| Механическая | Потенциальная Кинетическая | |
| ‹› | Внутренняя | |
| Электромагнитная | Электрическая Магнитная | |
| Химическая | ||
| Ядерная | ||
| G{\displaystyle G} | Гравитационная | |
| ∅{\displaystyle \emptyset } | Вакуума | |
| Гипотетические: | ||
| Тёмная | ||
| См.также:Закон сохранения энергии |
Таким образом, вводимое в феноменологической термодинамике количество теплоты может быть измерено посредством калориметрического тела (об изменении внутренней энергии которого можно судить по показанию соответствующего макроскопического прибора). Из первого начала термодинамики следует корректность введённого определения количества теплоты, то есть независимость соответствующей величины от выбора пробного тела Y{\displaystyle Y} и способа теплообмена между телами. При таком определении количества теплоты первое начало становится содержательным законом, допускающим экспериментальную проверку, так как все три величины, входящие в выражение для первого начала, могут быть измерены независимо.
Количество теплоты
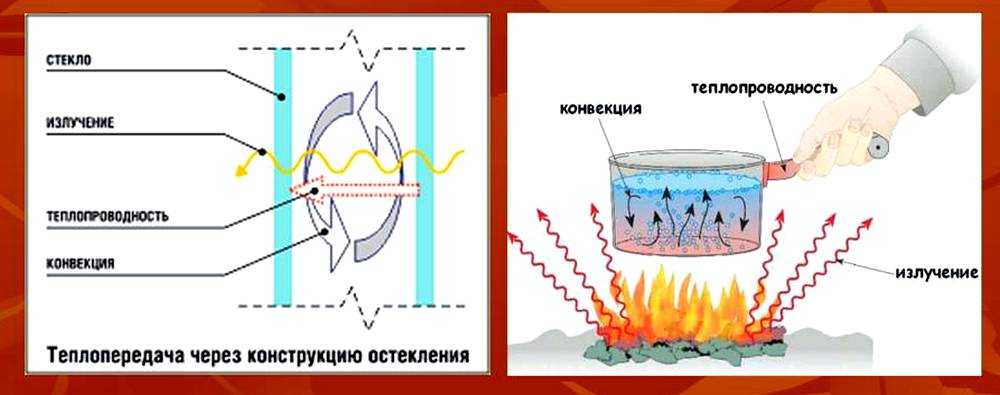
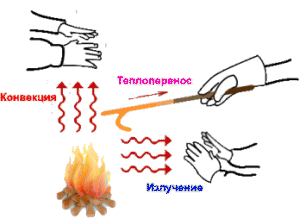
Внутреннюю энергию тела можно изменить путём совершения работы и путём теплопередачи.
ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ
В физике принято изменение любой физической величины обозначать греческой буквой Δ (читается «дельта»). Поэтому изменение внутренней энергии тела записывается следующим образом:ΔU = U2 – U1,
где U1 — начальная внутренняя энергия тела, a U2 — конечная внутренняя энергия тела (после изменения).
Изменение внутренней энергии может принимать как положительное, так и отрицательное значение.
Если внутренняя энергия тела изменилась за счёт совершённой работы, то изменение внутренней энергии равно совершённой работе А. Если же изменение произошло за счёт теплопередачи, то для характеристики этого процесса вводится понятие количество теплоты.
КОЛИЧЕСТВО ТЕПЛОТЫ
Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты. Количество теплоты принято обозначать буквой Q.
ОТ ЧЕГО ЗАВИСИТ КОЛИЧЕСТВО ТЕПЛОТЫ
Нагреем на двух одинаковых горелках два одинаковых сосуда с водой массой 100 г и 200 г соответственно. Начальная температура воды в обоих сосудах одинакова. Опыт показывает, что по прошествии некоторого промежутка времени температура воды во втором сосуде увеличится на меньшее число градусов, хотя оба сосуда получают одинаковое количество теплоты. Следовательно, количество теплоты, которое необходимо для нагревания тела до заданной температуры, зависит от массы тела.
Итак, чем больше масса тела, тем большее количество теплоты надо затратить, чтобы изменить его температуру на одно и то же значение.
При остывании тело передаёт окружающим предметам тем большее количество теплоты, чем больше его масса.
Если мы хотим подогреть воду в сосуде так, чтобы она стала тёплой (например, до температуры 40 ºС), нам потребуется меньше времени, чем для того, чтобы эту воду вскипятить (т. е. довести до температуры 100 ºС). В первом случае воде будет передано меньшее количество теплоты, чем во втором.
Таким образом, количество теплоты, которое необходимо для нагревания, зависит от разности температур тела до и после нагревания.
Теперь в одну пробирку нальём воды, а в другую — подсолнечное масло той же массы и температуры, что и вода. Обе пробирки поместим в сосуд с горячей водой. Наблюдая за показаниями термометров, мы увидим, что масло нагревается быстрее. Чтобы нагреть воду и подсолнечное масло до одной и той же температуры, воду следует нагревать дольше. Но чем дольше мы нагреваем воду, тем большее количество теплоты она получает от нагревателя (горячей воды в сосуде).
Следовательно, количество теплоты, которое необходимо для нагревания тела до определённой температуры, зависит от того, из какого вещества тело состоит.
ЕДИНИЦЫ КОЛИЧЕСТВА ТЕПЛОТЫ
Единицами количества теплоты являются те же единицы, что и для других видов энергии, — джоули (Дж) или килоджоули (кДж).
Существует и другая единица количества теплоты — калория (кал) или килокалория (ккал).
Калория (от лат. calor — тепло, жар) — это количество теплоты, которое необходимо для нагревания 1 г воды на 1 °С. Соотношение между джоулем и калорией следующее: 1 кал ~ 4,19 Дж.
Это означает, что за счёт работы, равной 4,19 кДж, температура 1 кг воды повысится на 1 ºС.
Калории обычно используют для определения энергетической ценности продуктов питания. При этом часто вместо слова «килокалория» пишут просто «Калория» с большой буквы. Количество калорий в пище определяется количеством энергии, которое получает из неё организм. Затем эта энергия будет использована для поддержания всех процессов жизнедеятельности: хорошего обмена веществ, сердцебиения, роста волос, лечения ран и т. д. Калории мы получаем из таких компонентов пищи, как белки, углеводы и жиры.
Джеймс Прескотт Джоуль (1818—1889). Английский физик, член Лондонского королевского общества.
Вы смотрели Конспект по физике для 8 класса «Количество теплоты».
Вернуться к Списку конспектов по физике (Оглавление).
Просмотров:
1 437
Тепло и температура

Зная ответ на вопрос, что такое тепло, многие могут подумать, что эта концепция аналогична понятию «температура», но это не так. Тепло — это кинетическая энергия, температура же — это мера этой энергии. Так, процесс передачи тепла зависит от массы вещества, от количества частиц, которые его составляют, а также от типа этих частиц и средней скорости их движения. В свою очередь температура зависит только от последнего из перечисленных параметров.
Отличие между теплом и температурой легко понять, если провести простой эксперимент: необходимо в два сосуда налить воду так, чтобы один сосуд был полный, а другой наполнен лишь наполовину. Поставив оба сосуда на огонь, можно наблюдать, что первым начнет кипеть тот, в котором меньше воды. Чтобы закипел второй сосуд, ему понадобиться еще некоторое количество тепла от огня. Когда оба сосуда будут кипеть, то можно измерить их температуру, она окажется одинаковой (100 oC), но при этом для полного сосуда понадобилось больше тепла, чтобы вода в нем закипела.