Особенности гальванизации с различными металлами дома
Ниже приведены нюансы, которые следует учитывать при воспроизведении отдельных технологий.
Никелирование металлических изделий
Для этого процесса применяют повышение температуры (от +24°C до +26°C) и гальванического тока до 1,2 А на дм кв., по сравнению с представленным выше серебрением. Тщательно контролируют водородный показатель. Рекомендованный диапазон pH – от 3 до 6. Прочный слой успеет образоваться за 30-40 мин.
Покрытие медью без погружения
Изделие из стали закрепляют в держателе, подключают к источнику постоянного тока (минус). Кисточку, сделанную из многожильного медного провода, обмакивают в электролит. Этот инструмент подключают к плюсу. Им водят по обрабатываемой части поверхности.
Электрохимическое цинкование
Электролит создают из следующих ингредиентов:
- дистиллированная вода – 2 литра;
- сернокислый аммоний – 100 г.;
- сернокислый цинк – 400 г.;
- натрий уксусный – 30 г.
Обработка длительностью 30-40 минут создаст прочный слой, хорошо защищающий детали от коррозии. Этот способ дешевле, чем применение аналогичных деталей из нержавеющей стали.
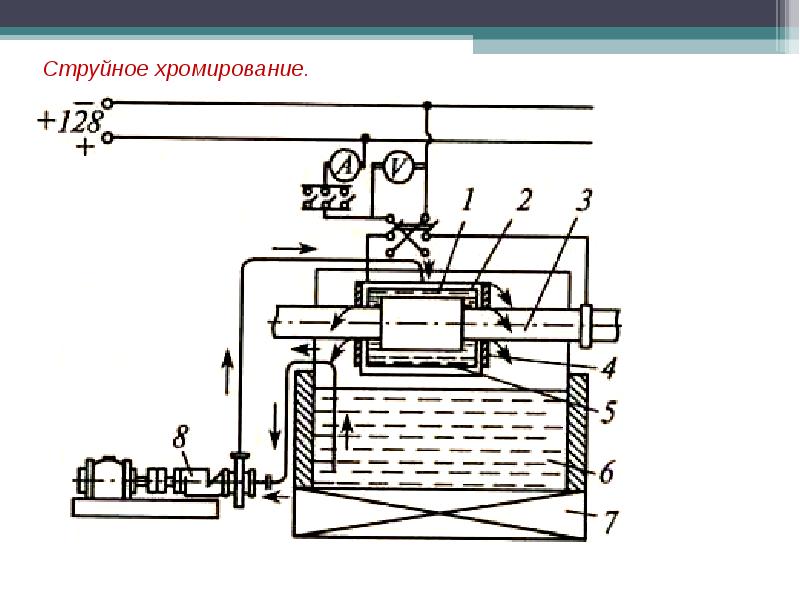
Хромирование изделий из металла
Для надежности этот слой закрепляют на технологической подложке из никеля. Такое решение не образует гальваническую пару. Повышением температуры увеличивают блеск декоративного покрытия. Прочные покрытия получают при плотности тока более 90 А на дм кв., что сложно обеспечить в домашних условиях.
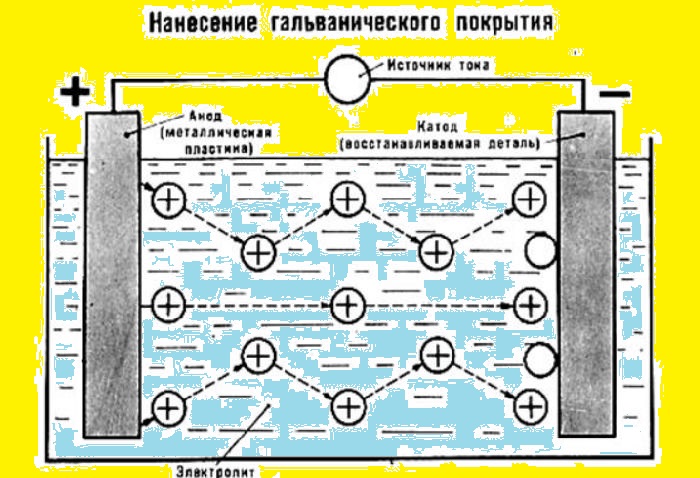
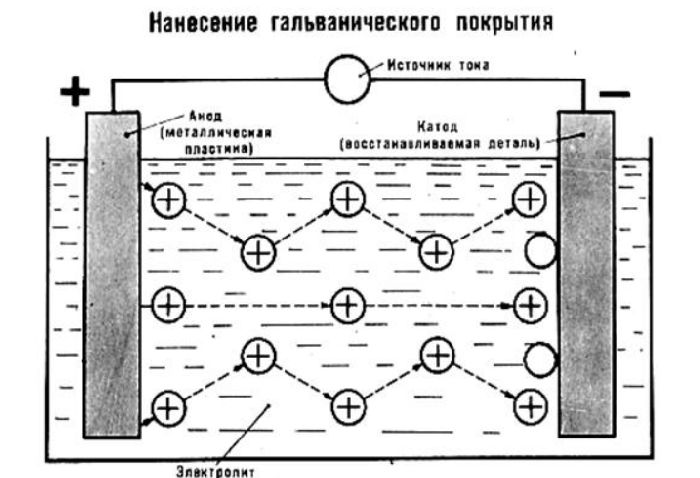
Схема реализации гальванического покрытия
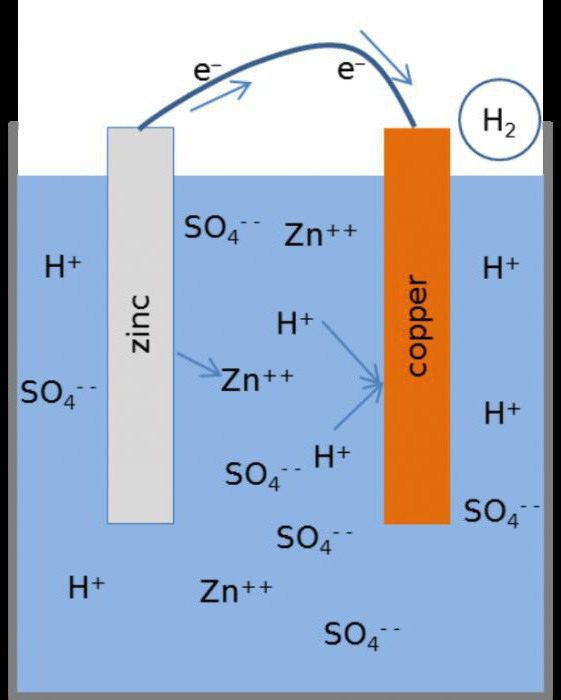
Процессы гальванизации впервые начал изучать русский физик Борис Якоби в 1836 году. Помещая различные металлы через электролитические солевые растворы, он наблюдал, как они распадались на ионы с отрицательными и положительными зарядами. Первые оседали на аноде, а вторые – на катоде (его роль в гальванике играют металлы, которые нуждаются в защите).
Перед нанесением гальванического покрытия поверхности должны быть правильно подготовлены.
Для очищения и обезжиривания металлов существуют специальные средства, которые не вызывают их коррозии. Составы на основе органических растворителей, к примеру, Очиститель метала MODENGY, обеспечивают удаление загрязнений любой химической природы – нефтепродуктов, силиконов, консервационных средств, адсорбированных пленок газов и др. Такие средства не вредят экологии, испаряются быстро и без остатка.
Гальваническое покрытие выделяет все недостатки поверхности, поэтому на ней не должно быть сколов, царапин, раковин. В связи с этим подготовка деталей к гальванизации в большинстве случаев не ограничивается их очисткой и обезжириванием, а включает также механические методы обработки (например, пескоструйный способ, шлифовку наждачной бумаги или с помощью специальных паст).
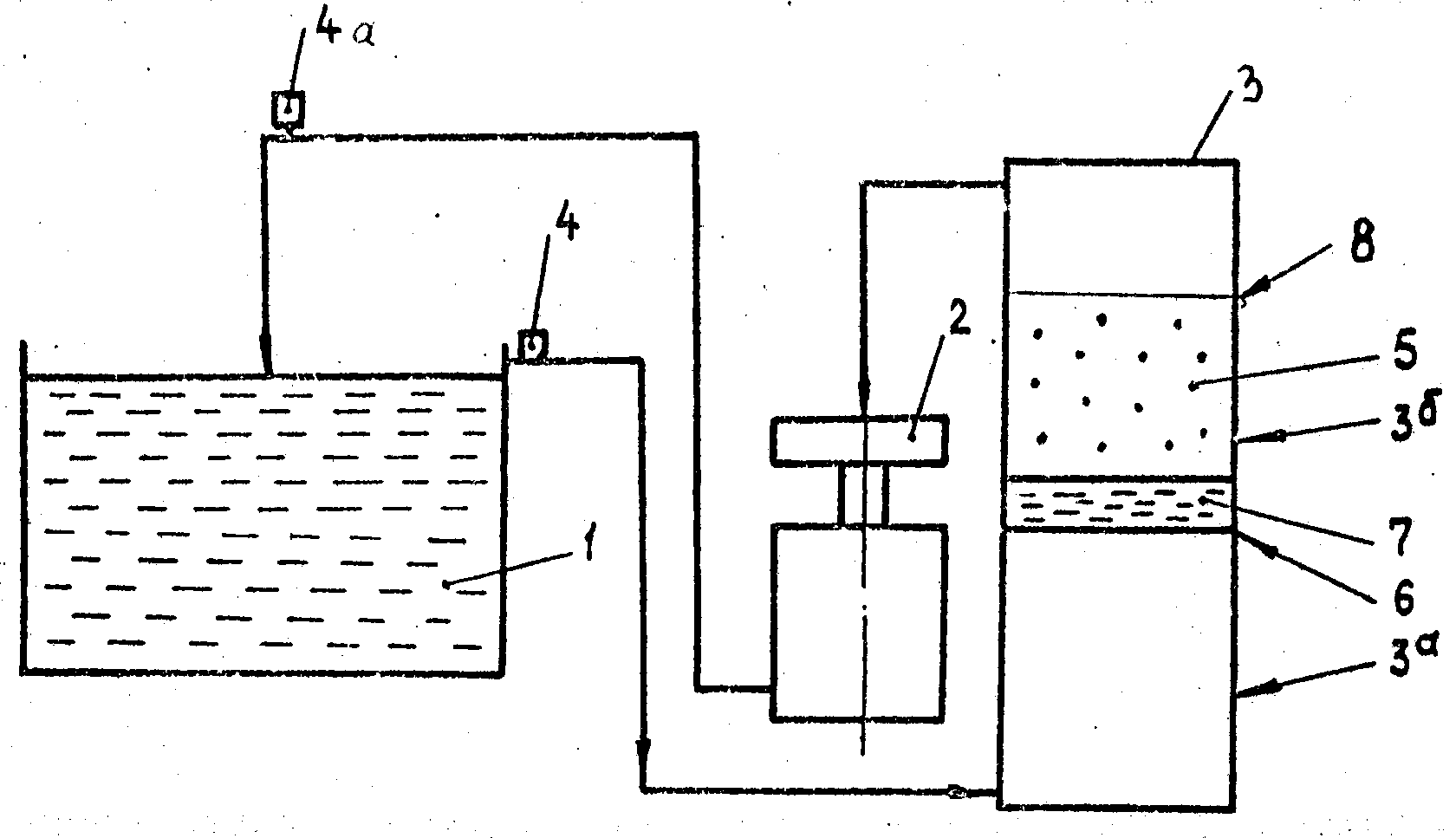
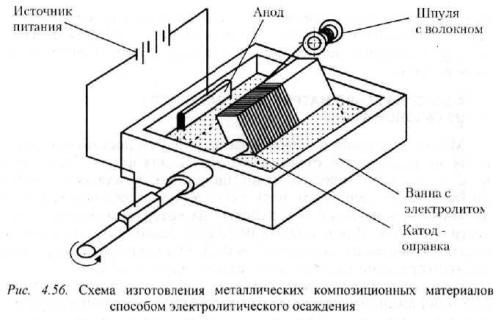
Схема реализации гальванического покрытия металла достаточно проста.
В емкость с раствором электролита помещается очищенная деталь, нуждающаяся в защите. На нее подается отрицательный заряд – таким образом деталь берет на себя роль катода. Металл, который в дальнейшем будет служить покрытием, заряжается положительно и принимает на себя функции анода. Электрическая сеть замыкается, металл анода переносится в среде электролита к отрицательно заряженному изделию (катоду) и создает на нем тонкую защитную пленку.
Это – анодный способ гальванизации. Гальваническая изоляция, полученная таким образом, первой воспринимает разрушительное воздействие коррозии, оставляя металл нетронутым.
В зависимости от вида покрываемых изделий (их размера, конструкции и пр.), а также производственных задач гальванизация проводится разными способами.
Детали больших размеров обрабатываются навесу в объемных ваннах. Более мелкие элементы получают гальваническое покрытие в емкостях барабанного типа – отрицательный заряд в них подается на барабан, вращающийся в электролите. Для обработки очень мелких деталей (например, крепежа) используются колокольные ванны: они медленно вращаются, способствуя равномерному покрытию изделий защитным металлом.
От плотности тока, проходящего через электролит, во многом зависит структура формируемого осадка. Эта величина измеряется как отношение силы тока к единице поверхности обрабатываемой детали.
Необходимо помнить, что при слишком высокой плотности тока образуется большое количество порошковых отложений, негативно влияющих на качество покрытия. Именно поэтому процесс гальванизации требует постоянного контроля.
Слой готового гальванического покрытия может иметь толщину от 6 до 20 мкр – она определяется особенностями участвующих в гальванизации материалов. Уровень адгезии металлического сплава с поверхностями определяется с помощью специальных тестов.
Используемые материалы и оборудование
Для всех видов гальванизации металла применяется однотипное гальваническое оборудование. Емкость, куда погружаются изделия из металла, называется ванной. Различие наблюдается только в разновидности электролита.
Исключение составляет холодное цинкование, совершаемое «Гальвонолом». Это жидкая суспензия, которая непосредственно наносится на металл. Отличается неустойчивостью к некоторым растворителям, поэтому нуждается в финишном покрытии.
Различается несколько групп гальванических ванн:
- Крупные. Рассчитаны на крупногабаритные изделия.
- Средние. В них нет возможности поместить большое изделие. При этом они остаются наиболее востребованными в условиях средних масштабов производства.
- Мелкие. В них можно проводить гальванизацию только мелких деталей.
В ванну помещаются анодные пластины. Изготавливаются из разных материалов. Их основная задача заключается в восполнении убывающего металла с изделия в процессе гальванизации.
Важными составляющими являются разновидность электролита и плотность тока. Эти параметры меняются в зависимости от вида операции.

Составы цианидных ванн для серебрения представлены в таблице.
| Состав | Номер электролита | |||
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | |
| Цианистое серебро | 2 | 6 | 30 | 100 |
| Цианистый натрий | 70 | 70 | – | – |
| Цианистый калий | – | – | 70 | 100 |
| Углекислый натрий | 10 | 10 | – | – |
| Углекислый калий | – | – | 10 | 25 |
| Гипосульфит натрия | – | – | 0,4 | 0,5 |
| Аммиак водный, мл/л | – | – | 1-2 | 2 |
| Едкий калий | – | – | – | 15 |
Величина плотности тока оказывает влияние на структуру формируемого осадка. Измеряется как отношение силы тока к единице поверхности обрабатываемой детали.
Пример недопустимых гальванических пар:

Гальваническое действие может возникнуть, если строительную конструкцию из нержавеющей стали скреплять оцинкованными болтами. В этой нежелательной паре пострадает высоко анодный крепеж, поскольку его электроны будут перемещаться в направлении катодной нержавеющей стали. Поэтому, крепежные детали должны быть изготовлены из менее гальванически активного металла, чем материал металлоконструкции.
На скорость течения гальванокоррозии оказывает влияние площадь поверхности анода и катода. Если большой по размеру анод соединить с маленьким катодом, то анод будет ржаветь медленно, а если сделать наоборот, то быстро. Например, используйте болты из нержавеющей стали для крепления алюминия, но не наоборот.
Степень интенсивности протекания контактной коррозии зависит и от условий эксплуатации соединения. В обычных атмосферных условиях процесс будет протекать менее быстро и возрастает в агрессивной электропроводной среде, например, растворах кислот и щелочей. Присутствие в воде других веществ увеличивает проводимость электролита и скорость коррозии. Поэтому при проектировании конструкций важна оценка окружающей среды.
Особенности процесса
Для получения качественного покрытия нужно правильно подобрать силу тока и напряжение. При слишком слабом токе металл осаждается слишком долго. В случае превышения нормативных параметров по току и напряжению, металл осаждается хлопьями. Еще один момент – приобретение жидкости для электролита. Проще использовать раствор для аккумулятора машины, а специализированные химикаты, например, серную кислоту, сложно приобрести обычному человеку. Чаще всего данный способ обработки предполагает омеднение изделий. Но можно посеребрить или позолотить заготовку при наличии драгметалла.
Золочение с помощью листиков сусального золота выглядит красиво, но его себестоимость гораздо выше, чем у позолоченных изделий в розничной продаже. Чем крупнее деталь, тем большего размера требуется пластина электрода и подаваемый ток. Поэтому в быту крупные вещи не подвергают гальванопластике.
Процесс гальванопластики начинается со сборки аппарата. Плюс от источника тока подается на пластину, а минус – на изделие. Чтобы провода не начали реагировать при гальванизации, место их соединения с пластиной залепляют пластилином. Площадь с положительным зарядом должна быть больше площади заготовки желательно не менее, чем в два раза. Чтобы выставить оптимальный ток на приборе, пользуются простой формулой. Площадь пластины умножают на плотность тока. Обычно берут значение плотности 1-2 А на каждый квадратный дециметр.
После выполнения расчетов приступают к обработке. Обезжиренную заготовку с помощью клея и медной проволоки прикрепляют к минусовому контакту. Если материал не токопроводящий, необходима обработка изделия графитовым спреем. Если будущее украшение имитирует ювелирное, нужно все камушки и стекла заклеить пластилином. Этот материал не позволит измениться цвету камня. Желательно брать для создания украшений стекло или устойчивые к агрессивным средам камни.
Полученный в течение двух часов слой отличается от слоя, выработанного за сутки большей толщины и прочностью
Важно учитывать, что ванна с электролитом и изделиями должна стоять неподвижно на протяжении многих часов для качественного результата. Готовое изделие не кажется железом, оно будет сверкать розоватым медным блеском
Такой результат свидетельствует о том, что процесс прошел успешно.
Гальваностегия
Гальваностегия цианидными растворами производится на коммерческих заводах; в противном случае используются заменители, не содержащие цианидов или цианидсодержа-щих материалов.
Гальваностегия не ограничивается покрытиями одного металла другим. В последние годы все большее значение приобретает электрохимическое получение сплавов металлов. Мы привыкли к тому, что сплавы всегда получали при высокой температуре, расплавляя два или более металла.
Гальваностегия — нанесение тонких покрытий ( от допей мк до десятков ивнек-рых случаях сотен мк), прочно сцепленных с покрываемыми изделиями и составляющих с ними как бы одно целое, с целью: защиты металлич. Различают анодные и катодные покрытия.
Гальваностегия, основанная на кристаллизации металла из солевого раствора при прохождении через раствор постоянного тока, позволяет создавать любые тончайшие защитные слои из металлов, которые не подвергаются окислению.
Гальваностегия применяется в основном для защиты металлов от коррозии.
Гальваностегия — покрытие пленкой окиси металла, как правило, не имеет значения для повышения стойкости металла к сельскохозяйственным химикатам, так как анодная пленка окиси алюминия растворяется в кислых или щелочных жидкостях. Она имеет некоторое значение при повышении прочности металла по отношению к нейтральным растворам солей тяжелых металлов. Для защиты широко используется окрашивание металлических частей самолета и оборудования с использованием в качестве ингибирующего грунта дихромата натрия.
|
Конструктивная прочность емкостей высокого давления. |
Гальваностегия представляет собой раздел химии, издавна тесно связанный с одной из важнейших отраслей народного хозяйства — с машиностроением. По мере изменения условий эксплуатации различных машин и повышения требований к ним менялись и требования к гальваническим покрытиям, увеличивалась их роль в обеспечении надежной работы деталей и узлов, расширялись области их назначения и применения.
Гальваностегия осуществляется в ваннах из материала, химически стойкого в отношении применяемого электролита. Крупные ванны выполняют стальными, сварными, причем для кислых растворов их изолируют внутри резиной, эбонитом, винипластом1 или по-крзшают кислотоупорными и термостойкими лаками. Обрабатываемые изделия устанавливаются обычно на подвесках в ванне. Для процессов, протекающих при малой плотности тока ( 0 01 — 0 1 А / см2), применяют стационарные ванны с неподвижными катодами. При больших плотностях тока ( например, при хромировании) применяют ванны непрерывного действия, в которых изделия в процессе покрытия перемещаются от одного края ванны к другому. Такие ванны обычно снабжены устройствами для перемешивания электролита Сжатым1 воздухом и его фильтрации. В таких автоматах изделия, перемещаясь шагами по горизонтали и вертикали, поочередно проходят все ванны.
Гальваностегия — электролитический способ покрытия металлических изделий слоем благородного металла ( золота, платины) или другого металла, не поддающегося окислению. Например, при никелировании предмета он сам служит катодом, кусок никеля — анодом. Пропуская через электролитическую ванну в течение некоторого времени электрический ток, покрывают предмет слоем никеля нужной толщины.
Гальваностегия располагает средствами, позволяющими получить осадки необходимой структуры всех технически важных металлов.
Гальваностегия располагает средствами, позволяющими получить осадки необходимой структуры всех технически важных металлов.
Гальваностегия, которая осуществляется после химической подготовки поверхности, мало чем отличается от обычной гальваностегии — нанесения металлопокрытий на металлические детали.
Гальваностегия имеет несравненно большее значение в промышленности, хотя гальванопластика была разработана раньше.
Гальваностегия и электрооксидирование относятся к покрытиям металлов и здесь не рассматриваются.
Описание процесса
Гальванопластика — электрохимический процесс, который позволяет делать копии изделий разной формы и размеров. Преимущество технологии — высокая точность обработки.
Гальваностегия — электрохимическая технология, которая подразумевает покрытие металлических заготовок слоем металла. Покрытие выбирается зависимо от необходимых технических характеристик, которые должны быть выше чем у основы. Чаще для покрытия металлических изделий используют хром, серебро, никель.
Технологии можно назвать одинаковыми, но они различаются способами подготовки рабочих поверхностей. Перед гальваностегией проводиться обработка, нацеленная на создание прочного соединения. Покрытие после гальванопластики должно без труда отделяться от основания.
Гальваническая пара
Потенциал гальванической пары железо ( П) железо ( Ш) равен — 0 771 В, толда как пара iHg2 ртуть ( П) создает потенциал 0 910 В.
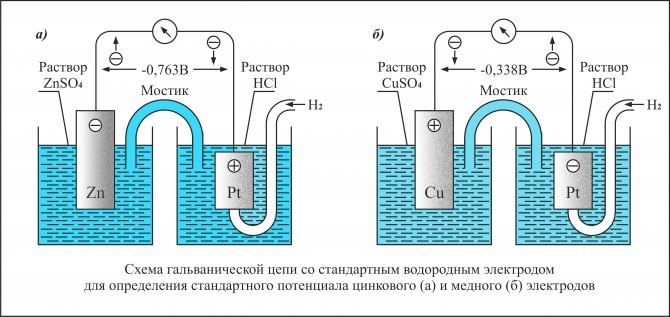
Рассмотрим гальваническую пару из цинкового и водородного электродов.
Составляя гальваническую пару по приведенной схеме с произвольной концентрацией ионов водорода в сосуде, куда опущен водородный электрод, и определяя компенсационным методом Е, получаем возможность вычислить рН раствора.
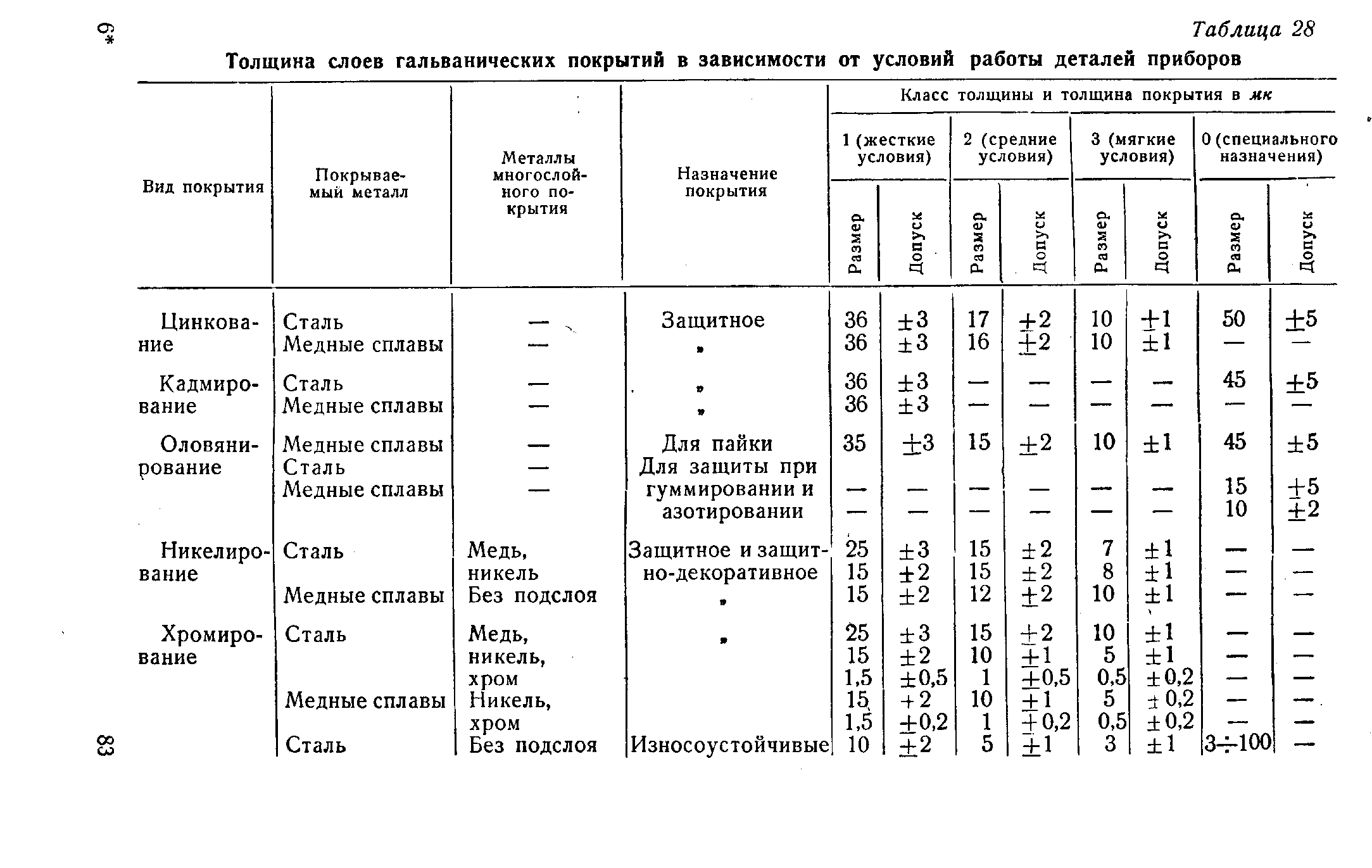
В гальванической паре никель — железо никель является катодом по отношению к железу и поэтому защищает основу ( различные углеродистые сплавы) только при условии полной беспористости покрытия. Так как гальванически осажденный никель даже в слое толщиной 25 — 30 мк обладает пористостью, то для более надежной защиты стали от коррозии он применяется обычно с подслоем меди.
В гальванической паре олово — железо слой олова является катодом по отношению к железу, и поэтому оловянное покрытие защищает сталь от коррозии только в тех случаях, когда оно сплошное и беспористое. При наличии пор олово может даже ускорить коррозию основного металла.
|
Катодная поляризация в никелевых электролитах. |
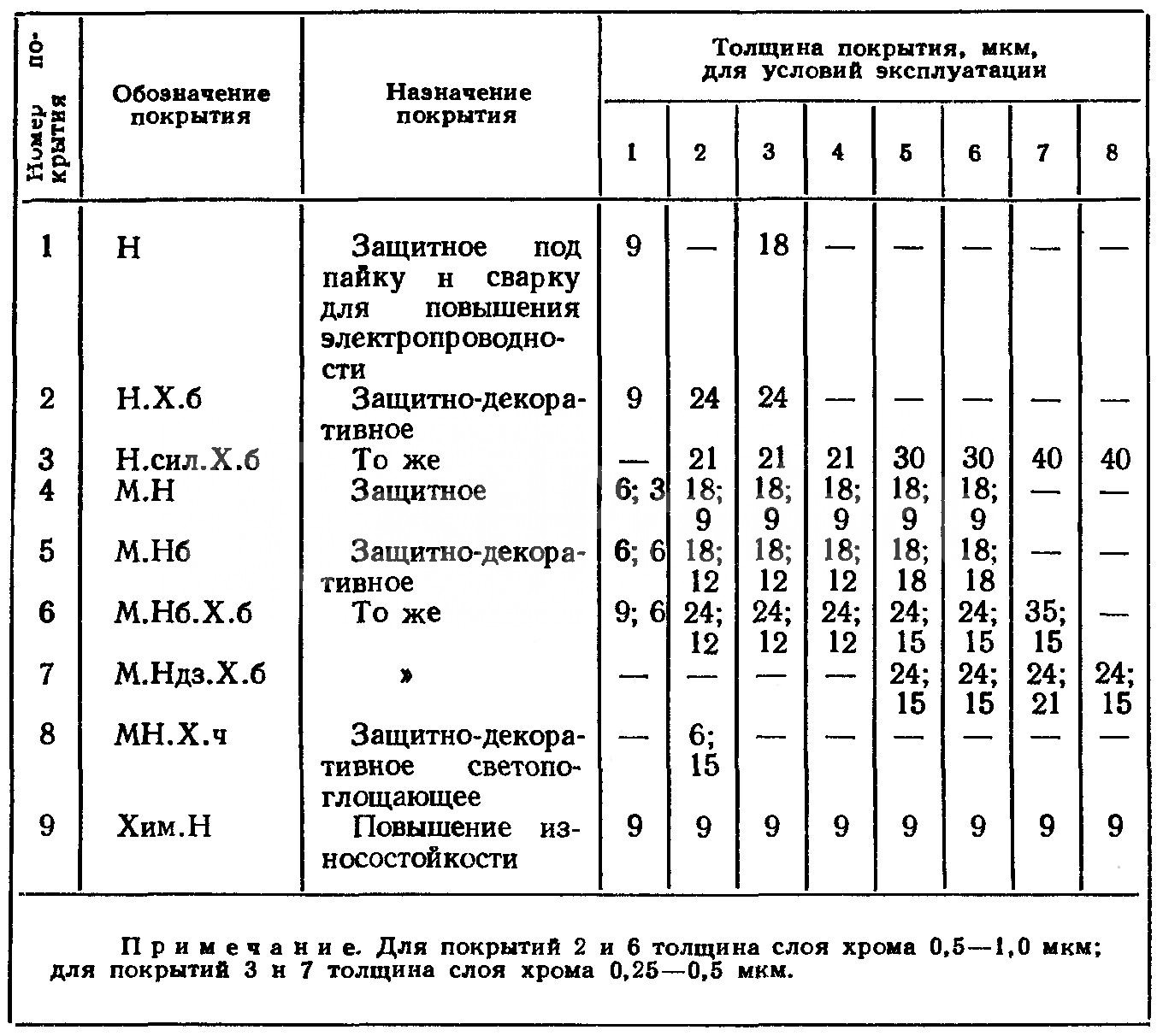
В гальванической паре никель-железо он является катодным покрытием и, следовательно, может защищать железо лишь при условии от сутствия оголенных участков и пор. Поэтому необходимо получать никелевые покрытия с минимальной пористостью. Это условие может быть соблюдено при правильном ведении процесса никелирования и определенной толщине слоя никеля. Для никелевого покрытия без подслоя на стали она колеблется в пределах 12 — 36 мк в зависимости от условий эксплуатации. Для уменьшения пористости на стали осаждают сначала слой меди, а затем уже слой никеля.
|
Катодная поляризация в никелевых электролитах. |
В гальванической паре никель — железо он является катодным покрытием и, следовательно, может защищать железо лишь при условии от сутствия оголенных участков и пор. Поэтому необходимо получать никелевые покрытия с минимальной пористостью. Это условие может быть соблюдено при правильном ведении процесса никелирования и определенной толщине слоя никеля. Для никелевого покрытия без подслоя на стали она колеблется в пределах 12 — 36 мк в зависимости от условий эксплуатации.
В гальванической паре Fe — Sn анодом будет уже железо, которое и разрушается ( рис. 107, б), а катодом — олово. Следовательно, олово защищает железо от коррозии до тех пор, пока оно обеспечивает сплошное его покрытие. Подобные же явления происходят и тогда, когда в металле, находящемся в электролите, будут находиться примеси других металлов. В этом случае на поверхности металла и в его трещинах возникает множество микрогальванических элементов, в которых примеси обычно представляют собой катоды, а кристаллики самого металла аноды. В стали находятся кристаллики железа, карбида железа Fe3C и углерода. В электролите разрушается железо.
В образовавшейся гальванической паре протектор Б является анодом, а защищаемая конструкция А — катодом.
В искусственно образованной гальванической паре один полуэлемент ( трубопровод) оказывается катодом, коррозия которого резко замедляется или прекращается совсем, а другой полуэлемент ( протектор) оказывается анодом, который корродирует более сильно, так как подвергается действию электрического тока, стекающего с него в процессе работы данного гальванического элемента.
В чугуне гальваническая пара феррит — графит обладает большой электродвижущей силой ( о 564 в), поэтому скорость растворения чугуна в электролитах очень значительна. Разрушение чугуна происходит главным образом около графитовых включений, и чем их больше, тем меньше коррозионное сопротивление чугуна. Однако чрезмерно крупный графит также нежелателен, ибо он уменьшает плотность отливки.
Например, гальваническая пара Fe-Zn в горячей водопроводной воде меняет свою полярность так: потенциал цинка облагораживается и цинк становится катодом по отношению к железу, потенциал которого с повышением температуры становится отрицательнее.
|
Электролитический ключ.| Схема переключателя тока ( вид сверху. |
Особенности процесса
При помощи гальванопластики выполняются точные копии любого предмета. Этот приём находит применение в исполнении бронзовых фигур, пластин для печати, восстановлении поверхностей повреждённых деталей.
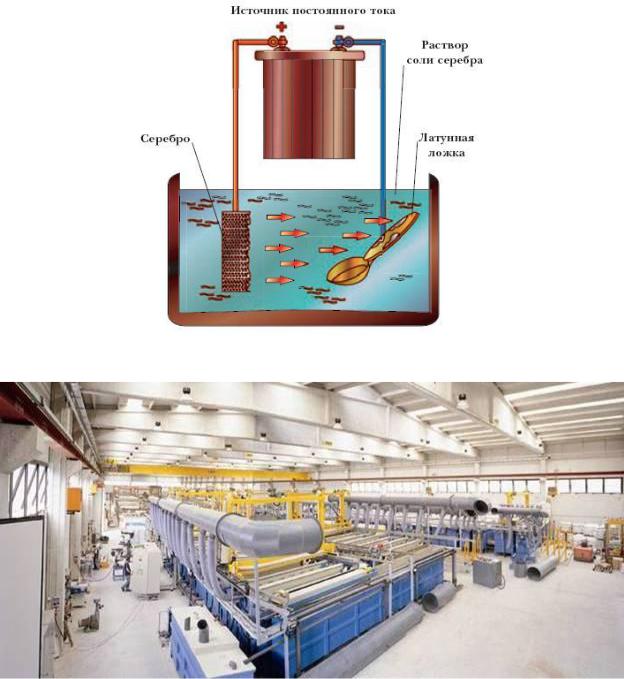
Суть процесса заключается в погружении в электролит объекта. В качестве электролита используется водный раствор соли металла, которым нужно выполнить покрытие. Когда соли растворяют в воде, в них молекулы распадаются на заряженные частицы противоположных зарядов:
- катионы металла или водорода – положительные ионы;
- анионы кислотных остатков, гидроксильных групп или кислорода – отрицательные ионы.
Как известно, электролиты проводят электрический ток. Если в них погружать металлические электроды, подключенные к источнику постоянного тока, то через электролит станет протекать ток. При этом положительные ионы начнут движение к катоду, отрицательные – двинутся к аноду.
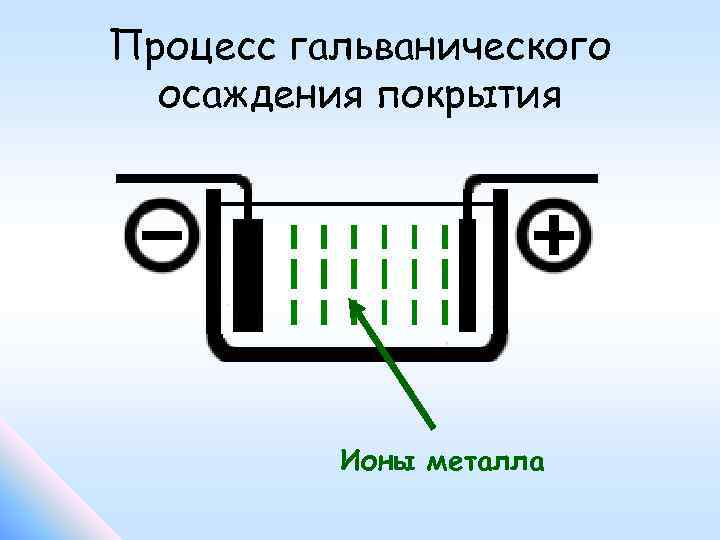
Схема гальванического процесса
Внимание! При восстановлении деталей с помощью гальванического осаждения в качестве катода может выступать сама деталь, анода – металлическая пластина. Аноды могут быть как растворимые, так и нерастворимые
Первые выполнены из осаждаемого на деталь металла, вторые – из свинца.
В результате протекания тока через раствор металл оседает на поверхности детали (катода) из-за того, что катионы металла и водорода на ней теряют заряд. Покрытие наносится на уровне молекул. Анионы, в свою очередь, разряжаются на аноде с выделением кислорода. Концентрация электролита всё время неизменна, потому что металл на аноде при разряде растворяется и пополняет раствор своими положительными ионами.
Гальваностегия, как вид гальванотехники, допускает выполнять защитные и декоративные покрытия металлических изделия либо придание их поверхности особых свойств. Её технологическая схема подразумевает нанесение на металлическую поверхность покрытия из другого металла, который более устойчив к механическим и химическим нагрузкам.
Создание формы
С изделия, которое будем копировать, снимаем отпечаток. Для этого понадобится какой-нибудь легкоплавкий металл, пластилин, гипс или воск. Если используем металл, обрабатываем копируемый предмет мылом и кладем его в картонную коробку. Далее заливаем туда легкоплавкий сплав.
Когда отливка завершена, достаем изделие и полученную форму подвергаем вначале обезжириванию, а затем меднению в электролите. Чтобы избежать металлических отложений с тех сторон, где нет оттиска, расплавляем металл в кипящей воде для получения матрицы. Форму заливаем гипсом. На выходе получаем копию.
Для создания матрицы понадобится такая композиция:
- воск — 20 частей;
- парафин — 3 части;
- графит — 1 часть.
Если форма создается из диэлектрического материала, на ее поверхность наносим электропроводное покрытие. Проводниковый слой наносим либо путем восстановления металлов, либо механическим способом, подразумевающим нанесение чешуйчатого графита при помощи кисточки.
Еще до начала механической обработки поверхности растираем графит в ступе, просеиваем его сквозь сито. Наилучшая адгезия графита наблюдается с пластилином. Гипсовые, деревянные, стеклянные и пластмассовые формы, а также папье-маше эффективнее всего обработать раствором бензина и воска. Когда поверхность еще не просохла, наносим на нее графитовую пыль, а прилипшее вещество сдуваем направленным потоком воздуха.
Гальваническое покрытие нетрудно отделить от матрицы. Если форма металлическая, создаем на поверхности оксидную или сульфидную электропроводящую пленку. К примеру, на серебре это будет хлорид, на свинце — сульфид. Пленка поможет легко отделять форму от покрытия. В случае с медью, серебром и свинцом покрываем поверхность 1% раствором сульфида натрия, чтобы возникли нерастворимые сульфиды.
Материалы для технологии
Необходимое оборудование если проводится гальванопластика дома
- Металлический объект, подлежащий покрытию (должен быть стальным).
- Блок питания (3v-6v).
- Сульфат цинка / гидроксид цинка / хлорид цинка.
- Вода.
- Стакан (вместо стеклянного или пластикового объекта).
- Цинк (может быть найден внутри батареек Zn-C).
- Песочная бумага (120).
- Гальваническая ванна, сделанная своими руками или подобная емкость.
- Тканевая бумага.
- Провода.
- Чистое рабочее место достаточное для гальваники.
- Необходим источник постоянного тока с регулировкой напряжения, домашняя розетка не подходит.

Гальваническая установка
Что нужно для приготовления электролита в домашних условиях? Для различных изделий требуются различные составы раствора. Для раствора используют воду с кислотами и другими важными включениями солей, металлов. Гальваника своими руками позволить обработать многие детали и инструменты для декора или повышения износостойкости. Температура электролита в различных операциях играет разную роль. Например, при хромировании чем температура выше, тем ярче выражается покрытие.
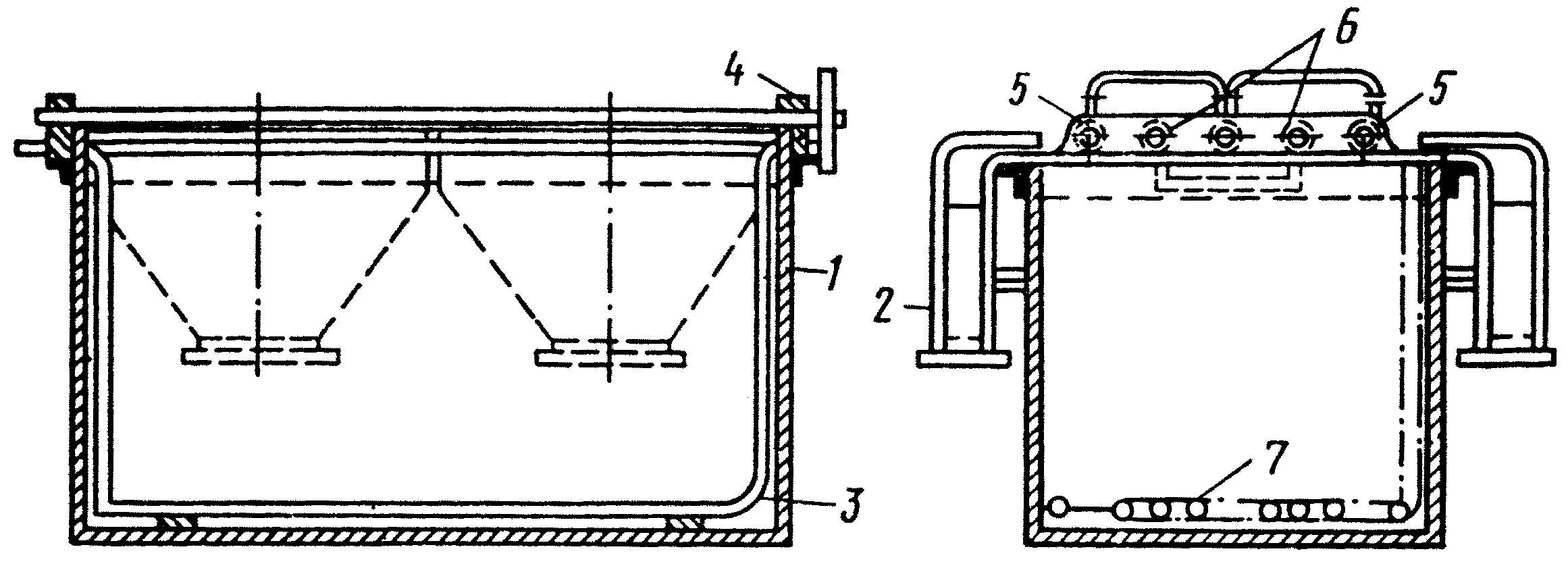
Принцип работы гальванических ванн, предназначение и виды конструкций
Гальванический процесс, работа которого построена на использовании электрического тока, дает возможность однотонного покрытия на поверхностях различных материалов. Чтобы понять принцип действия работы гальванических ванн, необходимо более детально ознакомится с конструкциями и принципом работы, это даст возможность самостоятельно изготовить устройство в домашних условиях.
Гальваника, что она собой представляет
Правильно используемая сила тока позволяет уменьшить растворенность катионов в металлах, этот принцип и есть основой гальваники. Использование гальваники позволяет видоизменять обрабатываемую поверхность, с учетом электрического окисления анионов по следующим параметрам:
- Улучшается внешний вид и эстетические качества.
- Увеличивается противостояние агрессивной среде, понижается скольжение.
- Удаление дефектных и поврежденных участков с учетом улучшения износостойкости.
- Процесс гальваники используют, как средство для увеличения толщены изделия в местах низкорослости, и при формировании плотности.
Использование гальванического травления именуют электроосаждением для очистки поверхностей, где предполагаемо, будет наноситься защитный слой. Принцип работы основан на применении в гальванической ванне производимой компанией plast-product.ru одного из вида электролита, который содержит одну, или несколько растворимых солей металла. Эта особенность дает возможность усиливать прохождение электрического тока и способствует накоплению ионов.
Толщина слоя зависит от времянахождения объекта в ванне, а скорость растворяемого анода зависит от катодной площади, обрабатываемого электротоком.
Отрасли, где применяется гальваника
Гальваника применяется в различных направлениях, но наиболее популярными является медицинская отрасль, декоративная металлургия и ювелирное дело. По популярности металлов, которые используют обработки поверхностей, выделяются:
- Родий.
- Золото.
- Палладий.
- Рутений.
- Серебро.
- Латунь.
В ювелирном деле и медицине технологию используют для хромирования деталей и инструмента, никелирования, оцинковки и обезжириваний.
Как организовать процесс гальваники самостоятельно в домашних мастерских
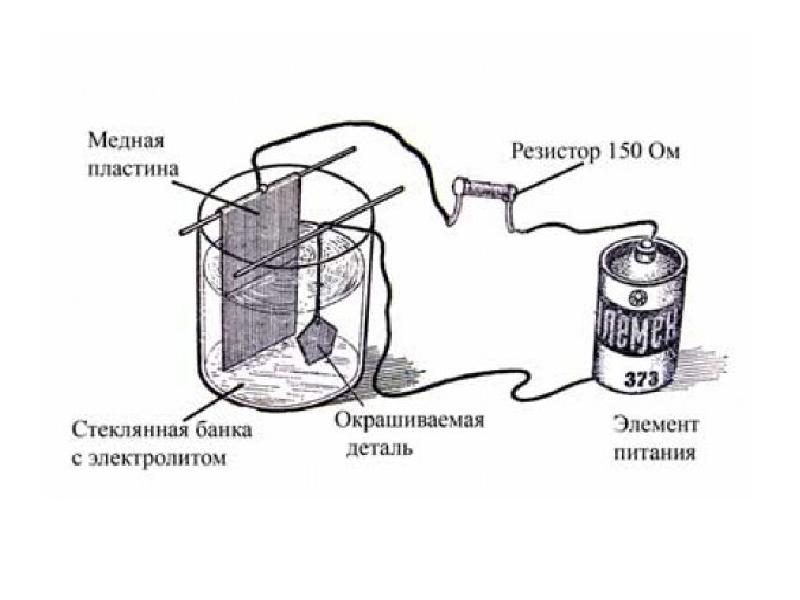
Процесс гальванизации не отличается сложностью и его вполне по силам организовать в домашних мастерских. Для этого потребуется следующее оборудование:
- Регулируемый блок питания.
- Осветитель.
- Медный купорос (вещество является ядовитым, требует корректного использования).
- Зажимы (в народе именуют «крокодилами»).
- Контейнер из стекла.
- Электроды, изготовленные из меди.
В домашних условиях сложных гальванических процессов невозможно организовать, но простейшее медное покрытие на различных покрытиях, задача выполнимая для всех желающих попробовать свои силы в подобного рода занятиях. Материал природного происхождения должен иметь слой эмали, иначе его просто испортят.
Процесс приготовления
Медный купорос растворяют в необходимом количестве воды, которая должна полностью покрывать предмет в специальном контейнере. Анод устанавливают в контейнере до полного погружения, не допуская контакта с материалом. Чем ниже напряжение, тем большее количество жидкости можно использовать.
Питание
Блок питания имеет два выхода: (+) присоединяется к аноду, таким образом, чтобы он находился над поверхностью жидкости, (-) крепится к катоду, заранее исключая прикосновение детали к меди. После чего можно подавать питание (достаточно 1 В).
Время от времени нужно проверять качество и слой покрытия, если увеличивается тусклость, нужно добавить в раствор немного отбеливателя. Сам процесс занимает несколько минут.
Полоскание
По завершению нанесения слоя деталь промывают проточной водой и вытирают насухо, следя за отсутствием на поверхности частиц медного купороса. Достаточно нескольких «тренировок», чтобы овладеть технологией обработки поверхностей на приличном уровне исполнения. Данный вид обработки поверхностей позволит вернуть привлекательность многих дорогих сердцу вещиц, которые по разным причинам потеряли нужный формат.
Рекомендуем к прочтению
Самостоятельная тонировка паркета — как это сделать правильно Как выбрать торфяной туалет для дачи Как выбрать хорошую строительную компанию: рекомендации специалистов Бани из бревна и бруса: преимущества и недостатки