Область применения
Карбид кальция (Calcium carbide) используется для получения цианамида кальция (методом реакции с азотом), из которого синтезируют цианистые соединения и удобрения, производства карбидно-карбамидных регуляторов роста растений и карбидного порошкового реагента.
Без этого вещества не обходится и проведение автогенных работ и освещения, изготовление ацетиленовой сажи и других материалов: синтетического каучука, алконитрила, стирола, винилхлорида, уксусной кислоты, хлорпроизводных ацетилена, искусственных смол, этилена, ацетона и др. Также оно применяется в процессе газосварки, производстве карбидных ламп.
Из специальной фракции calcium carbide (прошедшей переработку с применением отходов и некондиционного сырья) путем реакции с водой получают газ ацетилен и побочный продукт – гашеную известь. Эта процедура сопровождается выделением значительного количества тепла. Объем получаемого газа зависит от чистоты карбида кальция (чем чище материал, тем больше выйдет ацетилена) и варьируется в пределах 235-285 л от 1 кг карбида.
Теоретически для разложения 1 кг calcium carbide требуется 0,56 л воды, но на практике используют от 5 до 26 л жидкости, чтобы лучше охладить ацетилен и обеспечить безопасность процесса. Быстрота разложения будет зависеть от грануляции и чистоты исходного материала, а также от температуры и чистоты воды (чем чище и меньше размер, больше температура, тем выше скорость реакции).
Применение
Кольцо (ювелирное украшение) из карбида вольфрама с гладкой шлифованной поверхностью.
Кольцо (ювелирное украшение) из карбида вольфрама с огранкой.
Карбид вольфрама активно применяется в технике для изготовления инструментов, требующих высокой твёрдости и коррозионной стойкости, а также для износостойкой наплавки деталей, работающих в условиях интенсивного абразивного изнашивания с умеренными ударными нагрузками. Этот материал находит применение в изготовлении различных резцов, абразивных дисков, свёрл, фрез, долот для бурения и другого режущего инструмента. Марка твёрдого сплава, известная как «победит», на 90% состоит из карбида вольфрама.
Активно применяется в газотермическом напылении и наплавке в виде порошкового материала для создания износостойких покрытий. Так, рэлит, представляющий собой эвтектику WC−W2C, используется для наплавки на буровой инструмент и на другие изделия подвергаемые абразивному износу. Один из основных материалов, использующихся для замены гальванического хромирования методом высокоскоростного газопламенного напыления.
В качестве материала бронебойных сердечников
Бронебойный подкалиберный снаряд с отделяемым поддоном к британской пушке 76,2 мм Второй мировой войны и его твердосплавный (WC) сердечник.
Особо следует выделить использование карбида вольфрама для изготовления бронебойных сердечников пуль и снарядов. Начало широкого применения твердосплавных (основа WC на кобальтовой связке, типов РЭ-6 (7,62-мм патрон с пулей БС-40), ВК6, ВК8 и аналогичных) бронебойных сердечников, для замены выполненных из закалённой стали, приходится на 1940-е годы, и было связано с настоятельной необходимостью повышения эффективности бронепробивного действия боеприпасов в существующих калибрах стрелкового и артиллерийского вооружения, вызванной быстрым наращиванием защиты практически всех видов вооружения наземной техники. Наиболее широко такие боеприпасы в калибрах стрелкового оружия и малокалиберной артиллерии применялись вооруженными силами Германии (7,92-мм патрон с пулей SmK(H)) и СССР (14,5-мм патрон с пулей БС). В частности на вооружении сухопутных войск и ВВС Германии состояли боеприпасы с твердосплавными сердечниками в калибрах 15×96 мм/MG 151, масса пули 0,052 кг; 20×138 мм/S-18/1100, 30×184 мм/MK-101, MK-103 и далее, включая калибр 50 мм H-Pzgr и более крупные калибры противотанковой артиллерии.
В послевоенное время, в 1960 – 1970-х годах в Швейцарии и ФРГ были разработаны и приняты на вооружение новые подкалиберные боеприпасы с твердосплавными сердечниками, в том числе малокалиберной артиллерии в калибрах 20×128 мм «Эрликон-Контравес» и 20×139 мм «Испано-Сюиза», выпускавшиеся по лицензии целым рядом стран. По мере накопления опыта их применения пришло также понимание недостатков металлокерамических сердечников, связанное, в первую очередь, с их склонностью к разрушению от изгибающих напряжений при взаимодействии с бронезащитой под большими углами от нормали. При увеличении угла взаимодействия с броней (от нормали) эффективность бронепробивного действия боеприпасов с металлокерамическим сердечником снижалась. Кроме того, такие боеприпасы показали заметное снижение эффективности при стрельбе по разнесённым и экранированным бронепреградам вследствие их разрушения в результате резкого снятия напряжений сжатия после пробития первой преграды (экрана). Во второй половине 1970-х годов благодаря успехам в технологии вольфрамовых сплавов, позволившим повысить их пластичность до 5 – 7%, были разработаны подкалиберные боеприпасы нового поколения, активная часть которых выполнялась уже из тяжёлого сплава на основе вольфрама (W-Ni,Co) или обеднённого урана (U-0,75% Ti), обладавших определённым запасом пластичности. Новые выстрелы БПС с отделяемыми частями, были лучше приспособлены для действия по бронецелям 1980 – 2000-х годов.
Другие применения
Применяется при производстве сверхпрочных шариков для шариковых ручек размером 1 мм. Полировка этих шариков проводится в специальной машине на протяжении нескольких дней с использованием малого количества алмазной пасты.
Применяется для изготовления браслетов для дорогих швейцарских часов. Также карбид вольфрама приобрёл большую популярность при изготовлении ювелирных изделий — колец, кулонов — в которых его износостойкость позволяет гарантировать «вечный» блеск изделий.
Карбид вольфрама используется в виде подложки для платинового катализатора.
Также используется при изготовлении торцевых уплотнений валов механизмов (например в насосах) в случаях, когда контактирующая среда имеет высокую абразивность и/или вязкость.
Открытие и начало производства
Повторение эксперимента Г. Д. Раунда
О ранних, не систематических и часто непризнанных синтезах карбида кремния сообщали Деспретз (1849), Марсден (1880) и Колсон (1882 год). Широкомасштабное производство начал Эдвард Гудрич Ачесон в 1893. Он запатентовал метод получения порошкообразного карбида кремния 28 февраля 1893. Ачесон также разработал электрическую печь, в которой карбид кремния создаётся до сих пор. Он основал компанию The Carborundum Company для производства порошкообразного вещества, которое первоначально использовалось в качестве абразива.
Исторически первым способом использования карбида кремния было использование в качестве абразива. За этим последовало применение и в электронных устройствах.
В начале XX века карбид кремния использовался в качестве детектора в первых радиоприемниках.
В 1907 году Генри Джозеф Раунд создал первый светодиод, подавая напряжение на кристаллы SiC и наблюдая за жёлтым, зелёным и оранжевым излучением на катоде. Эти эксперименты были повторены О. В. Лосевым в СССР в 1923 году.
Метод производства
Карбид производится в электропечах путем сплавления (прокаливания) смеси кокса и оксида кальция (негашеной извести) при температуре от 1900°C до 2300°C. Резкий и неприятный чесночный запах карбида и вырабатываемого ацетилена вызван содержанием в карбидной смеси примесей фосфидов и сульфатов кальция.
Процесс осуществляется в несколько этапов:
- Производится обжиг известняка.
- Из обработанной извести и кокса создается порошкообразная смесь — шихта.
- Полученная смесь прокаливается в электродуговой печи до состояния расплава.
- Образовавшиеся бруски карбида дробятся для получения нужной фракции.

Средняя плотность карбидного вещества составляет 2,2 г/см3. В зависимости от содержания примесей, цвет карбида может быть темно-коричневым или темно-серым.
Конечный продукт состоит из 75-78% CaC2, остальное составляет известь и примеси. Гранулы карбида существуют разных размеров: 2×8; 8×15; 15×25; 25×80 мм. Большие гранулы обеспечивают получение большего количества ацетилена, но увеличивают время реакции. Если гранулы 8х15 и 15х25 мм разлагаются за 5-6 минут, то для разложения гранул 25х80 мм требуется более 10 минут.
Применение карбида кальция
Как ранее было отмечено, карбид кальция встречается в самых различных областях промышленности, зачастую поставляют для проведения промышленного синтеза. Свойства карбида кальция и реакция, протекающая при его соединении с различными веществами, определяют использование вещества в нижеприведенных случаях:
- Многие синтетически компоненты, входящих в состав современных материалов, производят на основе рассматриваемого компонента.
- Применяется для получения цианамида кальция. Подобный компонент используется для получения различных химических удобрений. Именно поэтому сырье применяется для регулирования скорости роста растений.
- Цианамид кальция также получают при соединении вещества с азотом.
- В некоторых случаях проводится восстановление металлов щелочной группы.
- Можно использовать рассматриваемое соединение в процессе газовой сварки.
При рассмотрении карбида кальция и области применения стоит учитывать, что подобное вещество чаще всего применяют для получения ацетилена. Подобный синтез карбида кальция разработал немецкий ученый. Среди особенностей подобного способа применения отметим следующие моменты:
- Ацетилен из карбида получают при оказании воздействия водой на используемое сырье.
- В результате прохождения химической реакции образуется требующийся газ, гашеная известь выпадает в осадок.
- Стоит учитывать, что при смешивании компонентов выделяется большое количество тепла. Поэтому работа должна проводится с учетом техники безопасности.
- В зависимости от вида применяемой технологии переработки сырья с 1 килограмма выходит около 290 литров газа.
- Скорость протекания процедуры зависит от чистоты применяемого сырья, температуры и количества воды.

Получение ацетилена из карбида кальция
Как показывает практика, при использовании чистого карбида на протекание химической реакции отводится около 20 литров волы на 1 килограмм сырья. Подобное количество воды требуется для того чтобы снизить температуру реакции, за счет чего обеспечиваются оптимальные условия для работы.
Получение
Карбид циркония можно получить одним из следующих способов.
Непосредственным насыщением циркония углеродом:
Процесс ведут в вакууме, а исходные компоненты берут в виде порошков;
Восстановлением оксида циркония углеродом с последующим образованием карбида:
Процесс идет через образование низших окислов циркония и последующего образования карбида циркония по реакции:
-
- ZrO+2C→ZrC+CO{\displaystyle {\mathsf {ZrO+2C\rightarrow ZrC+CO}}}
Этот метод применяется для получения технически чистого карбида циркония в промышленных масштабах. Обычно процесс проводят при температуре около 2000 °C;
Осаждением из газовой фазы:
В основе метода лежит реакция:
- ZrCl4+CH4+H2⇄ ZrC+4HCl+H2{\displaystyle {\mathsf {ZrCl_{4}+CH_{4}+H_{2}\rightleftarrows \ ZrC+4HCl+H_{2}}}}
Осаждение происходит на поверхности вольфрамовой нити, разогретой до температуры 1700—2400 °C. Проведение процесса при высокой температуре (около 2400 °C) позволяет получить монокристаллический осадок. Метан может быть заменен толуолом, бензолом или ацетиленом.
Что такое карбид?
Самодельные бомбы. Вот, что приходит на ум первым делом, когда слышим слово карбид. И нет, занимались производством этих опасных игрушек не предприятия оборонной промышленности, а, как правило, мальчишки, лет так десяти.
Лет двадцать назад это было излюбленное развлечение у подростков. Это сейчас все сидят за своими планшетами, а тогда миром правил пытливый ум ребенка, который норовил все испробовать на практике.
Для того, чтобы почувствовать себя Рембо, требовалось раздобыть один чудо-камешек. Находили их дети чаще всего на стройках. А дальше все было просто: пластиковый сосуд, камень, вода, плотно закрученный колпачок. Все это рьяно трясли, и в лучшем случае, отбрасывали куда подальше. А в худшем «снаряд» разрывало прямо в руках, тогда травм было не избежать.

Карбид кальция
Были и более безопасные пути использовать находку, к примеру, просто бросить в лужицу, тогда можно было наблюдать нечто похожее на действие современных бомбочек для ванны. Так что это за популярная «игрушка». Большинство из нас считали, что таким, как мы его знаем, карбид произвела природа. Но на самом деле это не так. И сегодня Вы в этом убедитесь.
Итак, вещество это всегда очень твердое, плюс ко всему, чтобы его расплавить, нужно приложить недюжинные усилия. На вид это темные, светлые, зеленоватые камни, либо порошок, все зависит от состава. Срок его годности недолог, как правило это полгода. Уложить емкости в общий склад не получится, у таких потенциально опасных веществ должен быть свой отсек.
Как Вы уже знаете, карбид постоянно норовит взорваться. Причем, некоторым соединениям даже особых условий не надо. Достаточно просто пересыпать порошок из тары в тару, как он может неожиданно рвануть.
Карбид кальция в сварке
Для сварочных работ карбид является чуть ли не идеальным веществом, потому что при взаимодействии с водой выделяет в окружающее пространство летучий газ ацетилен, который служит основой металлизации, напайки, кислородной сварки и множества иных процессов, относящихся к обработке металлических сплавов.
 Создается этот состав при очень высокой температуре (до 2400 градусов) посредством расплавления негашеной извести и кокса внутри электродуговой печки. Затем раскаленное жидкое вещество помещается в специальные формы (изложницы), где оно застывает и твердеет. Затем карбид раскалывают на кусочки размером не более 8 см. В итоге полученная субстанция будет состоять примерно на 78% из карбида кальция, а остальные 22% — это известковые окиси, примеси и иные вещества.
Создается этот состав при очень высокой температуре (до 2400 градусов) посредством расплавления негашеной извести и кокса внутри электродуговой печки. Затем раскаленное жидкое вещество помещается в специальные формы (изложницы), где оно застывает и твердеет. Затем карбид раскалывают на кусочки размером не более 8 см. В итоге полученная субстанция будет состоять примерно на 78% из карбида кальция, а остальные 22% — это известковые окиси, примеси и иные вещества.
Так как при воздействии воды карбид выделяет большое количество ацетиленового газа и тепловой энергии, это существенно затрудняет его хранение. Чтобы избежать порчи вещества, его нередко укладывают в герметичные стальные резервуары. При открытии этих металлических сосудов необходимо избегать открытого пламени и искр, иначе могут быть печальные последствия.
https://youtube.com/watch?v=QXp3OIBnSzk
Карбидная пыль (частички до 2 мм) непригодна для применения, потому что растворяется в воде практически моментально. Кроме того, при хранении большого количества пыли увеличивается риск, что применение состава в итоге приведет к взрыву резервуара. Специалисты отмечают, что килограмм рассматриваемого вещества способен выделить при взаимодействии с водой более 260 кубических дюймов ацетилена.
Физические свойства
Карбид вольфрама представляет собой порошок серого цвета. Имеет две кристаллографические модификации: α-WC с гексагональной решеткой (периоды решетки a = 0,2906 нм, c = 0,2839 нм), пространственная группа P6m2 и β-WC с кубической гранецентрированной решеткой (a = 0,4220 нм), пространственная группа Fm3m, которая устойчива свыше 2525 °C. При этом в интервале температур 2525−2755 °C существуют обе фазы. Фаза α-WC не имеет области гомогенности, поэтому отклонение от стехиометрического состава приводит к появлению W2C или графита. При нагреве выше 2755 °C α-WC разлагается образуя углерод и фазу β-WC. Фаза β-WC описывается формулой β-WC1-x, где (0 ≤ x ≤ 0,41) и имеет широкую область гомогенности, которая с понижением температуры уменьшается.
Обычно карбид вольфрама считается хрупким соединением, однако обнаружено, что под нагрузкой он проявляет пластические свойства, которые проявляются в виде полос скольжения.
Кристаллы карбида вольфрама имеют анизотропию твёрдости в различных кристаллографических плоскостях, так в зависимости от ориентации минимальное значение микротвёрдости составляет 13 ГПа, а максимальное 22 ГПа.
- Твёрдость по Роквеллу 92−94 HRA
- Модуль упругости 710 ГПа
- Стандартная энтропия 8,5±1,5 кал/(моль• °C)
- Энтропия образования из элементов −0,31 кал/(моль• °C)
- Коэффициент линейного теплового расширения 3,84−3,9•10−6 1/K
- Характеристическая температура (температура Дебая) 493 K
- Удельное электрическое сопротивление 19,2±0,3 мкОм•см при 20 °C
- Удельная электропроводность 52200 Ом−1•см−1
- Термический коэффициент электросопротивления +0,495•10−3 1/K при 20−1500 °C
- Коэффициент термо- э.д.с. −23,3 мкВ/град
- Работа выхода 3,6 эВ
- Постоянная Ричардсона 2,7 А/(см2•град2)
- Постоянная Холла −21,8±0,3 см3/K•104
- Коэффициент электронной теплоемкости 0,79 мДж/(моль•град2)
Состав и виды карбидов
Карбиды не являются отдельным веществом. Это соединение углерода с металлами и неметаллами. Причем, следует учитывать, что углерод должен обладать большей электроотрицательностью в получаемом веществе по сравнению с другими используемыми элементами. Это дает возможность избежать производства галогенов, оксидов и других углеродных соединений.
На сегодняшний день различают три вида карбида, состав которых отличен друг от друга:
- Ковалентные соединения. К данному виду относят два элемента — кремний и бром. Это соединения с прочной межатомной связью, что обеспечивает высокую температуру плавления и химическую инертность. Окисление веществ данной группы возможно только при их нагреве свыше 1000 градусов Цельсия. Твердость вещества с бромом настолько высока, что способна конкурировать даже с алмазами. Вещество с кремнием менее прочное, но 8 баллов по шкале Мооса имеет. При этом растворить данное вещество возможно только в царской водке или с помощью концентрированной азотной или плавиковой кислоты.
- Ионные соединения или солеобразные. Вещества данной группы образуются с помощью металлов 1 и 2 группы таблицы Менделеева, а также алюминием. Данные соединения характеризуются высокой температурой плавления. Карбиды ионного вида распадаются под воздействием воды и кислот. При протекании реакции выделяется углеводород и остается гидроксид металла.
- Ионно-ковалентно-металлические или металлоподобные соединения. Образуются с помощью металлов с 4 по 8 группу, а также кобальтом, никелем и железом. Отличительная особенность металлоподобных веществ — это высокая прочность и температура плавления. Данный вид соединений делится на два типа:
- Ацетилениды — при гидролизе образуют этин или ацетилен. Карбид кальция относится к данному типу соединений.
- Метаниды — при вступлении в реакцию с водой или разбавленными кислотами образуют метан. Чаще бесцветны. Сюда относят карбид алюминия, магния, бериллия.
Химическая классификация карбидов
Карбиды обычно можно классифицировать по типу химических связей следующим образом: (i) солеподобные (ионные), (ii) ковалентные соединения , (iii) межузельные соединения и (iv) «промежуточные» карбиды переходных металлов . Примеры включают карбид кальция (CaC 2 ), карбид кремния (SiC), карбид вольфрама (WC; часто называют просто карбидом, когда речь идет о станках) и цементит (Fe 3 C), каждый из которых используется в ключевых промышленных приложениях. Ионные карбиды не имеют систематического названия.
Солевидные / солевые / ионные карбиды
Солевидные карбиды состоят из высоко электроположительных элементов, таких как щелочные металлы , щелочноземельные металлы и металлы 3-й группы, включая скандий , иттрий и лантан . Алюминий из группы 13 образует карбиды , а галлий , индий и таллий — нет. Эти материалы имеют изолированные углеродные центры, часто описываемые как «C 4– » в метанидах или метидах; двухатомные единицы, » C»2- 2«в ацетилидах и трехатомных единицах» C4- 3«в аллидах. Соединение с интеркалированным графитом KC 8 , полученное из паров калия и графита, и производные C 60 щелочных металлов обычно не классифицируются как карбиды.
Метаниды
Метаниды — это подмножество карбидов, которые отличаются своей склонностью к разложению в воде с образованием метана . Три примера — карбид алюминия Al4C3, карбид магния Mg2C и карбид бериллия Be2C .
Карбиды переходных металлов не являются соляными карбидами, но их реакция с водой очень медленная, и ею обычно пренебрегают. Например, в зависимости от пористости поверхности 5–30 атомных слоев карбида титана гидролизуются с образованием метана в течение 5 минут в условиях окружающей среды, после чего происходит насыщение реакции.
Обратите внимание, что метанид в этом контексте — банальное историческое название. Согласно правилам систематического наименования IUPAC такое соединение, как NaCH 3 , будет называться «метанидом», хотя это соединение часто называют метилнатрием.
Ацетилиды / Этиниды
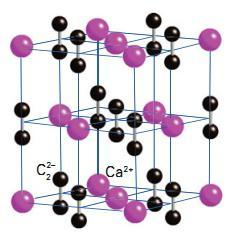
Карбид кальция .
Предполагается, что несколько карбидов являются солями ацетилид-аниона C 2 2– (также называемого перкарбидом), который имеет тройную связь между двумя атомами углерода. Щелочные металлы, щелочноземельные металлы и лантаноиды металлы образуют ацетилениды, например, карбид натрия Na 2 C 2 , карбид кальция СаС 2 и LAC 2 . Лантаноиды также образуют карбиды (сесквикарбиды, см. Ниже) с формулой M 2 C 3 . Металлы из группы 11 , также имеют тенденцию к образованию ацетиленидов, такому как медь (I) ацетилиду и серебро ацетилиду . Карбиды актинидных элементов , которые имеют стехиометрию MC 2 и M 2 C 3 , также описываются как солеподобные производные C2- 2.
Длина тройной связи CC варьируется от 119,2 пм в CaC 2 (аналогично этину) до 130,3 пм в LaC 2 и 134 пм в UC 2 . Связывание в LaC 2 было описано в терминах La III с дополнительным электроном, делокализованным на антисвязывающую орбиталь на C2- 2, объясняя металлическую проводимость.
Аллилиды
Многоатомные ионы С4- 3, иногда называемый аллилидом , содержится в Li 4 C 3 и Mg 2 C 3 . Ион является линейным и изоэлектронным с CO 2 . Расстояние CC в Mg 2 C 3 составляет 133,2 пм. Mg 2 C 3 дает метилацетилен , CH 3 CCH, и пропадиен , CH 2 CCH 2 , при гидролизе, что было первым признаком того, что он содержит C4- 3.
Ковалентные карбиды
Карбиды кремния и бора описываются как «ковалентные карбиды», хотя практически все соединения углерода проявляют некоторый ковалентный характер. Карбид кремния имеет две похожие кристаллические формы, обе связаны со структурой алмаза. Карбид бора , B 4 C, с другой стороны, имеет необычную структуру, которая включает икосаэдрические звенья бора, связанные атомами углерода. В этом отношении карбид бора похож на бориды, богатые бором . И карбид кремния (также известный как карборунд ), и карбид бора — очень твердые и тугоплавкие материалы . Оба материала важны в промышленном отношении. Бор также образует другие ковалентные карбиды, например B 25 C.
Молекулярные карбиды
Комплекс [Au 6 C (PPh 3 ) 6 ] 2+ , содержащий углеродно-золотое ядро.
Комплексы металлов, содержащие C, известны как карбидокомплексы металлов . Наиболее распространены октаэдрические кластеры с углеродным центром, такие как [Au 6 C (PPh 3 ) 6 ] 2+ и [Fe 6 C (CO) 6 ] 2– . Подобные разновидности известны для карбонилов металлов и ранних галогенидов металлов. Было выделено несколько концевых карбидов, например [CRuCl 2 {P (C 6 H 11 ) 3 } 2 ].
Металлокарбоэдрины (или «меткары») представляют собой стабильные кластеры с общей формулой M8C12 где M — переходный металл (Ti, Zr, V и т. д.).
Техника безопасности
Карбид для сварки относится к классу взрывоопасных веществ. Безопасное применение карбида обеспечивается учетом ряда условий:
- Ацетилен является легковоспламеняющимся газом, а сам сухой карбид также взрывоопасен, поэтому возле места проведения работ не должно быть источников открытого огня, даже таких незначительных, как зажигалки и зажженные сигареты.
- Запрещено использование карбида в гранулах до 2 мм или карбидной пыли, так как она растворяется очень быстро, что приводит к выделению большого количества газа. Из-за этого в генераторе образуется сверхвысокое давление и может произойти взрыв.
- Запрещена работа болгаркой или электросварочным аппаратом вблизи газосварочных работ и мест установки карбидных барабанов.
- Вещество должно храниться в сухом и герметичном месте, в котором нет водопроводов, канализационных труб и, тем более, газового оборудования.
- Карбидная пыль при попадании вызывает раздражение кожи, глаз, слизистых оболочек. Работа с этим веществом должна проходить с применением средств индивидуальной защиты – очков, перчаток и респиратора.
- При попадании карбида на кожу или в глаза его необходимо промыть большим количеством теплой воды, а затем аккуратно удалить остатки карбида пинцетом или влажным тампоном.
- При работе с карбидом в мастерской все сварочное оборудование должно быть размещено в отдельных частях помещения, система вентиляции помещения должна обеспечивать отвод горючих газов, а помещение должно быть освобождено от горючих материалов.

- Ацетиленовые генераторы запрещено устанавливать в подвальных помещениях и жилых зданиях.
- Перед запуском генератор следует осмотреть на предмет отсутствия видимых трещин и вмятин корпуса.
- Во время проведения работ генератор должен оставаться в вертикальном положении, манометр должен быть исправен и хорошо виден сварщику или его помощнику.
- По окончании работы оставшийся в генераторе раствор карбида должен быть выработан целиком, а образовавшаяся известь утилизирована.
- Повторное использование мокрых кусков карбида не допускается;
- Запрещено вскрывать генератор под давлением (во время продолжающейся реакции).
- Баллоны для ацетилена хранятся и перевозятся со специальными предохранительными колпаками на клапанах.
Если имеется необходимость в регулярном использовании оборудования для газовой сварки и резки, лучше купить профессиональное оборудование, изготовленное на промышленном предприятии. Применение самодельных генераторов чревато получением тяжелых травм и угрозой для жизни.
Получение
Карбид вольфрама можно получить одним из следующих способов.
Непосредственным насыщением вольфрама углеродом:
- В основе процесса получения карбида вольфрама лежит реакция:
- W+C=WC{\displaystyle {\mathsf {W+C=WC}}}
- Образование WC происходит с образованием на поверхности частиц вольфрама монокарбида вольфрама, из которого внутрь частицы диффундирует углерод и образует ниже лежащий слой составом W2C.
- При получении WC используют порошок вольфрама, восстановленный из его оксида, и сажу. Взятые в необходимом количестве порошки смешивают затем брикетируют или насыпают с утрамбовкой в графитовые контейнеры и помещают в печь. Для защиты порошка от окисления процесс синтеза ведут в среде водорода, который взаимодействуя с углеродом при температуре от 1300 °C образует ацетилен. Образование карбида вольфрама идет в основном через газовую фазу за счет углерода содержащегося в газах. Реакции карбидизации имеют следующий вид:
- 2C+H2=C2H2{\displaystyle {\mathsf {2C+H_{2}=C_{2}H_{2}}}}
- 2W+C2H2=2WC+H2{\displaystyle {\mathsf {2W+C_{2}H_{2}=2WC+H_{2}}}}
- При наличии в среде окиси углерода процесс идет по реакции:
- C+CO2=2CO{\displaystyle {\mathsf {C+CO_{2}=2CO}}}
- 2CO+W=WC+CO2{\displaystyle {\mathsf {2CO+W=WC+CO_{2}}}}
- Обычно процесс получения карбида вольфрама ведут при температуре 1300−1350 °C для мелкозернистых порошков вольфрама и 1600 °C для крупнозернистых, а время выдержки составляет от 1 до 2 часов. Полученные слегка спёкшиеся блоки карбида вольфрама измельчают и просеивают через сита.
Восстановлением оксида вольфрама углеродом с последующей карбидизацией:
- Этот метод в отличие от выше описанного совмещает процесс восстановления и карбидизации вольфрама, при этом в шихту добавляют недостающее количество сажи для образования карбида. Восстановление оксида вольфрама WO3 происходит через газовую фазу в среде CO и водорода.
Восстановлением соединений вольфрама с последующей карбидизацией:
- Еще одним способом получения карбида вольфрама является нагрев смеси вольфрамовой кислоты, вольфрамового ангидрида (WO3) или паравольфрамата аммония ((NH4)10•[H2W12O42]•xH2O) в среде водорода и метана при температуре 850−1000 °C.
Осаждением из газовой фазы:
- Получение карбида вольфрама из газовой фазы основано на разложении карбонила вольфрама при температуре 1000 °C.
Электролизом расплавленных солей:
- Электролиз смеси расплавленных бората натрия, карбоната натрия, фторида лития и вольфрамового ангидрида позволяет получить карбид вольфрама.
Монокристаллы карбида вольфрама:
- Монокристаллы WC могут быть получены выращиванием из расплава. Для этого смесь составом Co−40%WC плавят в тигле из оксида алюминия при температуре 1600 °C и после гомогенизации расплава температуру снижают до 1500 °C со скоростью 1−3 °C/мин. и выдерживают при этой температуре в течение 12 часов. После чего образец охлаждают и растворяют кобальтовую матрицу в кипящей соляной кислоте. Также может быть использован метод Чохральского для выращивания больших монокристаллов (до 1 см).