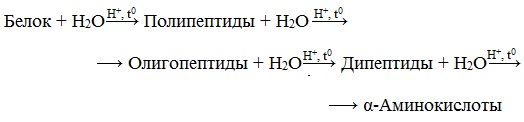Что такое денатурация белка
Так, при припускании птицы, рыбы, тушении мяса, мариновании мяса и рыбы перед жаркой добавляют кислоту, вино или другие кислые приправы для создания кислой среды со значениями рН, лежащими значительно ниже изоэлектрической точки белков продукта. В этих условиях дегидратация белков в студнях снижается и готовый продукт получается более сочным.
В кислой среде набухает коллаген мяса и рыбы, снижается его температура денатурации, ускоряется переход в глютин, в результате чего готовый продукт получается более нежным.
Температура денатурации белков повышается в присутствии других, более термостабильных белков и некоторых веществ небелковой природы, например сахарозы. Это свойство белков используют, когда при тепловой обработке возникает необходимость повысить температуру смеси (например, в целях пастеризации), не допуская денатурации белков. Тепловая денатурация некоторых белков может происходить без видимых изменений белкового раствора, что наблюдается, например, у казеина молока.
Пищевые продукты, доведенные тепловой обработкой до готовности, могут содержать большее или меньшее количество нативных, неденатурированных белков, в том числе некоторых ферментов.
Предыдущая12345678910111213141516Следующая
Дата добавления: 2015-08-14; просмотров: 1521;
Последствия
После денатурации происходит переход нативной компактной структуры в рыхлую развернутую форму, упрощается проникновение к пептидным связям ферментов, необходимых для разрушения.
Конформация белковых молекул определяется возникновением достаточного количества связей между разными участками определенной полипептидной цепочки.
Белки, состоящие из достаточного количества атомов, которые находятся в непрерывном хаотичном движении, способствует определенным перемещениям частей полипептидной цепи, что вызывает нарушение общей структуры белков, снижение его физиологических функций.
Белки имеют конформационную лабильность, то есть предрасположенность к незначительным изменениям конформации, происходящим в результате обрыва одних и образования других связей.
Денатурация белка приводит к изменениям его химических свойств, способности вступать во взаимодействие с другими веществами. Наблюдается изменение пространственной структуры и участка, непосредственно контактирующего с иной молекулой, и всей конформацией в целом. Наблюдаемые конформационные изменения имеют значение для функционирования белков в живой клетке.
Лабильность пространственной структуры белков и их денатурация. Факторы, вызывающие денатурацию.
Лабильность белка — склонность к небольшим изменениям конформации за счет разрыва одних и образовании других слабых связей. Конформация белка может меняться при изменении химических и физических свойств среды, а также при взаимодействии белка с другими молекулами. При этом происходит изменение пространственной структуры не только участка, контактирующего с другой молекулой, но и конформация в целом.
Денатурация — потеря нативной конформации белка с утратой специфической функции белка. Это происходит когда рвутся многочисленные, но слабые связи в молекуле белка под воздействие различных факторов. ОДНАКО! При денатурации не происходит разрыва пептидных связей, первичная структура БУДЕТ… ЖИТЬ…
Какие факторы способны денатурировать белок? Многочисленные. 1. Высокая температура, более 50 градусов по Цельсию. Увеличивается тепловое движение, связи рвутся. 2. Интенсивное стряхивание раствора, когда происходит контакт с воздушной средой и происходит изменение конфомации молекул. 3. Органические вещества (этиловый спирт, фенол и др.) спсобные взаимодействовать с функциональными группами аминокислот, что приводит, догадайтесь, правильно!, к изменению конформации. 3. Кислоты и щелочи, изменением рН среды приводят к перераспределению связей в белке. 4. Соли ТЯЖЁЛЫХ металлов, образуют прочные связи с функциональными группами, меняя активность и конформацию. 5. Детергенты (мыло) — содержащие гидрофобный углеводородный радикал и гидрофильную функц. группу. Гидрофобные участки белка и детергента находят друг друга в сложном мире раствора и изменяют конформацию белка, однако не оседают, так как их поддерживают на плаву гидрофильные участки детергента.
14. Шапероны – класс белков, защищающий другие белки от денатурации в условиях клетки и облегчающий формирование их нативной конформации.
Шапероны — белки, способные связываться с другими белками, находящимися в неустойчивом, склонном к агрегации состоянии. Они способны обеспечить их конформацию, обеспечивая фолдинг белков.
Классифицируются следующим образом — по молекулярной массе на 6 основных групп: 1. высокомолекулярные с мол.массой от 100 до 110 кД. 2.
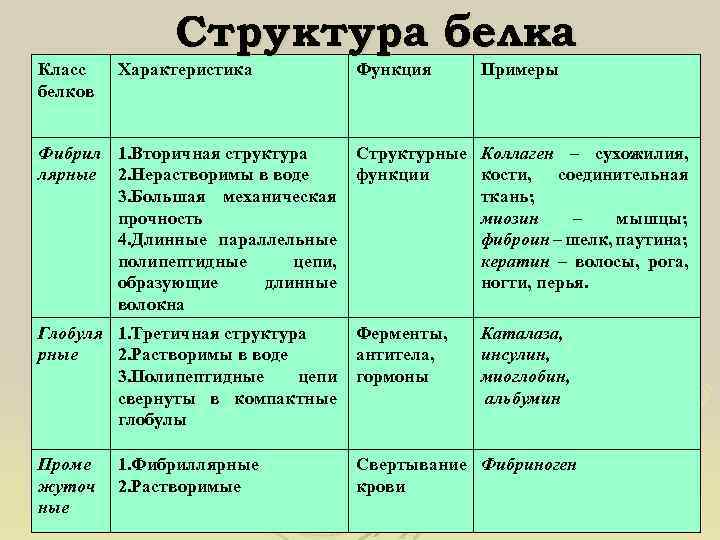
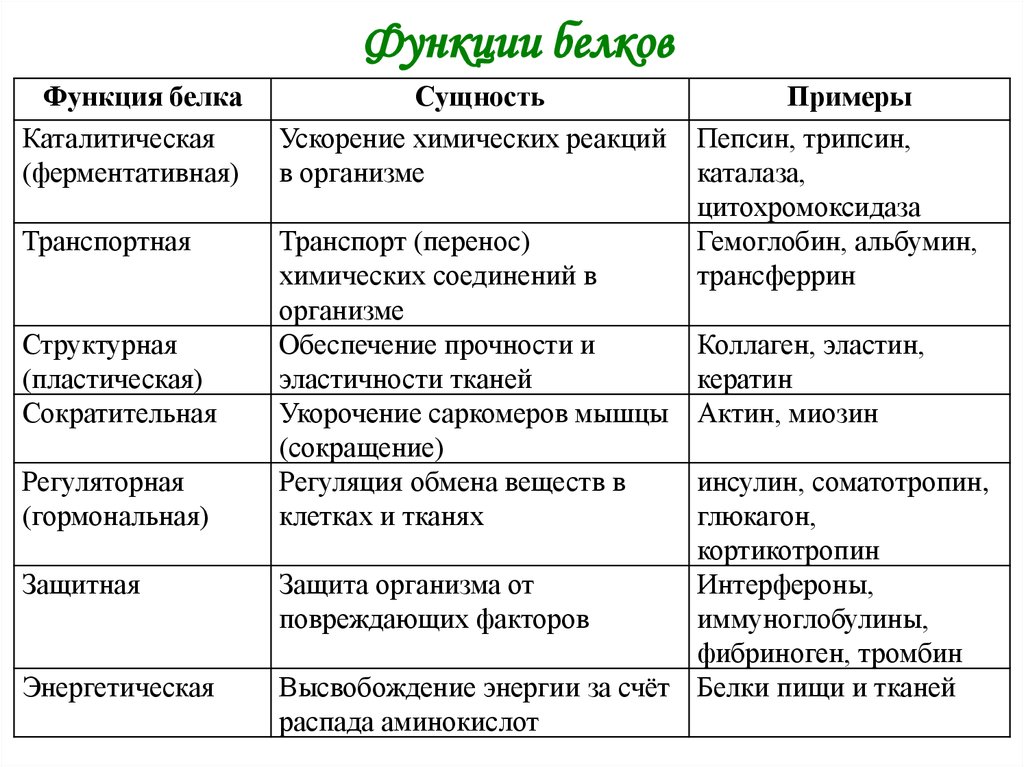
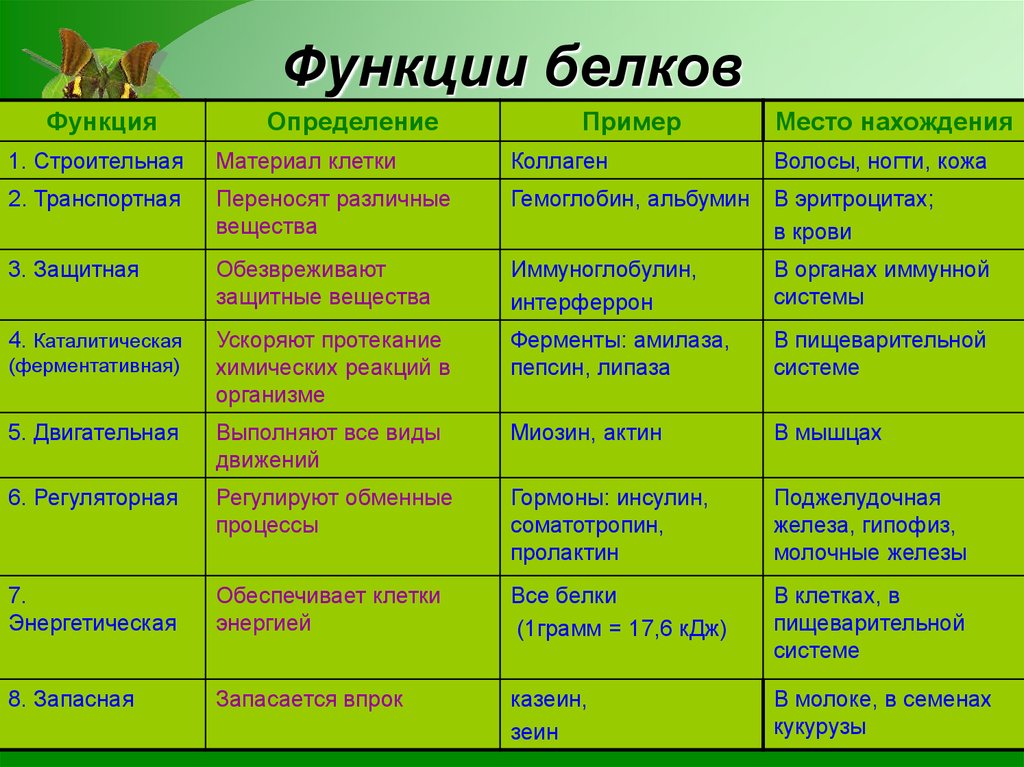
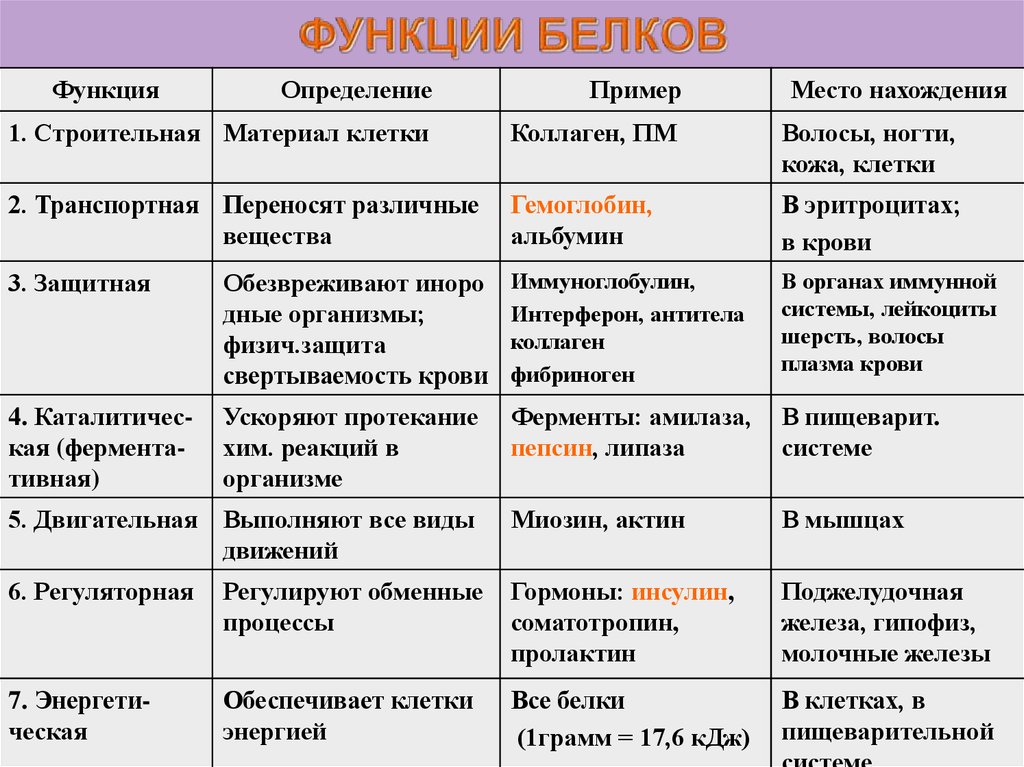
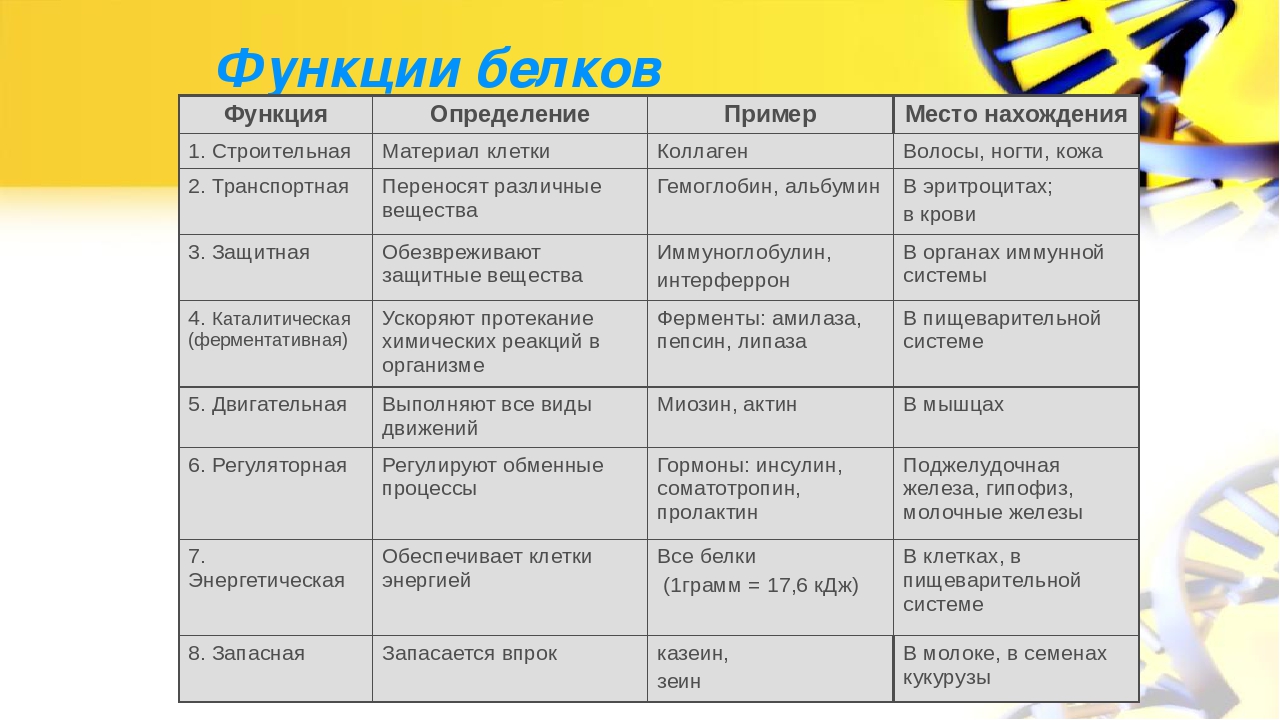
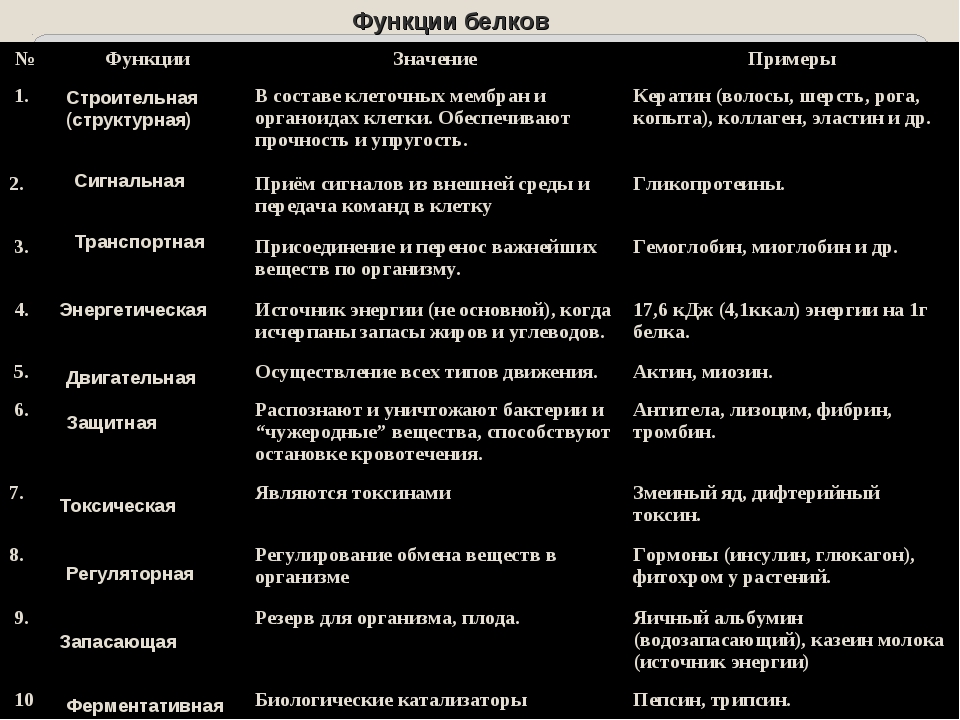
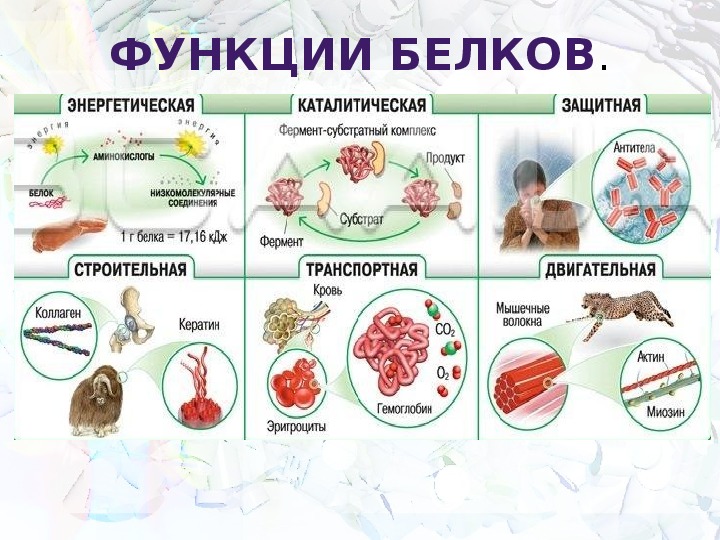
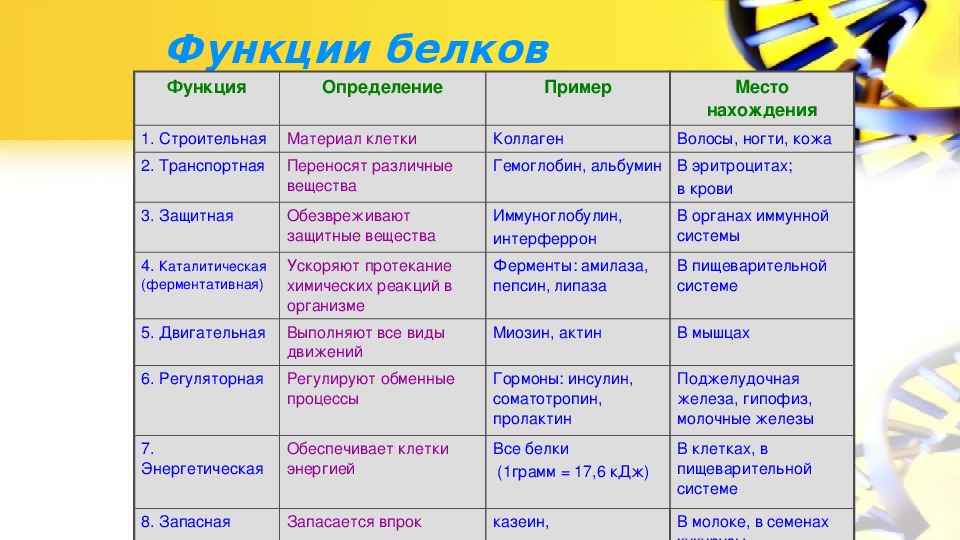
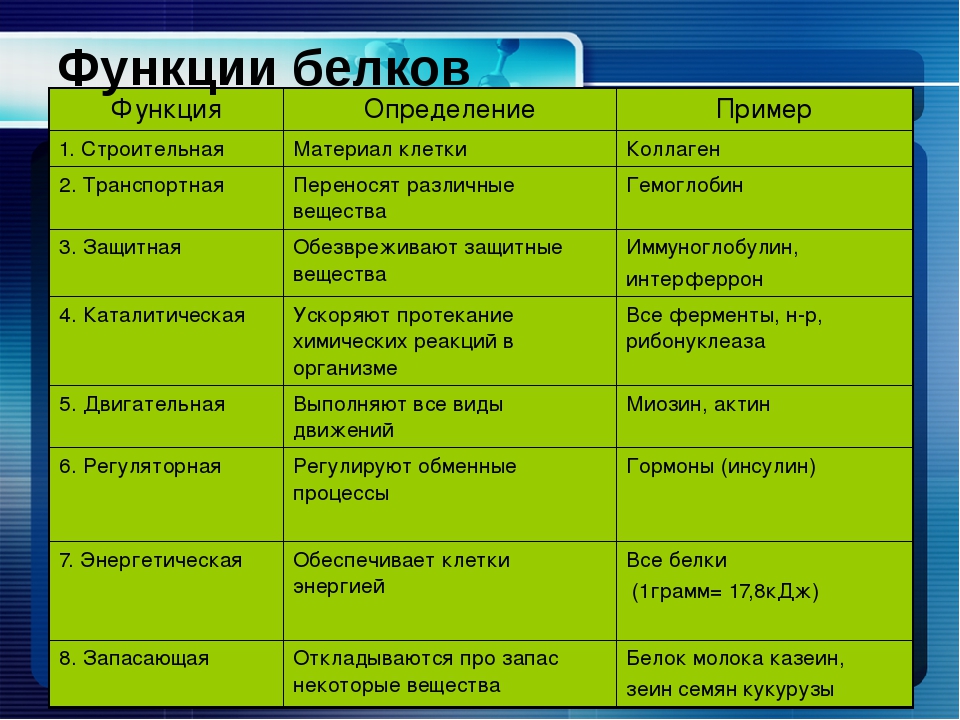
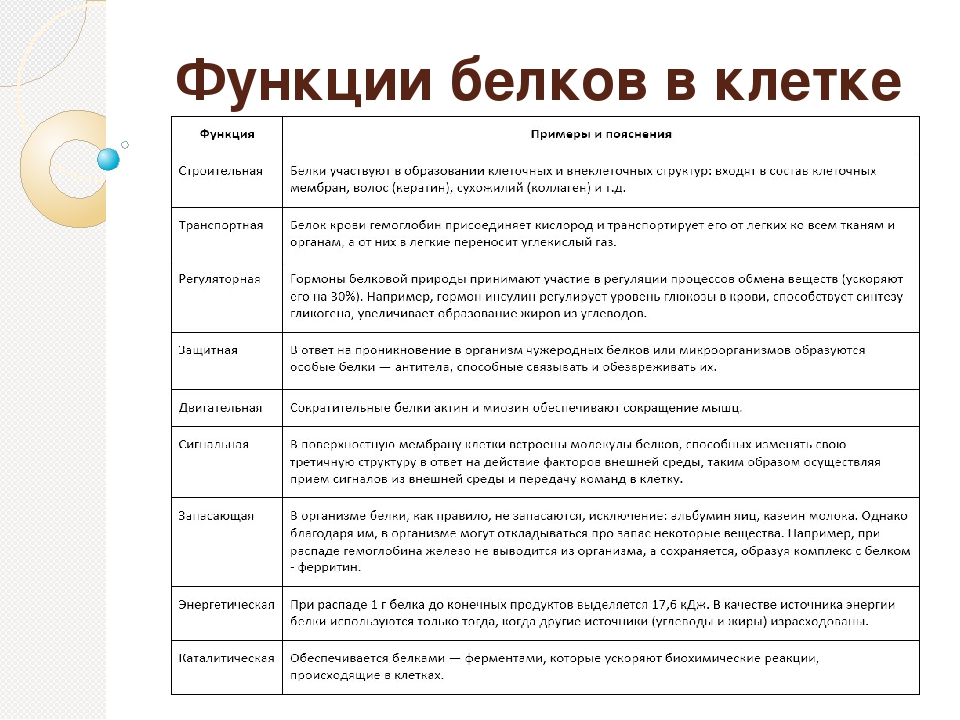
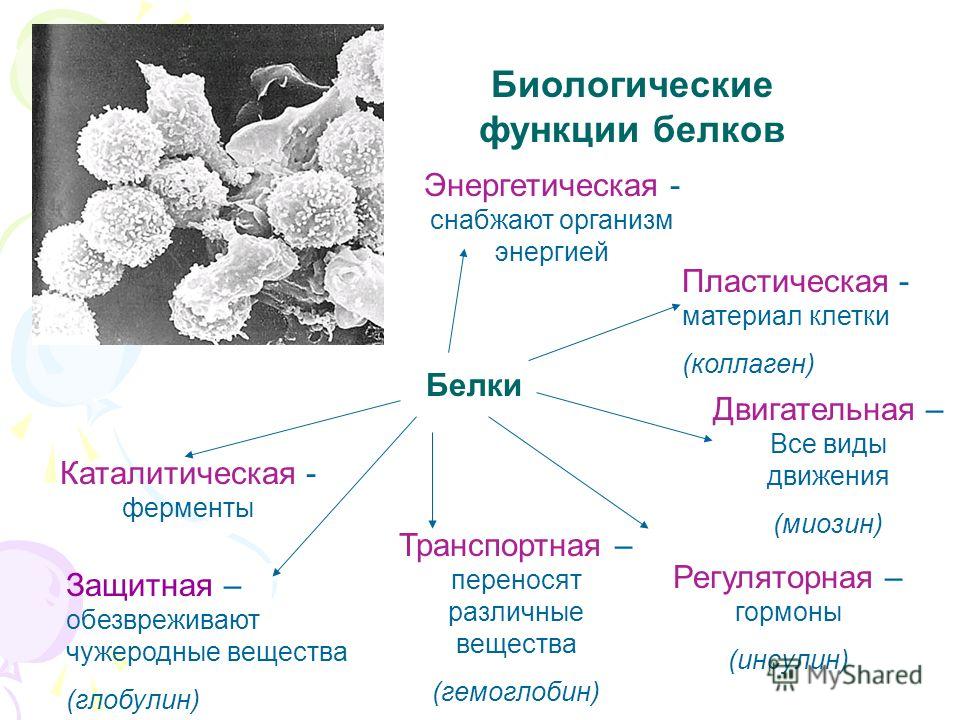
Функции белков
Белки выполняют следующие основные функции:
- Структурная (строительная). Входят в состав мембран, микротрубочек и микронитей, которые выполняют роль цитоскелета. В связях содержится белок эластин, в волосах, ногтях и перьях – белок кератин, в хрящах и сухожилиях – белок коллаген, в костях – белок осеин.
- Защитная. Лимфоцитами вырабатываются специализированные белки – антитела, которые способны распознавать и обезвреживать бактерии, вирусы, инородные для организма белки. В процессах свертывания крови принимают участие белки фибрин, тромбопластин и тромбин. Они предупреждают значительные потери крови. В ответ на атаку болезнетворных микроорганизмов растения также синтезируют ряд защитных белков.
- Сигнальная. Обеспечивает избирательное поглощение клеткой определенных веществ и способствует защите ее. При этом отдельные сложные белки клеточных мембран способны распознавать определенные химические соединения и реагировать на них. Они связываются с ними или изменяют свою структуру и передают сигналы об этих веществах на другие участки мембраны или вглубь клетки.
- Двигательная (сократительная). Обеспечивают способность клетки двигаться, изменять форму. Например, сокращающиеся белки актин и миозин функционируют в скелетных мышцах и во многих других клетках. В состав микротрубочек ресничек и жгутиков эукариотических клеток входит белок тубулин.
- Регуляторная. Являются гормонами белковой природы у животных, регулирующими рост, половое созревание, половые циклы, изменение покровов и т. п. Некоторые белки регулируют активность обмена веществ.
- Транспортная. Белки транспортируют неорганические ионы, газы (кислород, углекислый газ), специфические органические вещества. Транспортные белки содержатся в мембранах клеток, в эритроцитах и т. п. В крови есть белки-транспортеры, которые узнают и связывают определенные гормоны и несут их к определенным клеткам. Например, гемоцианин (белок синего цвета) у беспозвоночных, гемоглобин у позвоночных переносят кислород.
- Запасающая. Могут запасаться в эндосперме семени многих иидов растений (в злаковых от 15-25 %, бобовых – до 45 %), в яйцах птиц, пресмыкающих и т. п.
- Питательная. Зародыш семени некоторых растений потребляет на первых этапах развития белки, которые отложены в запас.
- Энергетическая. При расщеплении белков высвобождается энергия. Аминокислоты, которые образовались при расщеплении белков, или используются для биосинтеза белков, нужных организму, или раскладываются с высвобождением энергии. При полном расщеплении 1 г белков в среднем высвобождается 17,2 кДж энергии. Однако белки как источник энергии используются очень редко, преимущественно тогда, когда истощаются запасы углеводов и жиров.
- Ферментативная (каталитическая). Эту функцию выполняют белки – ферменты, которые ускоряют биохимические реакции в организме.
- Функция антифриза. В плазме крови некоторых живых организмов содержатся белки, которые предупреждают ее замерзание в условиях низких температур.
Некоторые организмы, живущие в горячих условиях, имеют белки, которые не денатурируют даже при температуре +50…90 °С.
Некоторые белки образуют сложные комплексы с пигментами, нуклеиновыми кислотами.
Ренатурация
Если денатурация — это процесс разрушения биополимеров, то ренатурация является обратным явлением. Восстановление нативной конформации белковой молекулы возможно в случае медленного охлаждения разрушенного при нагревании белка.
Подобное явление подтверждает строение первичной структуры белковых молекул. Образование нативной конформации является самопроизвольным процессом, предполагающим использование минимального количества энергии.
В пространственной структуре биополимера используется кодировка расположения последовательности аминокислот в полипептиде. Это усложняет процедуру ренатурации белковых молекул.

Особенности денатурированных белков
Он сопровождается разворачиванием полипептидной связи, которая в растворе изначально представлена в виде беспорядочного клубка.
Процесс денатурации белка сопровождается утрачиванием гидратной оболочки, выпадением белка в осадок, утрачиванием им нативных свойств.
Среди основных факторов, которые провоцируют процесс денатурации, выделим физические параметры: давление, температуру, механическое действие, ионизирующее и ультразвуковое излучение.
Денатурация белка происходит под воздействием органических растворителей, минеральных кислот, щелочей, солей тяжелых металлов, алкалоидов.
После того как произошла денатурация белка, он получает определенные свойства:
- В сравнении с нативной белковой молекулой увеличивается количество функциональных либо реактивных групп в молекуле.
- Уменьшается растворимость и процесс осаждения белков, чему способствует потеря водной оболочки. Происходит разворачивание структуры, появляются гидрофобные радикалы, наблюдается нейтрализация зарядов полярных фрагментов.
- Меняется конфигурация белковой молекулы.
- Утрачивается биологическая активность, причиной этого будет нарушение нативной структуры.
Денатурация – это процесс нарушения высших уровней организации белковой молекулы (вторичного, третичного, четвертичного) под действием различных факторов.
При этом полипептидная цепь разворачивается и находится в растворе в развернутом виде или в виде беспорядочного клубка.

При денатурации утрачивается гидратная оболочка и белок выпадает в осадок и при этом утрачивает нативные свойства.
Денатурацию вызывают физические факторы: температура, давление, механические воздействия, ультразвуковые и ионизирующие излучения; химические факторы: кислоты, щелочи, органические растворители, алкалоиды, соли тяжелых металлов.
Различают 2 вида денатурации:
- Обратимая денатурация – ренатурация или ренактивация – это процесс, при котором денатурированный белок, после удаления денатурирующих веществ вновь самоорганизуется в исходную структуру с восстановлением биологической активности.
- необратимая денатурация – это процесс, при котором биологическая активность не восстанавливается после удаления денатурирующих агентов.
Свойства денатурированных белков.
1. Увеличение числа реактивных или функциональных групп по сравнению с нативной молекулой белка (это группы COOH, NH2, SH, OH, группы боковых радикалов аминокислот).
2. Уменьшение растворимости и осаждение белка (связано с потерей гидратной оболочки), развертыванием молекулы белка, с «обнаружением» гидрофобных радикалов и нейтрализации зарядов полярных групп.
3. Изменение конфигурации молекулы белка.
https://www.youtube.com/watch?v=ytpolicyandsafety
4. Потеря биологической активности, вызванная нарушением нативной структуры.
5. Более легкое расщепление протеолитическими ферментами по сравнению с нативным белком – переход компактной нативной структуры в развернутую рыхлую форму облегчает доступ ферментов к пептидным связям белка, которые они разрушают.
Ферментные методы гидролиза основаны на избирательности действия протеолитических ферментов расщепляющих пептидные связи между определенными аминокислотами.
Пепсин расщепляет связи, образованные остатками фенилаланина, тирозина и глутаминовой кислоты.
Трипсин расщепляет связи между аргинином и лизином.
Химотрипсин гидролизует связи триптофана, тирозина и фенилаланина.
Гидрофобные взаимодействия, а также ионные и водородные связи относятся к числу слабых, тк энергия их лишь ненамного превосходит энергию теплового движения атомов при комнатной температуре(т е уже при данной температуре возможен разрыв связей ).
Поддержание характерной для белка конформации возможно благодаря возникновению множества слабых связей между различными участками полипептидной цепи.
Однако, белки состоят из огромного числа атомов , находящихся в постоянном (броуновском) движении, что приводит к небольшим перемещениям отдельных участков полипептидной цепи , которые обычно не нарушают общую структуру белка и его функции. Следовательно, белки обладают конформационной лабильностью – склонностью к небольшим изменениям конформации за счет разрыва одних и образования других слабых связей.

Конформация белка может меняться при изменении химических и физических средств среды, а также при взаимодействии белка с другими молекулами. При этом происходит изменение пространственной структуры не только участка, контактирующего с другой молекулой, но и конформации белка в целом. Конформационные изменения играют роль огромную в функционировании белков в клетке живой.
Денатурация и ренатурация белков
Разрушение нативной конформации сопровождается утратой функции белков, т. е. приводит к потере его биологической активности. Этот процесс называется денатурацией. Денатурация наступает при разрыве слабых связей, ответственных за формирование вторичной, третичной и четвертичной структуры белка. Большинство белков теряют биологическую активность при изменении свойств среды под действием сильных факторов:

Для большинства белков денатурация сопровождается необратимой потерей их биологической активности. Однако известны примеры ренатурации или обратимой денатурации, например, фермента рибонуклеазы. Рибонуклеаза, глобулярный белок, состоящий из 1 полипептидной цепи, при обработке β-меркаптоэтанолом подвергается денатурации и теряет ферментативную активность, глобула расплетается.
Если из среды удалить денатурирующие агенты (путем диализа) каталитическая активность рибонуклеазы восстанавливается, т. е. происходит ренатурация или ренативация белка. Это означает, что рибонуклеаза самопроизвольно восстанавливает из множества возможных комбинаций связей именно один вариант, который возвращает ей биологически активную конформацию.
Шапероновая защита белков in vivo
В клеточной среде белковые молекулы могут иметь нестабильные конформации, находится в неустойчивом состоянии, склонном к агрегации и денатурации. Ренатурация белков в условиях клетки затруднена. Но в организме существуют специальные белки, шапероны, которые способны стабилизировать состояние неустойчивых белков, восстановить нативную конформацию и защитить белки от поражающего воздействия стрессовых ситуаций.
Пространственная структура белка (вторичная и третичная) формируется в процессе трансляции (синтеза белка) по мере роста полипептидной цепи. Однако в условиях клеточной среды при высокой концентрации реакционно-способных биомолекул независимая укладка полипептидной цепи в пространстве затруднена.
Выбор нативной конформации синтезированного белка обеспечивают белки-шапероны.
Завершающий этап формирования трехмерной пространственной структуры, т. е. фолдинг высокомолекулярного белка, осуществляется внутри шаперонового комплекса, состоящего из 14 белковых молекул шаперонов – 60, где, находясь в изоляции от других молекул клеточной среды, белок находит свою единственную, наиболее устойчивую конформацию, обладающую биологической активностью.
Ренатурация, восстановление нативной конформации белков.
https://www.youtube.com/watch?v=ytcopyright
Известно, что в условиях клеточной среды с невысокой скоростью может происходить денатурация белковых молекул. Возвращение активного конформационного состояния белков, т. е. их ренатурация, в клетке осложняется тем, что денатурированные молекулы имеют развернутые полипептидные цепи, обнаженные гидрофобные и другие реакционноспособные участки, устанавливающие связи с другими молекулами, что затрудняет возвращение правильной пространственной структуры.
Шапероны-60 помогают вернуть нативную структуру частично поврежденного белка, который попадает в полость шаперонового комплекса, где нет факторов, мешающих ренативации. После восстановления термодинамически выгодной конформации белок возвращается в цитозоль.
Защита белков от действия поражающих факторов.
Такую защиту осуществляет особая группа шаперонов, называемых индуцибельными, т. е. их синтез в нормальных условиях незачительный, а при действии на организм чрезмерных факторов резко усиливается. Эту группу шаперонов относят к белкам теплового шока, т. к. впервые были обнаружены в клетках, после воздействия на них высокой температуры.
Нарушения фолдинга белковмогут иметь большие клинические последствия. Прионы – белки, которые являются матрицей для нарушения фолдинга собственных клеточных белков PrPc. В результате образуется форма белка PrPSc, содержащая большую долю β-структуры, способная к формированию больших агрегатов и устойчивая к протеолитической деградации.
Прионовые болезни могут начинаться с инфекции (коровье бешенство, скрепи, болезнь Куру) или с мутации (болезнь Крейцфельда-Якоба).
Классификация белков
Простые Сложные
Содержат только содержат белковую часть (апопротеин)
Небелковый компонент сложных белков может быть представлен различными веществами.
Химические свойства белков
По химическому составу белки делятся на две группы:
а) простые белки – протеины, которые при гидролизе распадаются только на аминокислоты;
б) сложные белки или протеиды, образующие при гидролизе аминокислоты и вещества небелковой природы (углеводы, нуклеиновые кислоты и др.) — соединения белковых веществ с небелковыми.
1. Амфотерные свойства белков
Как и аминокислоты, белки являются амфотерными соединениями, так как молекула любого белка содержит на одном конце группу -NH2, а на другом конце – группу -СООН.
Так, при действии щелочей белок реагирует в форме аниона – соединяется с катионом щелочи:

При действии же кислот он выступает в форме катиона:

Если в молекуле белка преобладают карбоксильные группы, то он проявляет свойства кислот, если же преобладают аминогруппы, — свойства оснований.
Очень важным для жизнедеятельности живых организмов является буферное свойство белков, т.е. способность связывать как кислоты, так и основания, и поддерживать постоянное значение рН различных систем живого организма.
Белки обладают и специфическими физико-химическими свойствами.
2. Денатурация белка (необратимое осаждение, свертывание)
Денатурация – это разрушение вторичной и третичной структуры белка (полное или частичное) и изменение его природных свойств с сохранением первичной структуры белка.
Сущность денатурации белка сводится к разрушению связей, обусловливающих вторичную и третичную структуры молекулы (водородных, солевых и других мостиков). А это приводит к дезориентации конфигурации белковой молекулы.
Денатурация бывает обратимой и необратимой.
Обратимая денатурация белка происходит при употреблении алкоголя, солёной пищи.
Необратимая денатурация может быть вызвана при действии таких реагентов, как концентрированные кислоты и щелочи, спирты, в результате воздействия высокой температуры, радиации, при отравлении организма солями тяжелых металлов (Hg2+, Pb2+, Си2+).
Например, яичный белок альбумин осаждается из раствора (свертывается) при варке яиц (при температуре 60-70С), теряя способность растворяться в воде.
Видеоопыт «Свертывание белков при нагревании»
Видеоопыт «Осаждение белков солями тяжелых металлов»
Видеоопыт «Осаждение белков спиртом»

3. Гидролиз белков
Гидролиз белков – это необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот.
Анализируя продукты гидролиза, можно установить количественный состав белков.
Переваривание белков в организме по своей сути представляет ферментативный гидролиз белковых молекул.
В лабораторных условиях и в промышленности проводится кислотный гидролиз.
В ходе гидролиза белков происходит разрушение пептидных связей. Гидролиз белка имеет ступенчатый характер:
4. Цветные (качественные) реакции на белки
Для белков известно несколько качественных реакций.
а) Ксантопротеиновая реакция (на остатки аминокислот, содержащих бензольные кольца)
Белки, содержащие остатки ароматических аминокислот (фенилаланина, тирозина), дают желтое окрашивание при действии концентрированной азотной кислоты.
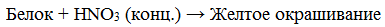
Причина появления окраски – образование нитропроизводных ароматических аминокислот, например, фенилаланина: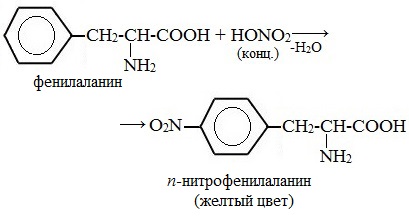
Видеоопыт «Ксантопротеиновая реакция на белки»
б) Биуретовая реакция (на пептидные связи)
Все соединения, содержащие пептидную связь, дают фиолетовое окрашивание при действии на них солей меди (II) в щелочном растворе.
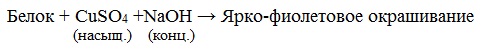
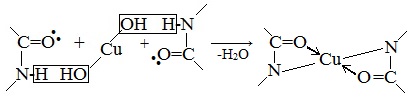
Причина появления окраски – образование комплексных соединений с координационным узлом:
Видеоопыт «Биуретовая реакция белков»
Видеоопыт «Качественные реакции на белки: биуретовая и ксантопротеиновая»
в) Цистеиновая реакция (на остатки аминокислот, содержащих серу)
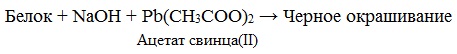
Причина появления окраски – образование черного осадка сульфида серебра (II) PbS.
Видеоопыт «Качественное определение азота в органических соединениях»
Рубрики: Белки
Последствия
После денатурации происходит переход нативной компактной структуры в рыхлую развернутую форму, упрощается проникновение к пептидным связям ферментов, необходимых для разрушения.
https://www.youtube.com/watch?v=https:accounts.google.comServiceLogin
Конформация белковых молекул определяется возникновением достаточного количества связей между разными участками определенной полипептидной цепочки.
Белки, состоящие из достаточного количества атомов, которые находятся в непрерывном хаотичном движении, способствует определенным перемещениям частей полипептидной цепи, что вызывает нарушение общей структуры белков, снижение его физиологических функций.
Белки имеют конформационную лабильность, то есть предрасположенность к незначительным изменениям конформации, происходящим в результате обрыва одних и образования других связей.
Механизм
В некоторых случаях используют для денатурации мочевину либо гуанидинхлорид, которые способны образовывать водородные связи с карбонильными или аминогруппами пептидного вида, а также с частью радикала аминокислот.
При этом они подменяют существующие в белковой молекуле внутримолекулярные водородные связи, что приводит к изменению вторичной и третичной структуры биополимеров. Денатурация белков зависит от присутствия в молекуле дисульфидных связей.
Например, в ингибиторе трипсана (панкреатическом белке) присутствуют дисульфидные мостики. При их восстановлении денатурация осуществляется без применения иных денатурирующих компонентов. При последующем помещении белка в окислительные условия, SH-групп цистеина окисляется.
В результате химического взаимодействия происходит восстановление исходной конформации. Наличие одной дисульфидной связи способствует существенному повышению стабильности всей пространственной структуры.
Денатурация — это процесс, приводящий к уменьшению растворимости белковой молекулы. В результате его происходит образование осадка «свернувшегося» белка. При высокой концентрации в растворе биополимера наблюдается полная «свертываемость» массы раствора.
Примером такого явления будут превращения, наблюдаемые при варке куриного яйца. Денатурация ДНК предполагает полную утрату биологической активности белка. Именно эти свойства способствовали использованию в качестве антисептика раствора карболовой кислоты.
Высокая вероятность разрушения структуры белковых молекул создает огромное количество сложностей в их выделении, изучении, практическом использовании в промышленных и медицинских целях.
Лабильность пространственной структуры белков и их денатурация. Факторы, вызывающие денатурацию.
Лабильность белка — склонность к небольшим изменениям конформации за счет разрыва одних и образовании других слабых связей. Конформация белка может меняться при изменении химических и физических свойств среды, а также при взаимодействии белка с другими молекулами. При этом происходит изменение пространственной структуры не только участка, контактирующего с другой молекулой, но и конформация в целом.
Какие факторы способны денатурировать белок? Многочисленные.1. Высокая температура, более 50 градусов по Цельсию. Увеличивается тепловое движение, связи рвутся.2. Интенсивное стряхивание раствора, когда происходит контакт с воздушной средой и происходит изменение конфомации молекул.3. Органические вещества (этиловый спирт, фенол и др.
) спсобные взаимодействовать с функциональными группами аминокислот, что приводит, догадайтесь, правильно!, к изменению конформации. 3. Кислоты и щелочи, изменением рН среды приводят к перераспределению связей в белке.4. Соли ТЯЖЁЛЫХ металлов, образуют прочные связи с функциональными группами, меняя активность и конформацию.5.
https://www.youtube.com/watch?v=ytabout
14. Шапероны – класс белков, защищающий другие белки от денатурации в условиях клетки и облегчающий формирование их нативной конформации.
Классифицируются следующим образом — по молекулярной массе на 6 основных групп:1. высокомолекулярные с мол.массой от 100 до 110 кД.2.
Свойства денатурированных белков, виды денатурации
Денатурация – это процесс нарушения высших уровней организации белковой молекулы (вторичного, третичного, четвертичного) под действием различных факторов.
При этом полипептидная цепь разворачивается и находится в растворе в развернутом виде или в виде беспорядочного клубка.
При денатурации утрачивается гидратная оболочка и белок выпадает в осадок и при этом утрачивает нативные свойства.
Денатурацию вызывают физические факторы: температура, давление, механические воздействия, ультразвуковые и ионизирующие излучения; химические факторы: кислоты, щелочи, органические растворители, алкалоиды, соли тяжелых металлов.
Различают 2 вида денатурации:
- Обратимая денатурация – ренатурация или ренактивация – это процесс, при котором денатурированный белок, после удаления денатурирующих веществ вновь самоорганизуется в исходную структуру с восстановлением биологической активности.
- необратимая денатурация – это процесс, при котором биологическая активность не восстанавливается после удаления денатурирующих агентов.
Свойства денатурированных белков.
1. Увеличение числа реактивных или функциональных групп по сравнению с нативной молекулой белка (это группы COOH, NH2, SH, OH, группы боковых радикалов аминокислот).
2. Уменьшение растворимости и осаждение белка (связано с потерей гидратной оболочки), развертыванием молекулы белка, с «обнаружением» гидрофобных радикалов и нейтрализации зарядов полярных групп.
3. Изменение конфигурации молекулы белка.
4. Потеря биологической активности, вызванная нарушением нативной структуры.
5. Более легкое расщепление протеолитическими ферментами по сравнению с нативным белком – переход компактной нативной структуры в развернутую рыхлую форму облегчает доступ ферментов к пептидным связям белка, которые они разрушают.
Ферментные методы гидролиза основаны на избирательности действия протеолитических ферментов расщепляющих пептидные связи между определенными аминокислотами.
Пепсин расщепляет связи, образованные остатками фенилаланина, тирозина и глутаминовой кислоты.
Трипсин расщепляет связи между аргинином и лизином.
Химотрипсин гидролизует связи триптофана, тирозина и фенилаланина.
Гидрофобные взаимодействия, а также ионные и водородные связи относятся к числу слабых, тк энергия их лишь ненамного превосходит энергию теплового движения атомов при комнатной температуре(т е уже при данной температуре возможен разрыв связей ).
Поддержание характерной для белка конформации возможно благодаря возникновению множества слабых связей между различными участками полипептидной цепи.
Однако, белки состоят из огромного числа атомов , находящихся в постоянном (броуновском) движении, что приводит к небольшим перемещениям отдельных участков полипептидной цепи , которые обычно не нарушают общую структуру белка и его функции. Следовательно, белки обладают конформационной лабильностью – склонностью к небольшим изменениям конформации за счет разрыва одних и образования других слабых связей. Конформация белка может меняться при изменении химических и физических средств среды, а также при взаимодействии белка с другими молекулами. При этом происходит изменение пространственной структуры не только участка, контактирующего с другой молекулой, но и конформации белка в целом. Конформационные изменения играют роль огромную в функционировании белков в клетке живой.
Справочник химика 21
Фактически наступающая необратимость создается, как оказалось, сопутствующими реакциями — агрегацией белка, окислением SH-групп с образованием новых дисульфидных (S—S) связей и пр. Если эти реакции в достаточной мере исключены, то тенденция к возвращению белка в нативное состояние (ренатурация) проявляет себя сразу же по прекращении действия денатурирующего агента.
Если Д. по существу представляет собой физ. переход упорядоченность — беспорядок, то в ренатурации ярко проявляется биол, особенность белков — способность к самоорганизации, путь к-рой определен строением полипептидной цепи, т. е. наследственной информацией. В условиях живой клетки данная информация, вероятно, является решающей для преобразования беспорядочной полипептидной цепи во время или после ее биосинтеза на рибосоме в нативную молекулу белка.
Библиография: Белицер В. А. Макроструктура и денатурационные превращения белков, Укр. биохим, журн., т. 24, в. 2, с. 290, 1962, библиогр.; Ж о л и М. Физическая химия денатурации белков, пер. с англ., М., 1968, библиогр.; Пти-ц ы н О. Б. Физические принципы самоорганизации белковых цепей, Усп. совр, биол., т. 69, в. 1, с. 26, 1970, библиогр.; Anfinsen С. В. The formation and stabilization of protein structure, Biochem. J., v. 128, p. 737, 1972, bibliogr.; Anfinsen G. B. a. Scheraga H. A. Experimental and theoretical aspects of protein folding, Advanc. Protein Chem., v. 29, p. 205, 1975, bibliogr.; Morawetz H. Rate of conformational transitions in biological macromolecules and their analogs, ibid., v. 26, p. 243, 1972, bibliogr.
В. А. Белицер.
Основные свойства белков
Структура и свойства белков могут изменяться под влиянием разных физико-химических факторов: действие концентрированных кислот и щелочей, тяжелых металлов, изменение температуры и т. п. Одни из белков легко изменяют структуру под незначительным действием разнообразных факторов, другие – стойкие к подобным влияниям. Основные свойства белка это – денатурация, ренатурация, деструкция.
Денатурация
Денатурация – это процесс нарушения естественной структуры белка с сохранением пептидных связей (первичной структуры). Может быть необратимым процессом. Но при условии прекращения действия отрицательных факторов на первых стадиях белок может восстанавливать свое нормальное состояние, то есть происходит обратная денатурация – ренатурация.
Ренатурация
Ренатурация – это способность белка восстанавливать нормальную структуру после устранения действия отрицательных факторов. Выполнение некоторых функций – двигательной, сигнальной, каталитической и т. п. – у живых организмов связано с частичной обратной денатурацией белков.
Особенности процесса
Он сопровождается разворачиванием полипептидной связи, которая в растворе изначально представлена в виде беспорядочного клубка.
Процесс денатурации белка сопровождается утрачиванием гидратной оболочки, выпадением белка в осадок, утрачиванием им нативных свойств.
Среди основных факторов, которые провоцируют процесс денатурации, выделим физические параметры: давление, температуру, механическое действие, ионизирующее и ультразвуковое излучение.
Денатурация белка происходит под воздействием органических растворителей, минеральных кислот, щелочей, солей тяжелых металлов, алкалоидов.

Заключение
Белковые молекулы, обладающие одинаковой либо схожей конформацией, способны иметь существенные различия в первичной структуре. При этом отличающиеся аминокислоты аналогичны по химико-физическим характеристикам боковых цепей. В процессе денатурации происходит разворачивание молекулы, она лишается способности выполнять свое биологическое предназначение.
При ультрафиолетовом либо инфракрасном излучении происходит передача кинетической энергии биополимеру, в результате чего возникает вибрация его атомов. Это вызывает полное разрушение водородных связей, провоцирует свертывание белковой молекулы.
Заключение
Температура денатурации белков превышает 56 градусов Цельсия. Типичными признаками прохождения необратимой денатурации белковых молекул считаются снижение растворимости и гидрофильности молекул, повышение оптической активности, понижение стойкости белковых растворов, увеличение вязкости.
https://www.youtube.com/watch?v=ytpress
Денатурацию используют в ветеринарии, медицине, клинике, фармации, при проведении биохимических исследований, связанных с осаждением в биологическом материале протеина. Далее проводится идентификация в исследуемом растворе небелковых и низкомолекулярных инстанций, в результате чего можно установить количественное содержание веществ. В настоящее время ищут способы защиты белковых молекул от разрушения.