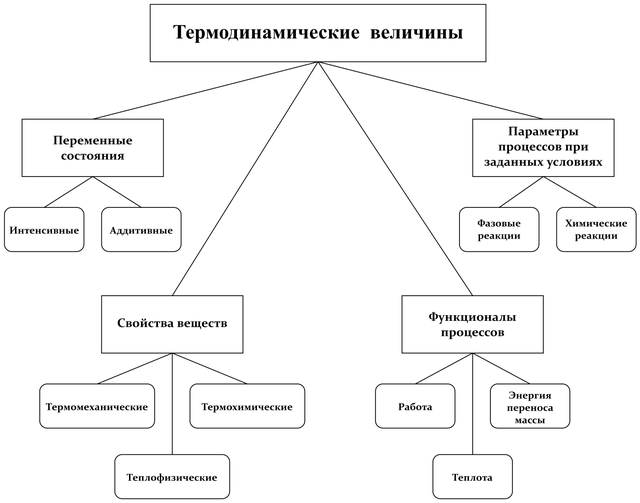
Системные модели
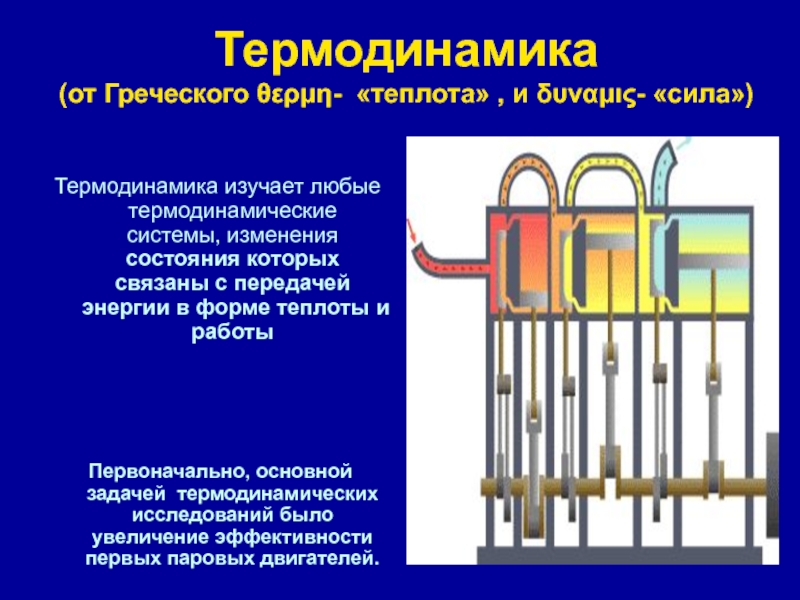
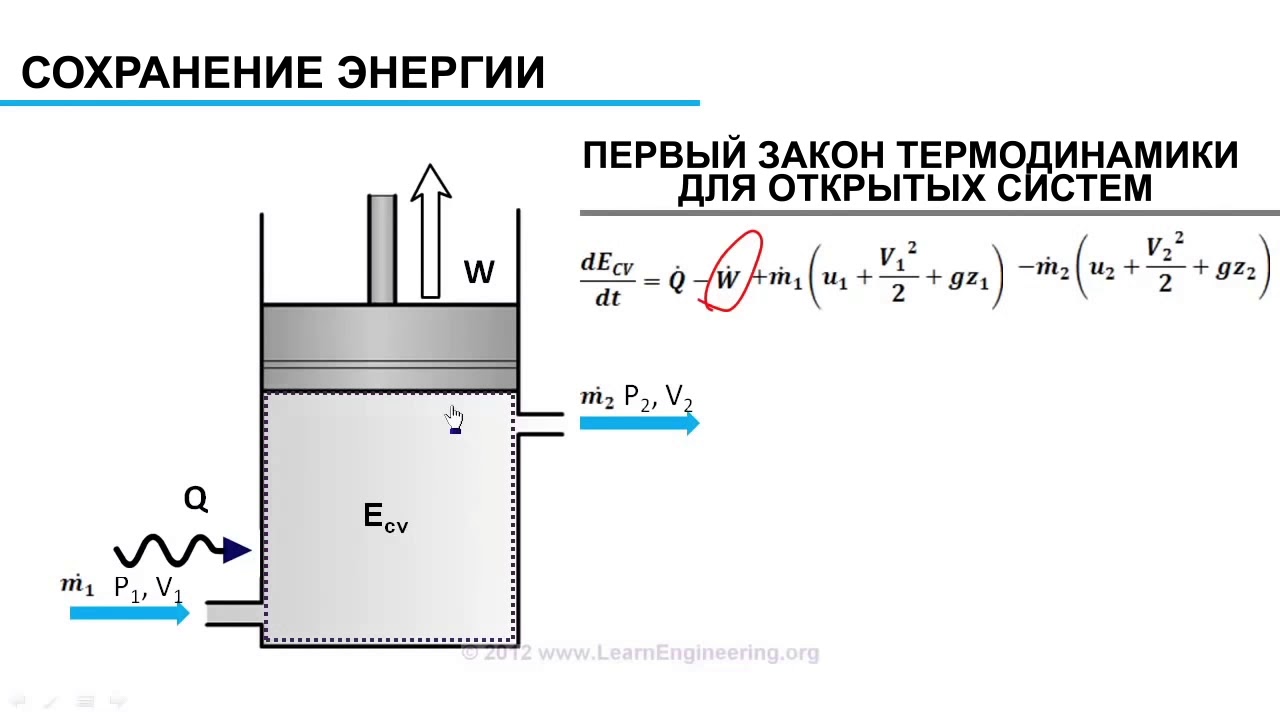
Схема типовой термодинамической системы
Важным понятием термодинамики является термодинамическая система , которая представляет собой точно определенную область исследуемой Вселенной. Все во Вселенной, кроме системы, называется окружением . Система отделена от остальной Вселенной границей, которая может быть физической или условной, но служит для ограничения системы конечным объемом. Отрезки границы часто называют стенами ; у них есть соответствующие определенные «проницаемости». Передача энергии в виде работы , тепла или материи между системой и окружающей средой происходит через стены в зависимости от их проницаемости.
Материя или энергия, которые проходят через границу, чтобы вызвать изменение внутренней энергии системы, должны быть учтены в уравнении баланса энергии. Объем, содержащийся в стенках, может быть областью, окружающей отдельный атом, резонирующий с энергией, такой как Макс Планк, определенный в 1900 году; это может быть тело пара или воздуха в паровой машине , такой как Сади Карно определил в 1824 году. Система также могла быть всего лишь одним нуклидом (то есть системой кварков ), как предполагалось в квантовой термодинамике . Когда свободнее точка зрения принимается, и требование термодинамического равновесия падает, система может быть тело тропического циклона , такие как Керри Эмануэль теоретизировал в 1986 году в области атмосферной термодинамики , или горизонта событий в виде черной дыры .
Границы бывают четырех типов: фиксированные, подвижные, реальные и мнимые. Например, в двигателе фиксированная граница означает, что поршень заблокирован в своем положении, в котором может происходить процесс постоянного объема. Если поршню позволяют перемещаться, эта граница является подвижной, в то время как границы цилиндра и головки цилиндра фиксированы. Для закрытых систем границы реальны, в то время как для открытых систем границы часто являются воображаемыми. В случае реактивного двигателя можно предположить фиксированную воображаемую границу на входе в двигатель, фиксированные границы вдоль поверхности корпуса и вторую фиксированную воображаемую границу поперек выпускного сопла.
В целом термодинамика различает три класса систем, определяемых с точки зрения того, что может пересекать их границы:
| Тип системы | Массовый поток | работай | Высокая температура |
|---|---|---|---|
| N | |||
| Термически изолированный | N | N | |
| Механически изолирован | N | N | |
| Изолированные | N | N | N |
Со временем в изолированной системе внутренние различия давления, плотности и температуры имеют тенденцию выравниваться. Система , в которой пошли к завершению все уравнительные процессы , как говорят, в состоянии от термодинамического равновесия .
Находясь в термодинамическом равновесии, свойства системы по определению не изменяются во времени. Равновесные системы намного проще и легче понять, чем системы, которые не находятся в равновесии. Часто при анализе динамического термодинамического процесса делается упрощающее допущение, что каждое промежуточное состояние в процессе находится в равновесии, вызывая термодинамические процессы, которые развиваются так медленно, что позволяют каждому промежуточному этапу быть равновесным состоянием и считаются обратимыми процессами. .
Частные случаи
Рассмотрим несколько частных случаев:
- Если q>,{\displaystyle q>0,} то это означает, что теплота к системе подводится.
- Если q<,{\displaystyle q<0,} то это означает, что теплота от системы отводится.
- Если q=,{\displaystyle q=0,} то система или не обменивается теплотой с окружающей средой по одной из причин: либо она находится с ней в состоянии термодинамического равновесия, либо является адиабатически изолированной, или находится в состоянии стационарного теплообмена.
Обобщая: в конечном процессе 1→2{\displaystyle 1\to 2} элементарные количества теплоты могут быть любого знака. Общее количество теплоты, которое мы назвали просто q{\displaystyle q} — это алгебраическая сумма количеств теплоты, сообщаемых на всех участках этого процесса. В ходе процесса теплота может поступать в систему или уходить из неё разными способами.
При отсутствии потоков энергии, когда q={\displaystyle q=0}, выполнение системой работы w{\displaystyle w} приводит к тому, что δU<{\displaystyle \delta U<0}, и энергия системы U{\displaystyle U} убывает. Поскольку запас внутренней энергии U{\displaystyle U} ограничен, то процесс, в котором система бесконечно долгое время выполняет работу без подвода энергии извне, невозможен, что запрещает существование вечных двигателей первого рода.
при кругом (циклическом) процессе (ΔU=0){\displaystyle (\Delta U=0)}
- W=−Q{\displaystyle W=-Q} в термодинамической системе знаков
- W=Q {\displaystyle W=Q~~~} в теплотехнической системе знаков
при изобарном процессе
- Q=ΔU+W=ΔU+pΔV{\displaystyle Q=\Delta U+W=\Delta U+p\Delta V}
при изохорном процессе (W=0{\displaystyle W=0})
- Q=ΔU=mMCVΔT{\displaystyle Q=\Delta U={m \over M}C_{V}\Delta T}
при изотермическом процессе (ΔU=0){\displaystyle (\Delta U=0)}
- Q=W=mMRTlnV2V1{\displaystyle Q=W={m \over M}RT\ln {V_{2} \over V_{1}}}
Здесь m{\displaystyle \ m} — масса газа, M{\displaystyle \ M} — молярная масса газа, CV{\displaystyle \ C_{V}} — молярная теплоёмкость при постоянном объёме, p,V,T{\displaystyle \ p,V,T} — давление, объём и температура газа соответственно, причём последнее равенство верно только для идеального газа.
Марина Мелия «Отстаньте от ребенка! Простые правила мудрых родителей»
Потенциал Гиббса.
В тех случаях, когда изменяться могут и температура и давление, используется более общая функция
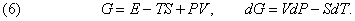
Эту функцию иногда называют полным термодинамическим потенциалом или полезной энергией, но сейчас ее принято называть потенциалом Гиббса или гиббсовой энергией и обозначать символом G по имени Дж.Гиббса (1839–1903). Как будет показано ниже, представленные термодинамические функции позволяют определить условия, необходимые для равновесия.
В случае повышения давления на малую величину dP в системе, поддерживаемой при постоянной температуре (dT = 0), потенциал Гиббса увеличится на величину dG, а скорость его увеличения, или «чувствительность» потенциала Гиббса G к изменениям давления, дается термодинамическим выражением для объема системы
где символ частной производной указывает на то, что изменение происходит при постоянных значениях всех других параметров (в данном случае температуры T).
и это равенство можно рассматривать как еще одно определение энтропии.
Плохие приметы о Ваньке мокром
Термодинамический процесс
Если меняется хотя бы один из макроскопических параметров, то говорят, что в системе происходит термодинамический процесс. Такой процесс может возникнуть, если изменяются внешние параметры или система начинает получать или передавать энергию. В результате она переходит в другое состояние.
Вспомним пример с чаем в термосе. Если мы опустим в чай кусочек льда и закроем термос, то сразу же появится разница в температурах в разных частях жидкости. Жидкость в термосе будет стремиться к выравниванию температур. Из областей с более высокой температурой тепло будет передаваться туда, где температура ниже. То есть, будет происходить термодинамический процесс. В конце концов, температура чая в термосе снова станет одинаковой. Но она уже будет отличаться от первоначальной температуры. Состояние системы изменилось, так как изменилась её температура.
Термодинамический процесс происходит, когда ночью остывает песок, нагретый на пляже в жаркий день. К утру его температура понижается. Но как только взойдёт солнце, процесс нагревания начнётся снова.
О чем говорит руна в аспекте личных отношений
При прямом положении руны в раскладе на ситуацию в отношениях стоит принять во внимание тот факт, что стоит поговорить по душам с любимыми и близкими. Непонимание и обиды, накопившиеся за время отношений, могут погубить любовь

Рунический символ «Турисаз» в прямом положении при раскладе на отношения говорит, что спрашивающему необходимо по душам поговорить со своей второй половиной
Руна Турисаз, выпавшая перевернутой, говорит о том, что может случиться незначительный конфликт, который не несет в себе особой угрозы. Человек может продолжать жить прежним образом. Но если застой в любви не устраивает, то пришло время все изменить.
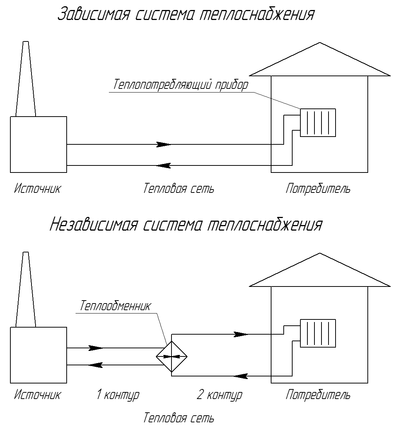
Теплопередача
Теплопередачей называют физический процесс передачи тепловой энергии (теплоты) от одного тела к другому либо при непосредственном контакте, либо через разделяющую перегородку. Как правило, теплота передаётся от более тёплого тела к более холодному. Это процесс заканчивается, когда система приходит в состояние термодинамического равновесия.
Энергия, которую получает или отдаёт тело при теплопередаче, называется количеством теплоты.
По способу передачи теплоты теплообмен можно разделить на 3 вида: теплопроводность, конвенция, тепловое излучение.
Теплопроводность
Если между телами или частями тел существует температурная разница, то между ними будет происходить процесс теплопередачи. Теплопроводностью называют процесс переноса внутренней энергии от более нагретого тела (или его части) к менее нагретому телу (или его части).
К примеру, нагрев на огне один конец стального прута, через некоторое время мы почувствуем, что и другой его конец также становится тёплым.
Стеклянную палочку, один конец которой раскалён, мы легко держим за другой конец, не обжигаясь. Но если мы попробуем проделать такой же эксперимент с железным прутом, у нас ничего не получится.
Разные вещества по-разному проводят тепло. Каждое из них имеет свой коэффициент теплопроводности, или удельной проводимости, численно равный количеству теплоты, которая проходит через образец толщиной 1 м, площадью 1 м2 за 1 секунду. За единицу температуры принимают 1 К.
Лучше всего проводят тепло металлы. Это их свойство мы используем в быту, готовя пищу в металлических кастрюлях или на сковородках. А вот их ручки не должны нагреваться. Поэтому их делают из материалов с плохой теплопроводностью.
Теплопроводность жидкостей меньше. А газы обладают слабой теплопроводностью.
Мех животных также плохо проводит тепло. Благодаря этому они не перегреваются в жаркую погоду и не замерзают в холодную.
Конвенция
При конвенции теплота передаётся струями и потоками газа или жидкости. В твёрдых телах конвенции нет.
Как возникает конвенция в жидкости? Когда мы ставим на огонь чайник с водой, нижний слой жидкости нагревается, его плотность уменьшается, он движется вверх. Его место занимает более холодный слой воды. Через какое-то время он тоже нагреется и тоже поменяется местами с более холодным слоем. И т.д.
Подобный процесс происходит и в газах. Не случайно батареи отопления размещают в нижней части комнаты. Ведь нагретый воздух всегда поднимается в верхнюю часть комнаты. А нижний, холодный, наоборот, опускается. Затем он нагревается также и вновь поднимается, а верхний слой за это время остывает и опускается.
Конвенция бывает естественная и принудительная.
Естественная конвенция постоянно происходит в атмосфере. В результате этого происходят постоянные перемещения тёплых воздушных масс вверх, а холодных — вниз. В результате возникает ветер, облака и другие природные явления.
Когда естественной конвенции недостаточно, применяю принудительную конвенцию. Например, потоки тёплого воздуха перемещают в комнате с помощью лопастей вентилятора.
Тепловое излучение
Солнце нагревает Землю. При этом не происходит ни теплопередачи, ни конвенции. Так почему же тела получают тепло?
Дело в том, что Солнце является источником теплового излучения.
Тепловое излучение — это электромагнитное излучение, возникающее за счёт внутренней энергии тела. Все окружающие нас тела излучают тепловую энергию. Это может быть видимое световое излучение настольной лампы, или источники невидимых ультрафиолетовых, инфракрасных или гамма-лучей.
Но тела не только излучают тепло. Они его также и поглощают. Одни в большей степени, другие в меньшей. Причём тёмные тела и нагреваются, и охлаждаются быстрее, чем светлые. В жаркую погоду мы стараемся надеть светлую одежду, потому что она поглощает меньше тепла, чем одежда тёмных тонов. Автомобиль тёмного цвета нагревается на солнце гораздо быстрее, чем стоящий с ним рядом автомобиль, имеющий светлую окраску.
Это свойство веществ по-разному поглощать и излучать тепло используется при создании систем ночного видения, систем самонаведения ракет на цель и др.
Энтропия.
Тепловая энергия dQў, которая не может быть преобразована в работу, пропорциональна нижней температуре T, так что можно записать dQў = TdS, где dS – приращение энтропии S системы. Как и E, величина S является характеристикой самой системы, а потому мы обозначаем ее приращение буквой d, а не d.
Обозначив через dW работу, которую можно получить за счет теплоты dQ, можно написать

Если рабочее тело в результате некоего термодинамического процесса не возвращается в исходное состояние, то значительная часть энергии оказывается бесполезной с точки зрения совершения работы, и внутренняя энергия увеличивается на соответствующую разность dE. Увеличение внутренней энергии может проявиться в изменении физического состояния рабочего тела, например в переходе из твердого в жидкое состояние (плавлении) или из жидкого в газообразное (испарении). Такая тепловая энергия называется теплотой плавления и теплотой парообразования соответственно. Повышение внутренней энергии может быть связано также с химическими изменениями (диссоциацией, разрывом связей) и даже с делением ядер.
Проблемы энергетики и охрана окружающей среды
Тепловые двигатели широко применяются на транспорте и в энергетике (тепловые и атомные электростанции). Использование тепловых двигателей сильно влияет на состояние биосферы Земли. Можно выделить следующие вредные факторы:
- при сжигании топлива используется кислород из атмосферы, что приводит к снижению содержания кислорода в воздухе;
- при сгорании топлива в атмосферу выделяется углекислый газ. Концентрация углекислого газа в атмосфере повышается. Это изменяет прозрачность атмосферы, так как молекулы углекислого газа поглощают инфракрасное излучение, что ведет к повышению температуры (парниковый эффект);
- при сжигании угля в атмосферу поступают азотные, серные соединения и соединения свинца, вредные для здоровья человека.
Решение проблемы охраны окружающей среды от вредного воздействия предприятий тепловой энергетики требует комплексного подхода. Массовыми загрязнителями при работе тепловых электростанций являются летучая зола, диоксид серы и оксиды азота. Методы сокращения выбросов зависят от свойств топлива и условия его сжижения. Предотвращение загрязнения летучей золой достигается очисткой всего объема продуктов сгорания твердого топлива в высокоэффективных золоуловителях. Сокращение выбросов оксидов азота с продуктами сгорания топлива на тепловых электростанциях, а также в парогазовых и газотурбинных установках обеспечивается, главным образом, технологией сжигания топлива. Уменьшение выброса диоксида серы может быть достигнуто различными методами облагораживания и переработки топлива вне тепловых электростанций либо непосредственно на тепловых электростанциях, а также очисткой дымовых газов.
Контроль за выбросом вредных веществ электростанций осуществляется специальными приборами.
В ряде случаев достаточно эффективным решением вопросов очистки выбросов в атмосферу остается сооружение фильтров-уловителей и дымовых труб. У дымовой трубы два назначения: первое — создавать тягу и тем самым заставлять воздух — обязательный участник процесса горения — в нужном количестве и с должной скоростью входить в топку; второе — отводить продукты горения (вредные газы и имеющиеся в дыме твердые частицы) в верхние слои атмосферы. Благодаря непрерывному турбулентному движению вредные газы и твердые частицы уносятся далеко от источника их возникновения и рассеиваются.
Для рассеивания сернистого ангидрида, содержащегося в дымовых трубах тепловых электростанций, сооружаются дымовые трубы высотой 180, 250 и 320 м. Тепловые электростанции России, работающие на твердом топливе, за год выбрасывают в отвалы около 100 млн т золы и шлаков. Зола и шлаки занимают большие площади земель, неблагоприятно влияют на окружающую среду.
Более половины всех загрязнений создает транспорт. Один из путей решения проблемы защиты окружающей среды заключается в переходе на дизельные двигатели, электродвигатели, повышение КПД.
Алгоритм решения задач раздела «Термодинамика»:
- выделить систему тел и определить ее тип (замкнутая, адиабатически замкнутая, замкнутая в механическом смысле, незамкнутая);
- выяснить, как изменяются параметры состояния \( (p,V,T) \) и внутренняя энергия каждого тела системы при переходе из одного состояния в другое;
- записать уравнения, связывающие параметры двух состояний системы, формулы для расчета изменения внутренней энергии каждого тела системы при переходе из одного состояния в другое;
- определить изменение механической энергии системы и работу внешних сил по изменению ее объема;
- записать формулу первого закона термодинамики или закона сохранения и превращения энергии;
- решить систему уравнений относительно искомой величины;
- проверить решение.
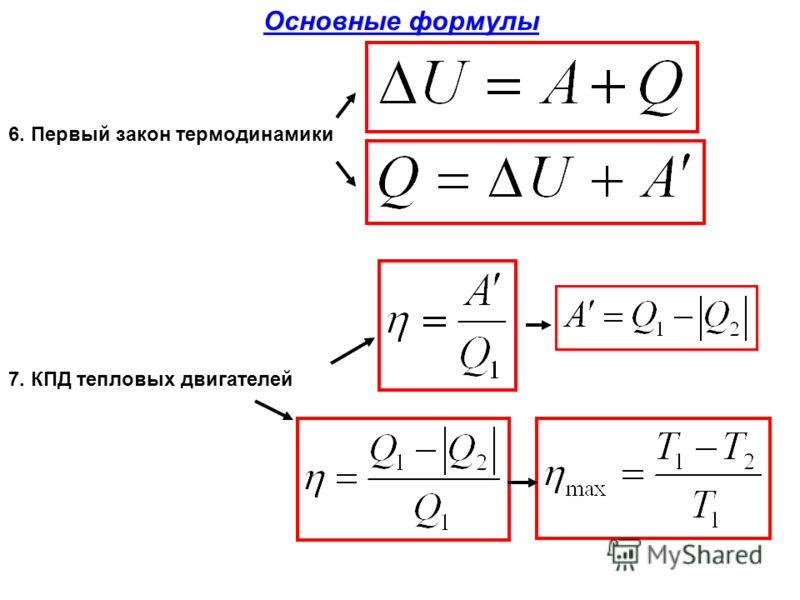
Основные формулы раздела «Термодинамика»
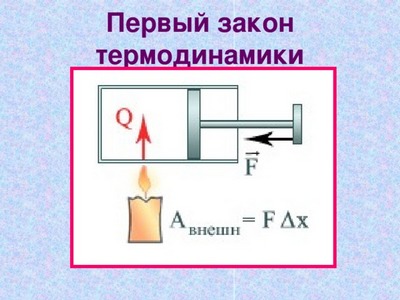
Изменение внутренней энергии механической работой
Бенджамин Румфорд
Внутреннюю энергию тела можно изменить, совершив над ней механическую работу. Если работа совершается над телом, то механическая энергия превращается во внутреннюю энергию. А если работу совершает тело, то его внутренняя энергия превращается в механическую.
Почти до конца XIX века считалось, что существует невесомое вещество — теплород, которое передаёт тепло от тела к телу. Чем больше теплорода втекает в тело, тем теплее оно будет, и наоборот.
Однако в 1798 г. англо-американский учёный граф Бенджамин Румфорд стал сомневаться в теории теплорода. Причиной тому были нагревания стволов пушек при сверлении. Он предположил, что причиной нагревания является механическая работа, которая совершается во время трения сверла о ствол.
И Румфорд провёл эксперимент. Чтобы увеличить силу трение, взяли тупое сверло, а сам ствол поместили в бочку с водой. К концу третьего часа сверления вода в бочке закипела. Это означало, что ствол получил тепло при совершении механической работы над ним.
Сопряженные переменные
Центральное понятие термодинамики — это энергия , способность выполнять работу . Согласно Первому закону сохраняется полная энергия системы и ее окружения. Энергия может передаваться в систему путем нагрева, сжатия или добавления вещества и извлекаться из системы путем охлаждения, расширения или извлечения вещества. В механике , например, передача энергии равна произведению силы, приложенной к телу, и результирующего смещения.
Сопряженные переменные — это пары термодинамических концепций, первая из которых сродни «силе», приложенной к некоторой термодинамической системе , вторая — сродни результирующему «смещению», а произведение двух равняется количеству переданной энергии. Общие сопряженные переменные:
- Давление — объем ( механические параметры);
- Температура — энтропия (тепловые параметры);
- Химический потенциал — число частиц (параметры материала).
Сонник — Лук репчатый
Вы сделаете открытие, возможно денежное вознаграждение. Если вы едите лук — это к семейным ссорам. Вы выбрасываете лук — возможен разлад в семье. Покупаете лук — скорая награда. Разные цыгане дают различные толкования таких сновидений, обычно лук связывают с судьбой, доброй или злой. Есть лук, по мнению одних цыган — значит, что вам возвратят украденную собственность. Многие цыгане считают, что есть лук — к запутанному спору, возможно, с собственной семьей. Выбрасывать лук — к разрыву отношений с супругом или любимым человеком. Если вы покупаете лук — получите неожиданную награду.
Термодинамическое равновесие
Это понятие также введено в термодинамику, как обобщение результатов экспериментов.
Термодинамическим равновесием называют такое состояние системы, при котором все её макроскопические величины — температура, давление, объём и энтропия — не изменяются во времени, если система является изолированной. В такое состояние может самопроизвольно перейти любая замкнутая термодинамическая система, если остаются постоянными все внешние параметры.
Самый простой пример системы в состоянии термодинамического равновесия — термос с горячим чаем. Температура в нём одинакова в любой точке жидкости. Хотя термос можно назвать изолированной системой лишь приблизительно.
Любая замкнутая термодинамическая система самопроизвольно стремится перейти в термодинамическое равновесие, если не меняются внешние параметры.
Цикл Карно.
К 1824, когда Карно опубликовал свой трактат Размышления о движущей силе огня… (Réflections sur la puissance motrice du feu…), было уже хорошо известно, что за счет теплоты можно получать механическую энергию, но ни у кого не было ни малейшего представления о том, каким может быть КПД тепловой машины, и были не совсем ясны термодинамические основы ее действия. Прошло десять лет, прежде чем Б.Клапейрон, который первым по достоинству оценил трактат Карно, повторно опубликовал его, снабдив важными дополнениями. Карно представлял тепловую машину (рис. 2) в виде идеально теплоизолированного цилиндра, наполненного фиксированным количеством рабочего тела (газа) и снабженного движущимся без трения поршнем. Машину можно без энергетических потерь переносить с одной подставки на другую. Одна подставка, поддерживаемая при температуре T1, служит нагревателем. Другую, поддерживаемую при более низкой температуре T2, назовем холодильником. Сначала цилиндр стоит на нагревателе, и газообразное рабочее тело изотермически (т.е. поглощая теплоту так, что его температура не изменяется) расширяется от точки 1 до точки 2 на графике зависимости объем – давление (рис. 3,а). Затем машину переносят на теплоизолированную подставку и газ адиабатически расширяется от точки 2 до точки 3, совершая работу – поднимая поршень. В результате он охлаждается до температуры T2. После этого машину переставляют на холодильник, и газ изотермически сжимается от точки 3 до точки 4, отдавая теплоту холодильнику. Переставив затем машину снова на теплоизолированную подставку, можно теперь адиабатически сжать газ от точки 4 до точки 1 и вернуть его в исходное состояние (к прежним значениям температуры, объема и давления), так что цикл может начаться снова.

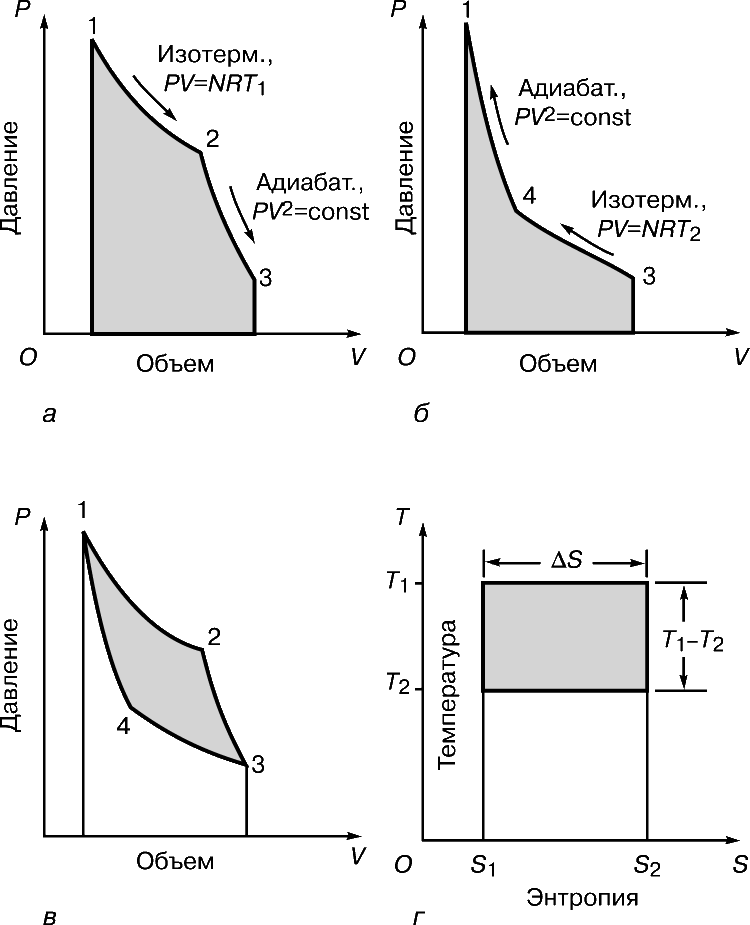
Мерой полезной работы, совершенной машиной, является разность площадей (рис. 3,а и б), показанная на рис. 3,в. Нетрудно сообразить, что при заданном изменении объема эту разность площадей можно увеличить либо повысив T1, либо понизив T2. Если же температура T1 фиксирована (а это значит, что фиксировано полное количество подводимой теплоты), то работу, производимую машиной, можно увеличить, только понизив T2. С особой наглядностью это показывает «диаграмма Молье» (график зависимости температура – энтропия), представленная на рис. 3,г. Здесь тоже полезная работа пропорциональна выделенной площади; подводимая теплота определяется площадью T1DS, а часть ее, соответствующая площади прямоугольника T2DS, «бесполезна» в смысле совершения работы. Таким образом, какова бы ни была температура T1, отличная от абсолютного нуля, какая-то часть подводимой теплоты не может быть превращена в работу.
На изложенных соображениях основан вывод формулы Карно, которая дает максимально возможный КПД идеальной тепловой машины, работающей при заданной разности температур нагревателя и холодильника:

Реальная машина не может работать с таким КПД, поскольку в ней неизбежны трение и утечки тепла. Для паровой машины, работающей, например, при температуре котла 130° C (403 К) и температуре конденсатора 30° C (303 К), термодинамический КПД равен 100/403, т.е. меньше 25%.