Основные понятия
Гомогенная реакция — реакция, в которой реагирующие вещества находятся в одной фазе.
Гетерогенная реакция — реакция, происходящая на границах раздела фаз – между газообразным веществом и раствором, между раствором и твёрдым веществом, между твёрдым и газообразным веществами.
Реакция называется простой, если продукт образуется в результате непосредственного взаимодействия молекул (частиц) реагентов.
Реакция называется сложной, если конечный продукт получается в результате осуществления двух и более простых реакций (элементарных актов) с образованием промежуточных продуктов.
Порядок химической реакции

График зависимости концентрации реагента A в реакции A → B от времени для нулевого порядка реакции

График зависимости концентрации реагента A для первого порядка реакции
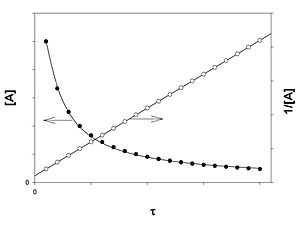
График зависимости концентрации реагента A для второго порядка реакции
Порядок реакции по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции.
Реакция нулевого порядка
Кинетическое уравнение имеет следующий вид:
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Нулевой порядок характерен, например, для гетерогенных реакций в том случае, если скорость диффузии реагентов к поверхности раздела фаз меньше скорости их химического превращения.
Реакция первого порядка
Кинетическое уравнение реакции первого порядка:
Приведение уравнения к линейному виду даёт уравнение:
Константа скорости реакции вычисляется как тангенс угла наклона прямой к оси времени:
Период полупревращения:
Реакция второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
или
В первом случае скорость реакции определяется уравнением:
Линейная форма уравнения:
Константа скорости реакции равна тангенсу угла наклона прямой к оси времени:
Во втором случае выражение для константы скорости реакции будет выглядеть так:
Период полупревращения (для случая равных начальных концентраций!):
Поверхность соприкосновения реагирующих веществ
Скорость реакций, идущих на поверхности веществ, т. е. гетерогенных, зависит при прочих равных условиях от свойств этой поверхности. Известно, что растертый в порошок мел гораздо быстрее растворяется в соляной кислоте, чем равный по массе кусочек мела.
Увеличение скорости реакции объясняется в первую очередь увеличением поверхности соприкосновения исходных веществ, а также рядом других причин, например, нарушением структуры «правильной» кристаллической решетки. Это приводит к тому, что частицы на поверхности образующихся микрокристаллов значительно реакционноспособнее, чем те же частицы на «гладкой» поверхности.
В промышленности для проведения гетерогенных реакций используют «кипящий слой», чтобы увеличить поверхность соприкосновения реагирующих веществ, подвод исходных веществ и отвод продуктов. Например, при производстве серной кислоты с помощью «кипящего слоя» проводят обжиг колчедана.
Зависимость скорости реакции от концентрации реагентов.
Скорость большинства реакций со временем постепенно снижается. Этот результат хорошо согласуется с теорией столкновений: по мере протекания реакции концентрации исходных веществ падают, снижается и частота столкновений между ними; соответственно уменьшается и частота столкновения активных молекул. Это приводит к уменьшению скорости реакции. В этом состоит сущность одного из основных законов химической кинетики: скорость химической реакции пропорциональна концентрации реагирующих молекул. Математически это можно записать в виде формулы v = k, где k – постоянная, называемая константой скорости реакции. Приведенное уравнение называется уравнением скорости химической реакции или кинетическим уравнением. Константа скорости для данной реакции не зависит от концентрации реагентов и от времени, но она зависит от температуры в соответствии с уравнением Аррениуса: k = ke–Ea/RT.
Простейшее уравнение скорости v = k всегда справедливо в том случае, когда молекулы (или другие частицы, например, ионы) А, сталкиваясь с молекулами В, могут непосредственно превращаться в продукты реакции. Подобные реакции, идущие в один прием (как говорят химики, в одну стадию), называются элементарными реакциями. Таких реакций немного. Большинство реакций (даже таких с виду таких простых как H2 + I2 2HI) не являются элементарными, поэтому исходя из стехиометрического уравнения такой реакции записать его кинетическое уравнение нельзя.
Кинетическое уравнение можно получить двумя способами: экспериментально – измеряя зависимость скорости реакции от концентрации каждого реагента по отдельности, и теоретически – если известен детальный механизм реакции. Чаще всего (но не всегда) кинетическое уравнение имеет вид v = kxy, где x и y называются порядками реакции по реагентам А и В. Эти порядки, в общем случае, могут быть целыми и дробными, положительными и даже отрицательными. Например, кинетическое уравнение для реакции термического распада ацетальдегида CH3CHO CH4 + CO имеет вид v = k[CH3CHO]1,5, т.е. реакция имеет полуторный порядок. Иногда возможно случайное совпадение стехиометрических коэффициентов и порядков реакции. Так, эксперимент показывает, что реакция H2 + I2 2HI имеет первый порядок как по водороду, так и по иоду, то есть ее кинетическое уравнение имеет вид v = k[H2][I2] (именно поэтому эту реакцию в течение многих десятилетий считали элементарной, пока в 1967 не был доказан ее более сложный механизм).
Если известно кинетическое уравнение, т.е. известно, как скорость реакции зависит от концентраций реагентов в каждый момент времени, и известна константа скорости, то можно рассчитать зависимость от времени концентраций реагентов и продуктов реакции, т.е. теоретически получить все кинетические кривые. Для таких расчетов используются методы высшей математики или компьютерные расчеты, и они не представляют принципиальных трудностей.
С другой стороны, полученное экспериментально кинетическое уравнение помогает судить о механизме реакции, т.е. о совокупности простых (элементарных) реакций. Выяснение механизмов реакций является важнейшей задачей химической кинетики. Это очень трудная задача, так как механизм даже простой с виду реакции может включать множество элементарных стадий.
Можно проиллюстрировать применение кинетических методов для определения механизма реакции на примере щелочного гидролиза алкилгалогенидов с образованием спиртов: RX + OH– → ROH + X–. Экспериментально было обнаружено, что для R = CH3, C2H5 и т.д. и X = Cl скорость реакции прямо пропорционально концентрациям реагентов, т.е. имеет первый порядок по галогениду RX и первый – по щелочи, и кинетическое уравнение имеет вид v = k1. В случае третичных алкилиодидов (R = (CH3)3C, X = I) порядок по RX – первый, а по щелочи – нулевой: v = k2. В промежуточных случаях, например, для изопропилбромида (R = (CH3)2CH, X = Br), реакция описывается более сложным кинетическим уравнением: v = k1 + k2. На основании этих кинетических данных был сделан следующий вывод о механизмах подобных реакций.
В первом случае реакция идет в один прием, путем непосредственного столкновения молекул спирта с ионами ОН– (так называемый механизм SN2). Во втором случае реакция идет в две стадии. Первая стадия – медленная диссоциация алкилиодида на два иона: RI → R+ + I–. Вторая – очень быстрая реакция между ионами: R+ + OH– → ROH. Скорость суммарной реакции зависит только от медленной (лимитирующей) стадии, поэтому она не зависит от концентрации щелочи; отсюда – нулевой порядок по щелочи (механизм SN1). В случае вторичных алкилбромидов осуществляются одновременно оба механизма, поэтому кинетическое уравнение более сложное.
Илья Леенсон
Скорость химической реакции
Дадим определение основному понятию химической кинетики – скорости химической реакции:
Скорость химической реакции есть число элементарных актов химической реакции, происходящих в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности (для гетерогенных реакций).
Скорость химической реакции есть изменение концентрации реагирующих веществ в единицу времени.
Первое определение является наиболее строгим; из него следует, что скорость химической реакции можно также выражать как изменение во времени любого параметра состояния системы, зависящего от числа частиц какого-либо реагирующего вещества, отнесенное к единице объема или поверхности – электропроводности, оптической плотности, диэлектрической проницаемости и т.д. и т.п. Однако наиболее часто в химии рассматривается зависимость концентрации реагентов от времени. В случае односторонних (необратимых) химических реакций (здесь и далее рассматриваются только односторонние реакции) очевидно, что концентрации исходных веществ во времени постоянно уменьшаются (ΔСисх < 0), а концентрации продуктов реакции увеличиваются (ΔСпрод > 0). Скорость реакции считается положительной, поэтому математически определение средней скорости реакции в интервале времени Δt записывается следующим образом:
В различных интервалах времени средняя скорость химической реакции имеет разные значения; истинная (мгновенная) скорость реакции определяется как производная от концентрации по времени:
Графическое изображение зависимости концентрации реагентов от времени есть кинетическая кривая (рисунок 2.1).
Рис. 2.1 Кинетические кривые для исходных веществ (А) и продуктов реакции (В).
Истинную скорость реакции можно определить графически, проведя касательную к кинетической кривой (рис. 2.2); истинная скорость реакции в данный момент времени равна по абсолютной величине тангенсу угла наклона касательной:
Рис. 2.2 Графическое определение Vист.
Необходимо отметить, что в том случае, если стехиометрические коэффициенты в уравнении химической реакции неодинаковы, величина скорости реакции будет зависеть от того, изменение концентрации какого реагента определялось. Очевидно, что в реакции
концентрации водорода, кислорода и воды изменяются в различной степени:
ΔС(Н2) = ΔС(Н2О) = 2 ΔС(О2).
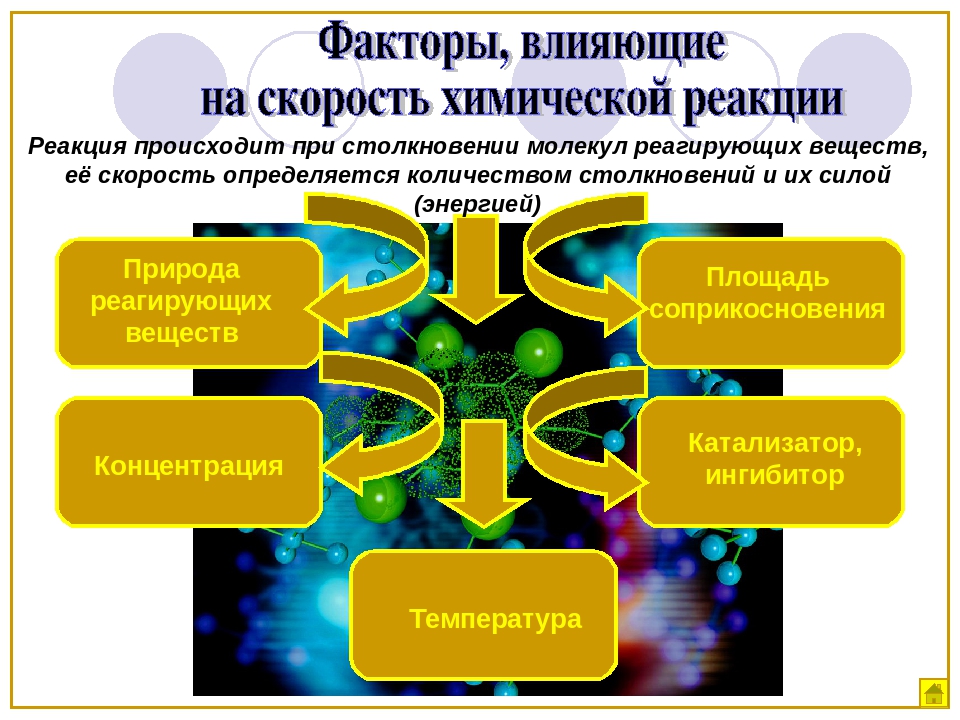
Скорость химической реакции зависит от множества факторов: природы реагирующих веществ, их концентрации, температуры, природы растворителя и т.д.
Одной из задач, стоящих перед химической кинетикой, является определение состава реакционной смеси (т.е. концентраций всех реагентов) в любой момент времени, для чего необходимо знать зависимость скорости реакции от концентраций. В общем случае, чем больше концентрации реагирующих веществ, тем больше скорость химической реакции. В основе химической кинетики лежит т. н. основной постулат химической кинетики
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях.
Т. е. для реакции
Коэффициент пропорциональности k есть константа скорости химической реакции. Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ, равных 1 моль/л.
Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется кинетическим уравнением химической реакции. Очевидно, что для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции (в уравнении (II.4) соответственно x, y и z) есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (x + y + z) представляет собой общий порядок реакции. Следует подчеркнуть, что порядок реакции определяется только из экспериментальных данных и не связан со стехиометрическими коэффициентами при реагентах в уравнении реакции. Стехиометрическое уравнение реакции представляет собой уравнение материального баланса и никоим образом не может определять характера протекания этой реакции во времени.
В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ от времени для необратимых (односторонних) реакций нулевого, первого и второго порядков.
Экспериментальные методы химической кинетики
Экспериментальные методы химической кинетики подразделяются на химические, физические, биохимические в зависимости от способа измерения количества вещества или его концентрации в ходе реакции.
К химическим относятся методы кинетики, основанные на традиционных способах количественного химического анализа — титриметрических, гравиметрических и др.
В современной экспериментальной кинетике к числу наиболее широко применяемых физических методов относятся различные спектральные методы. Эти методы основаны на измерениях, как правило спектров поглощения реагентов или продуктов в ультрафиолетовой, видимой и инфракрасной областях. Широко используют также спектры электронного парамагнитного резонанса (ЭПР) и ядерного магнитного резонанса (ЯМР).
Природа реагирующих веществ (их состав, строение)
Значение энергии активацииявляется тем фактором, посредством которого сказывается влияние природы реагирующих веществ на скорость реакции.
Если энергия активации мала (< 40 кДж/моль), то это означает, что значительная часть столкновений между частицами реагирующих веществ приводит к их взаимодействию, и скорость такой реакции очень большая. Все реакции ионного обмена протекают практически мгновенно, ибо в этих реакциях участвуют разноименно заряженные ионы, и энергия активации в данных случаях ничтожно мала.
Если энергия активации велика (> 120 кДж/моль), то это означает, что лишь ничтожная часть столкновений между взаимодействующими частицами приводит к реакции. Скорость такой реакции поэтому очень мала. Например, протекание реакции синтеза аммиака при обычной температуре заметить практически невозможно.
Если энергии активации химических реакций имеют промежуточные значения (40120 кДж/моль), то скорости таких реакций будут средними. К таким реакциям можно отнести взаимодействие натрия с водой или этиловым спиртом, обесцвечивание бромной воды этиленом, взаимодействие цинка с соляной кислотой и др.
Эндотермические и экзотермические реакции
Реакция метана с кислородом воздуха, как известно, сопровождается выделением большого количества тепла. Поэтому ее используют в быту для приготовления пищи, нагревания воды и отопления. Природный газ, поступающий в дома по трубам, на 98% состоит именно из метана. Реакция оксида кальция (СаО) с водой тоже сопровождается выделением большого количества тепла.
О чем могут говорить эти факты? При образовании новых химических связей в продуктах реакции выделяется большеэнергии, чем требуется на разрыв химических связей в реагентах. Избыток энергии выделяется в виде тепла, а иногда и света.
СН4 + 2О2 = СО2 + 2Н2О + Q (энергия (свет, тепло));
СаО + Н2О = Са(ОН)2 + Q (энергия (тепло)).
Такие реакции должны протекать легко (как легко катится под гору камень).
Реакции, в которых энергия выделяется, называются ЭКЗОТЕРМИЧЕСКИМИ(от латинского «экзо» – наружу).
Например, многие окислительно-восстановительные реакции являются экзотермическими. Одна из таких красивых реакций — внутримолекулярное окисление-восстановление, протекающее внутри одной и той же соли — дихромата аммония (NH4)2Cr2O7:
(NH4)2Cr2O7 = N2 + Cr2O3 + 4 H2O + Q (энергия).
Другое дело – обратные реакции. Они аналогичны закатыванию камня в гору. Получить метан из CO2 и воды до сих пор не удается, а для получения негашеной извести СаО из гидроксида кальция Са(ОН)2 требуются сильное нагревание. Такая реакция идет только при постоянном притоке энергии извне:
Са(ОН)2 = СаО + Н2О — Q (энергия (тепло))
Это говорит о том, что разрыв химических связей в Ca(OH)2 требует большей энергии, чем может выделиться при образовании новых химических связей в молекулах CaO и H2O.
Реакции, в которых энергия поглощается, называются ЭНДОТЕРМИЧЕСКИМИ(от «эндо» – внутрь).
Примеры реакций с различной скоростью
Взаимодействия химических веществ могут осуществляться с различной скоростью. Так, скорость нарастания сталактитов, то есть образования карбоната кальция, составляет всего 0,5 мм за 100 лет. Медленно идут некоторые биохимические реакции, например, фотосинтез и синтез белка. С довольно низкой скоростью протекает коррозия металлов.
Средней скоростью можно охарактеризовать реакции, требующие от одного до нескольких часов. Примером может послужить приготовление пищи, сопровождающееся разложением и превращением соединений, содержащихся в продуктах. Синтез отдельных полимеров требует нагревания реакционной смеси в течение определенного времени.
Примером химических реакций, скорость которых довольно высока, могут послужить реакции нейтрализации, взаимодействие гидрокарбоната натрия с раствором уксусной кислоты, сопровождающееся выделением углекислого газа. Также можно упомянуть взаимодействие нитрата бария с сульфатом натрия, при котором наблюдается выделение осадка нерастворимого сульфата бария.
Большое число реакций способно протекать молниеносно и сопровождаются взрывом. Классический пример – взаимодействие калия с водой.

Лимитирующая стадия реакции.
Если реакция осуществляется путем последовательно протекающих стадий (не обязательно все из них являются химическими) и одна из этих стадий требует значительно большего времени, чем остальные, то есть идет намного медленнее, то такая стадия называется лимитирующей. Именно эта самая медленная стадия определяет скорость всего процесса. Рассмотрим в качестве примера каталитическую реакцию окисления аммиака. Здесь возможны два предельных случая.
1. Поступление молекул реагентов – аммиака и кислорода к поверхности катализатора (физический процесс) происходит значительно медленнее, чем сама каталитическая реакция на поверхности. Тогда для повышения скорости образования целевого продукта – оксида азота совершенно бесполезно повышать эффективность катализатора, а надо позаботиться об ускорении доступа реагентов к поверхности.
2. Подача реагентов к поверхности происходит значительно быстрее самой химической реакции. Вот здесь имеет смысл совершенствовать катализатор, подбирать оптимальные условия для каталитической реакции, так как лимитирующей стадией в данном случае является каталитическая реакция на поверхности.