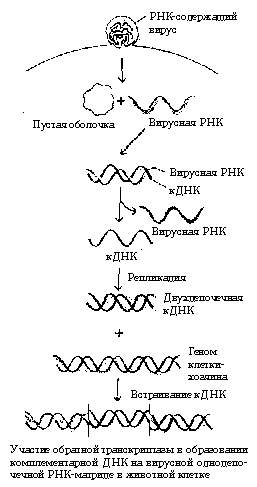
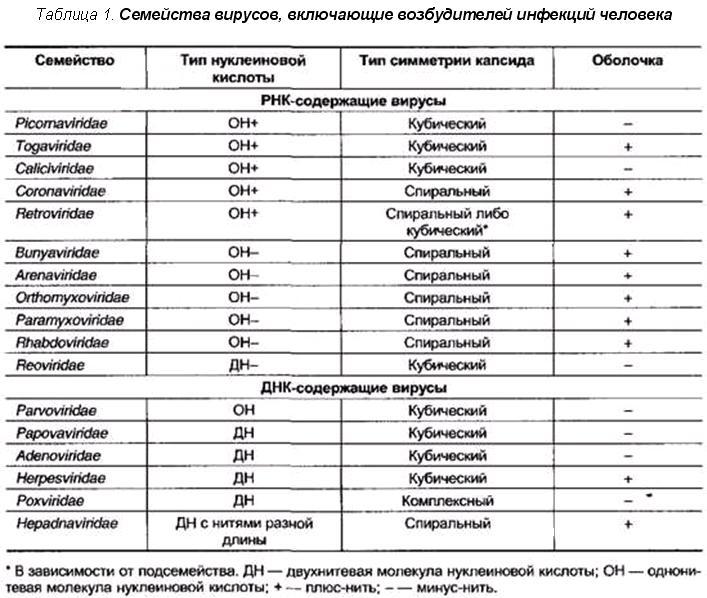
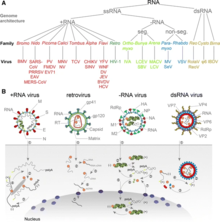
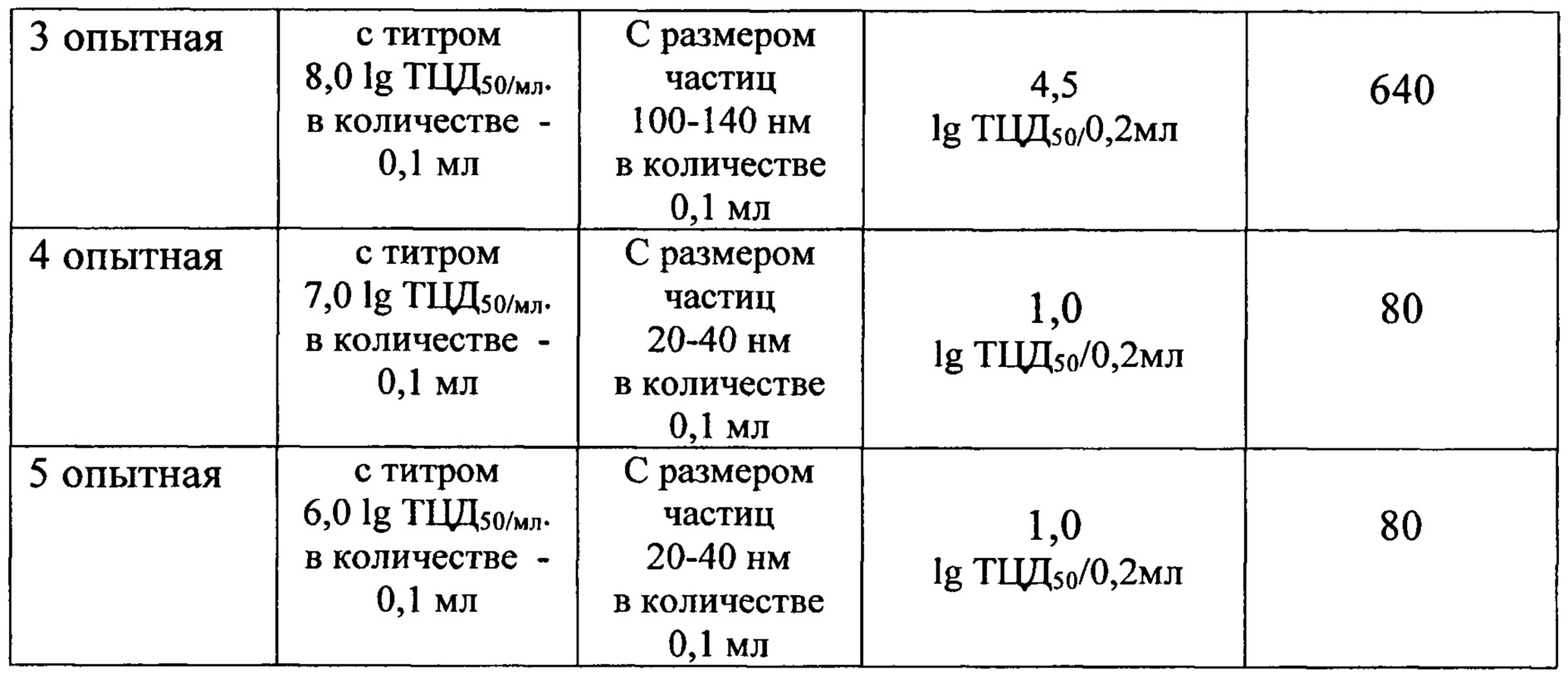
Характеристики
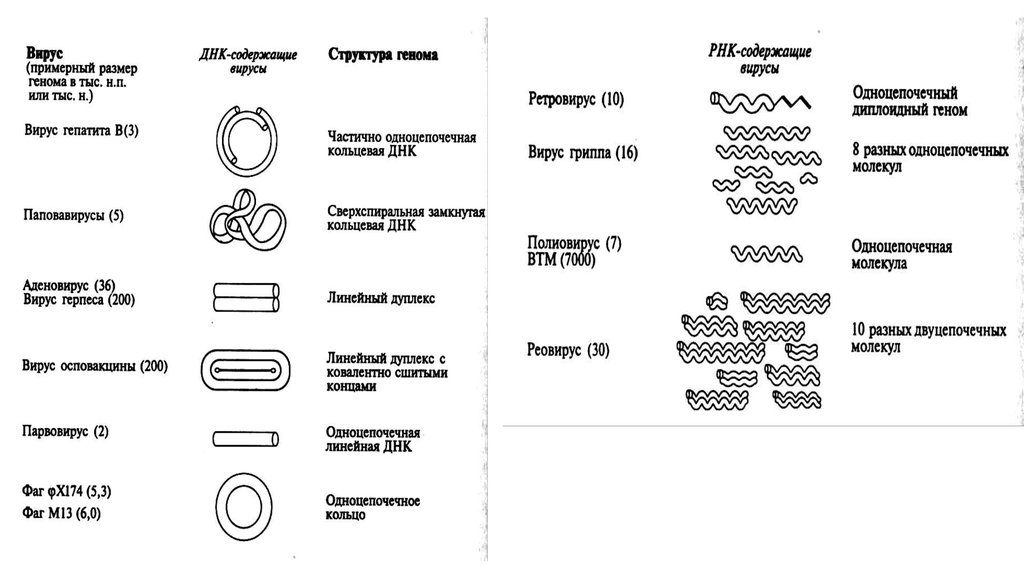
Одноцепочечные РНК-вирусы и смысловая РНК
РНК-вирусы могут быть дополнительно классифицированы в соответствии с полярностью их РНК на и , или РНК . Вирусы, содержащие одноцепочечную (+)РНК похожую на мРНК и таким образом может непосредственно транслирована зараженной клеткой. Поэтому (+)РНК также называется смысловой. Антисмысловая (-)РНК вируса комплиментарна мРНК и таким образом может быть превращена в (+)РНК действием РНК-зависимой РНК-полимеразой перед трансляцией. Очищенная РНК (+)РНК-содержащих вирусов сама по себе может напрямую вызывать инфекцию, хотя её инфекционность ниже, чем у полноценных вирусных частиц. Очищенная РНК (-)РНК-содержащих вирусов неинфекционна сама по себе, так как она должна транскрибироваться в (+)РНК; каждый вирион после транскрипции может быть источником нескольких смысловых цепей (+)РНК. Двухцепочечные(±)РНК вирусы напоминают (-)РНК-содержащие вирусы тем, что они также транслируют гены с отрицательной (некодирующей) цепи РНК.
Двуцепочечные РНК вирусы
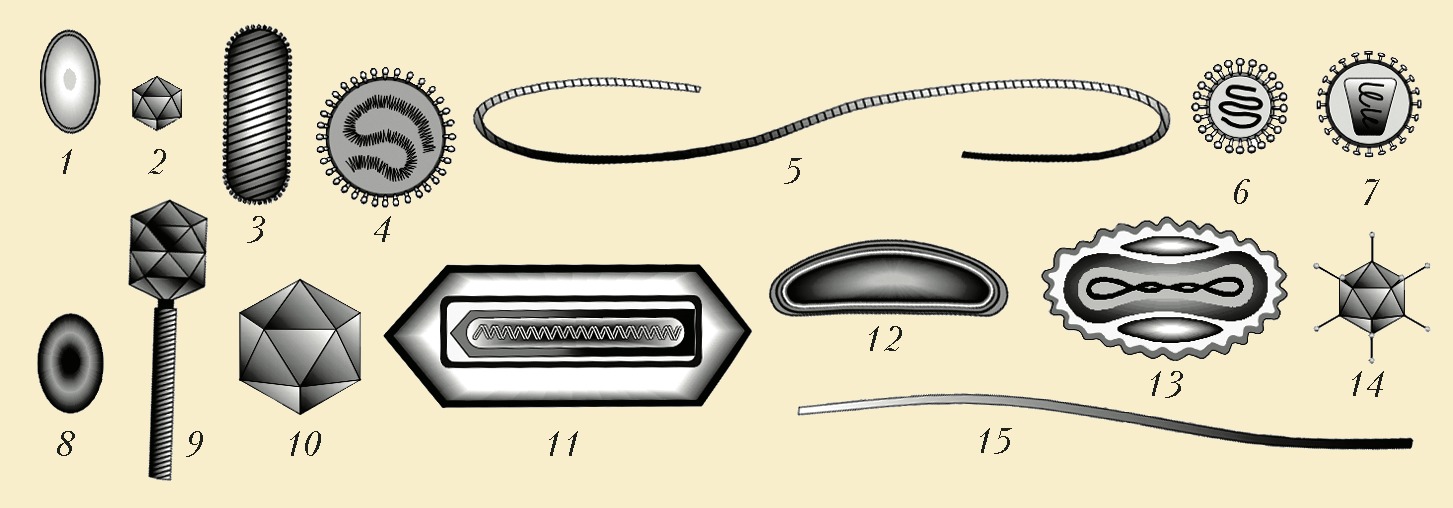
Структура вириона реовируса
Двуцепочечные РНК вирусы представляет разнообразную группу вирусов отличающихся по заражаемому кругу хозяев (людей, животных, растений, грибов, и бактерий), числу фрагментов генома (от 1 до 12 сегментов), и организацией вириона (формой капсида, количеством слоев капсида, выросты, шипы, и т. п.). Члены этой группы включают ротавирусы, всемирно известные как наиболее распространённая причина детских гастроэнтеритов, и пикорнавирусы, известный во всём мире как наиболее часто встречающийся вирус в фекалиях людей и животных с признаками диареи или без них. является экономически важным возбудителем болезни коз и овец. В прошлые годы, достигнут большой прогресс в определении атомной и субнанометровой структуры ряда ключевых вирусных белков и капсидов вирионов нескольких дцРНК-вирусов, подчёркивая существенные параллели в структуре и механизмах процессов репликации многих из этих вирусов.
Частота мутаций
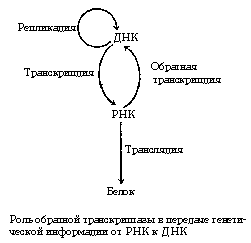
РНК вирусы имеют очень высокую частоту мутаций по-сравнению с ДНК-вирусами, потому что вирусная РНК-зависимая РНК-полимераза не имеет способности (3′-5′-экзонуклеазной гидролитической активности) к коррекции ошибок, как ДНК-полимеразы. Это одна из причин того, почему так трудно сделать эффективную вакцину для предотвращения болезней, вызываемых РНК-вирусами.
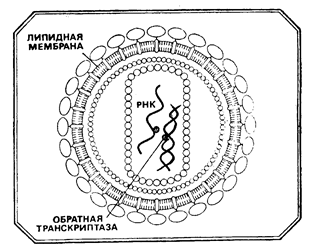
Ретровирусы также имеют высокую частоту мутаций, даже несмотря на то, что их промежуточная форма генома в виде ДНК интегрируется в геном хозяина (и, следовательно, после интеграции в геном, во время репликации, подвергается корректирующей проверке ДНК-полимеразой хозяина). Высокая частота мутаций обусловлена высокой частотой ошибок во время обратной транскрипции, до стадии интеграции в геном хозяина. Ошибки при этом встраиваются в обе цепи ДНК.
Некоторые гены РНК-вирусов важны для их репликации и мутации в них не допустимы. Например, участок генома вируса гепатита С кодирующий коровый белок, высоко консервативен, потому что он содержит структурную РНК, вовлеченную в образование участка внутренней посадки рибосомы.
Профилактика
Профилактика коронавируса 2019-nCoV (SARS-CoV-2), рекомендованная Всемирной Организацией Здравоохранения (ВОЗ) включает в себя:
Обратите внимание на то, что использование обычных бумажных масок не гарантирует безопасность от коронавирусных инфекций, поскольку они способны перемещаться в воздухе и проникать в дыхательные пути через щели, между маской и кожей. Прививка от SARS-CoV-2 по состоянию на 13.03.2020 г находится в стадии доклинических испытаний, и как заявляет ВОЗ, в свет она выйдет не ранее лета 2021 года
Но, несмотря на этот, многие мошенники уже на различных досках объявлений торгуют вымышленным лекарством – будьте бдительны!
Прививка от SARS-CoV-2 по состоянию на 13.03.2020 г находится в стадии доклинических испытаний, и как заявляет ВОЗ, в свет она выйдет не ранее лета 2021 года. Но, несмотря на этот, многие мошенники уже на различных досках объявлений торгуют вымышленным лекарством – будьте бдительны!
Группа IV — оц(+)РНК-вирусы
Основная статья: Одноцепочечные РНК-вирусы с позитивной цепью
В этой группе есть три порядка и 34 семейства. Кроме того, существует ряд неклассифицированных и родов.
- Порядок Nidovirales
- Семейство Arteriviridae
- Семейство Coronaviridae — включает Coronavirus, SARS, MERS
- Семейство Mesoniviridae
- Семейство Roniviridae
- Порядок Picornavirales
- Семейство Dicistroviridae
- Семейство Iflaviridae
- Семейство Marnaviridae
- Семейство Picornaviridae — включает Poliovirus, Rhinovirus (общая простуда), вирус гепатита А
- Семейство Secoviridae включает подсемейство Comovirinae
- Род Bacillariornavirus
- Род Dicipivirus
- Род Labyrnavirus
- Род Sequiviridae
- Вид Kelp fly virus
- Порядок Tymovirales
- Семейство Alphaflexiviridae
- Семейство Betaflexiviridae
- Семейство Gammaflexiviridae
- Семейство Tymoviridae
- Неклассифицированные
- Семейство Alphatetraviridae
- Семейство Alvernaviridae
- Семейство Astroviridae
- Семейство Barnaviridae
- Семейство Benyviridae
- Семейство Bromoviridae
- Семейство Caliciviridae — включает Norovirus
- Семейство Carmotetraviridae
- Семейство Closteroviridae
- Семейство Flaviviridae — включает вирус жёлтой лихорадки, вирус лихорадки Западного Нила, вирус гепатита С, вирус лихорадки денге, вирус Зика
- Семейство Fusariviridae
- Семейство Hepeviridae
- Семейство Hypoviridae
- Семейство Leviviridae
- Семейство Luteoviridae — включает Barley yellow dwarf virus
- Семейство Polycipiviridae
- Семейство Narnaviridae
- Семейство Nodaviridae
- Семейство Permutotetraviridae
- Семейство Potyviridae
- Семейство Sarthroviridae
- Семейство Statovirus
- Семейство Togaviridae — включает вирус краснухи, Ross River virus, Sindbis virus, Вирус Чикунгунья
- Семейство Tombusviridae
- Семейство Virgaviridae
- Неклассифицированные роды
- Род Blunervirus
- Род Cilevirus
- Род Higrevirus
- Род Idaeovirus
- Род Negevirus
- Род Ourmiavirus
- Род Polemovirus
- Род Sinaivirus
- Род Sobemovirus
- Неклассифицированные виды
- Acyrthosiphon pisum virus
- Bastrovirus
- Blackford virus
- Blueberry necrotic ring blotch virus
- Cadicistrovirus
- Chara australis virus
- Extra small virus
- Goji berry chlorosis virus
- Hepelivirus
- Jingmen tick virus
- Le Blanc virus
- Nedicistrovirus
- Nesidiocoris tenuis virus 1
- Niflavirus
- Nylanderia fulva virus 1
- Orsay virus
- Osedax japonicus RNA virus 1
- Picalivirus
- Plasmopara halstedii virus
- Rosellinia necatrix fusarivirus 1
- Santeuil virus
- Secalivirus
- Solenopsis invicta virus 3
- Wuhan large pig roundworm virus
Вирусы-сателлиты
- Семейство Sarthroviridae
- Род Albetovirus
- Род Aumaivirus
- Род Papanivirus
- Род Virtovirus
- Chronic bee paralysis virus
Также был описан неклассифицированный астровирусный / гепевирусоподобный вирус.
Мы построили им рай
Пожалуй, главное оружие вирусов — это способность чрезвычайно быстро меняться. В частности, у ВИЧ это свойство обусловлено тем, что фермент обратная транскриптаза делает ошибки при копировании вируса в организме. Как будто полиция ищет преступника по фотороботу и отпечаткам, а он каждый день меняет свой облик. У других вирусов есть свои механизмы изменчивости. Благодаря им, к примеру, вирус Эбола за двадцать лет с момента открытия изменился на целую четверть.

Наш эксперт Евгений Комаровский, врач-педиатр, инфекционист, телеведущий: «Главная сложность лечения вирусных инфекций состоит в том, что некий лекарственный препарат должен проникнуть внутрь клетки человеческого организма и уничтожить вирус, не повредив при этом саму клетку и ее соседей. Поэтому действие противовирусных препаратов, как правило, направлено на замедление размножения вируса и активизацию собственного иммунитета. Лучшая стратегия противодействия вирусам — профилактика. 1. Прививки. Введение в организм ослабленного вируса приводит к выработке вполне полноценных антител, защищающих человека от конкретной вирусной инфекции (кори, краснухи, полиомиелита, гепатита В, гриппа, клещевого энцефалита и проч.). 2. Предотвращение или ограничение контактов с вероятным источником инфекции (отдельная комната для больного острой респираторной инфекцией и маски для его родственников, «разборчивая» половая жизнь для предотвращения СПИДа и т. д.). 3. Образ жизни и система воспитания, формирующие нормальный иммунитет».
Сегодня не только ВИЧ представляет опасность для человечества. Мало кто знает о мировой эпидемии, вызванной вирусом гепатита С. Он был открыт в 1989 году, и сейчас по всему миру насчитывается 150 млн человек — его носителей. И 400 000 человек ежегодно умирает от вызванных им осложнений. Атипичная пневмония, лихорадка Эбола, «птичий» грипп, коронавирус MERS и другие, неизвестные пока инфекции при определенных обстоятельствах могут вызвать эпидемии с большими человеческими жертвами. Природный резервуар «запчастей» для вирусов огромен, и они могут складываться в опасные формы.
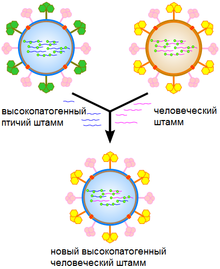
Этот процесс называется рекомбинацией вирусов — вирусы обмениваются своими генами друг с другом, создавая новые виды. Такая рекомбинация может происходить как между разными ДНК, так и разными РНК. Причем участвует в обмене генетический материал не только вирусов, но и их носителей — к примеру, может соединяться вирус животного и человека. Именно так появляются новые опасные формы вирусов.

Но почему именно сегодня новые вирусы появляются все чаще? Профессор Института молекулярной биологии и генетики, академик Виталий Кордюм называет несколько основных причин, главные из них — сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и возможность быстрого перемещения носителей вируса. Благодаря научному и техническому прогрессу носитель опасной инфекции за несколько суток может добраться с одного континента на другой. Этот же прогресс стал причиной того, что последние 70 лет происходит односторонняя миграция населения из сел и малых городов в крупные города, что привело к возникновению компактных многомиллионных поселений.
Очевидно, что наш современный «урбанистический» образ жизни играет в процессах стремительной эволюции вирусов не последнюю роль. Человек, устраивая свою жизнь с комфортом и переделывая все вокруг на свой вкус, вдруг забыл, что он обычный биологический вид, и перестал жить по законам природы. А вирусы напоминают нам об этом.
Статья «Золотой век вирусов» опубликована в журнале «Популярная механика»
(№9, Сентябрь 2015).
Вирус гепатита С, определение РНК
Гепатит С – заболевание печени, которое вызывается вирусом гепатита С (Hepatit C Virus). Источниками вируса являются больные всеми формами острого и хронического гепатита С, а также вирусоносители. Около 80% заболевших острым гепатитом С болеют лица в возрасте 15-29 лет.
Заразиться можно при инъекциях, абортах, прививках, стоматологических процедурах и т. д. Группы повышенного риска инфицирования: больные, получающие лечение хроническим гемодиализом, больные гемофилией, наркоманией. К группе повышенного риска инфицирования относят и медицинских работников, имеющих контакт с кровью (например, сотрудники отделений гемодиализа).
Передача вируса может случиться при родах, менструации, сексуальном контакте, повреждении кожи и слизистых в быту и на производстве.
Начало заболевания гепатитом С постепенное. В продромальном периоде основными симптомами могут быть: слабость, анорексия, тошнота, рвота и др. Так же, как и при гепатите В, могут быть зарегистрированы боли в суставах (15—20%). Это значительно осложняет диагностику. Продромальный период — период заболевания, который протекает между бессимптомным периодом и собственно болезнью.
Часто заболевание переходит в хроническую стадию и обнаруживается в случае профилактических анализов. Хроническое течение болезни приводит к циррозу печени и гепатоцеллюлярной карциноме (рак печени).
Страдает не только печень, появляются смешанная криоглобулинемия и другие ревматические заболевания.
Возможно три варианта завершения острого гепатита С:
Выздоровление. У 20% пациентов происходит нормализация показателей работы печени АЛТ, АСТ в течении 6—12 месяцев и исчезает РНК ВГС. В случае выздоровления антитела класса IgM обычно исчезают в течение первых двух месяцев. Антитела класса IgG остаются четыре-восемь лет.
Носительство ВГС. У 20—30% нормализуется уровень АЛТ, АСТ с наличием антител ВГС.
Развитие хронического гепатита. Он регистрируется у 60— 70% переболевших острым гепатитом. Причем его развитие не зависит от тяжести течения острого заболевания. Переход острого гепатита С в хронический происходит постепенно. В течение нескольких лет нарастает активность патологического процесса и фиброза печени. Показатели активности АЛТ, АСТ в пределах нормы или незначительно повышены. Показатели общего белка и альбумина в пределах нормы, вплоть до развития цирроза печени. В этот период, продолжительность которого может быть 15-20 лет, пациенты, чаще всего, не считают себя больными.
Раннее обнаружение инфекции возможно с помощью анализа РНК вируса гепатита С в крови методом ПЦР.
Диагноз гепатита С ставит врач на основании данных лабораторных исследований, данных других диагностических исследований и клинической картины заболевания.
Выявить PHK HCV методом ПЦР можно уже через 10-12 дней после инфицирования. Это позволяет исключить или подтвердить инфицирование лиц, которые имели риск заболевания. Выявленный PHK HCV в крови подтверждается факт инфицирования, свидетельствует о размножении вируса в организме. В период, когда в крови определяется PHK HCV носитель вируса, может быть распространителем, поскольку вирус находится в активной фазе. По результатам лечения этот анализ позволяет установить гибель вируса.
Хронический вирусный гепатит С протекает с повышением печеночных ферментов, эти изменения отражают результаты таких анализов как АЛТ, АСТ, билирубин.
Анализ проводится для подтверждения результатов лечения в конце терапии, затем через 6 и 24 месяца наблюдения.
Обратите внимание, что сроки выполнения могут быть увеличены при проведении подтверждающих тестов.
Распространение 2019-nCoV (эпидемиология)
Дальше выяснилось, что несмотря на инкубационный период в 2-10 дней, инфицированный человек становится заразным для окружающих еще до появления первых признаков болезни. В связи с этим, в эпидемиологических целях г. Ухань и его округа были закрыты на карантин. Позже количество городов на карантине увеличилось.
30 января 2020 года ВОЗ признала новый коронавирус чрезвычайной ситуацией международного значения.
11 марта 2020 Всемирная Организация Здравоохранения назначила для COVID-19 статус — пандемия.
По состоянию на 5.02.2020: официально подтверждено 24584 инфицированных человека, из которых 493 умерло, а 727 выздоровело.
Наибольшее число зараженных выявлено в Китае – 23260 человек. Остальные инфицированные люди проживают в других 27 странах, преимущественно в Юго-Восточной Азии (Япония – 33, Таиланд – 25, Сингапур – 24, Гонконг – 21 и прочие).
По состоянию на 07.03.2020: уже подтверждено 1 363 123 случаев инфицирования, из которых 76 383 умерло, а 293 833 выздоровело. Лидером в антирейтинге являются США — 368174, далее Испания — 140510, Италия — 132547, Германия — 103717, Франция — 98010, .
На территории России на 07.04.2020 выявлено 7497 случаев заражения, в Украине – 1462.
Определение РНК гепатита С
Определение РНК вируса HCV-RNA, также именуемый ПЦР гепатита С, это исследование биологического материала (крови), с помощью которого можно определить в организме непосредственное наличие самого геноматериала вируса гепатита (любой отдельно взятый вирус является одной-единственной частичкой РНК).
Основной метод проведения теста — ПЦР, или метод полимеразно-цепной реакции.
Существуют два вида тестов крови на определение РНК HCV:
- качественный;
- количественный.
Качественный тест
Проведение качественного анализа дает возможность определить, находится ли вирус в составе крови. Все пациенты, у которых найдены антитела С-гепатита, должны пройти данный тест. По его результатам можно получить 2 ответа: «присутствует» либо «отсутствует» вирус. По положительному результату теста (обнаружено) можно судить об активном размножении вируса, который заражает здоровые клетки в печени.
Тест, проводимый на качественный ПЦР, настроен на конкретную чувствительность, от 10 до 500 МЕ/мл. Если обнаруженный в составе крови вирус гепатита при удельном содержании меньше 10 МЕ/мл, то обнаружение вируса может стать невозможным. Очень низкое значение удельного содержания вируса наблюдается среди пациентов, для которых назначена противовирусная терапия. Поэтому важным является тот факт, насколько высока чувствительность медицинской системы для диагностирования и постановки качественного результата при полимеразной цепной реакции.
Зачастую полимеразная цепная реакция C-гепатита проводится сразу же после нахождения соответствующих антител. Последующие тесты, при прохождении противовирусной терапии, проводятся на 4-ю, 12-ю и 24-ю недели. И еще один анализ после прекращения ПВТ делается через 24 недели. Затем — один раз в год.
Количественный тест
Количественный анализ ПЦР РНК, иногда называемый вирусной нагрузкой, определяет концентрацию (удельное содержание) вируса в составе крови. Другими словами, под вирусной нагрузкой понимается определенное количество вирусной РНК, которое может находиться в конкретном количестве крови (принято использовать 1 мл, равный 1 см в кубе).
Единицы измерения для результатов теста — международные (стандартные) единицы, разделенные на один миллилитр (МЕ/мл). Содержание вируса иногда представляется по-разному, это зависит от лабораторий, где проводятся исследования. Для гепатита С количественное определение иногда использует такие значения, как копии/мл.
Проверка «вирусной нагруженности» позволяет определить степень инфекционности заболевания. Так риск заразить вирусом другого человека повышается при повышении концентрации гепатита в составе крови. К тому же высокое содержание вируса снижает эффект от проводимого лечения. Поэтому малая вирусная нагрузка является очень благоприятным фактором для успешного лечения.
К тому же тест гепатита С и его определение методом ПЦР играют большую роль при применении терапии от болезни и определения успешности лечения. На основании результатов теста осуществляется планирование курса реабилитации. Например, при слишком медлительном уменьшении удельной концентрации вируса гепатита, противовирусная терапия продлевается, и наоборот.
В современной медицине считается, что нагрузка больше 800000 ME/мл является высокой. Нагрузка же сверх 10000000 ME/мл считается критической. Но у специалистов из разных стран и по сей день не появилось одинакового мнения о пределах вирусной нагрузки.
Частота проведения количественного теста
В общих случаях количественный анализ на гепатит HCV-RNA делается перед проведением противовирусной терапии и через 3 месяца по окончании лечебных процедур для определения качества проведенной терапии.
В качестве результата для количественного теста станет считаться количественная оценка результатов по образцу, указанному выше. В результате будет вынесен вердикт «ниже измеряемого диапазона» или «в крови не обнаружено» — это является нормой для здорового человека.
Параметр чувствительности качественного теста обычно ниже, чем чувствительность количественного анализа. Расшифровка «Отсутствующий» показывает, что оба вида анализов не нашли РНК вируса. При показателе теста «ниже измеренного диапазона» анализ количественного типа, скорее всего, не нашел РНК гепатита, хотя это подтверждает наличие вируса с очень маленьким удельным содержанием.
Как работает иммунитет?
Одновременно в организме реализуется еще один молекулярный защитный механизм: пораженные вирусом клетки начинают производить специальные белки, интерфероны, способные выходить из клетки и взаимодействовать с соседними клетками, снижая уровень белкового синтеза и препятствуя размножению вируса. Поражается как сам вирус, так и клетка-хозяин, зато распространение заразы блокируется.
Попутно интерфероны активируют ряд механизмов иммунной системы. Интерферон-альфа (ИФ-α) стимулирует синтез лейкоцитов, участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производит клетки соединительной ткани, фибробласты, и обладает тем же действием, что и ИФ-α, но с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) усиливает выработку Т-клеток, Т-хелперов и С08+Т-лимфоцитов, что придает ему свойство иммуномодулятора.
Проникновение вирусов в клетку-хозяина
Капсид в основном защищает нуклеиновую кислоту от действия клеточного нуклеазного фермента. Но некоторые белки капсида способствуют связыванию вируса с поверхностью клеток-хозяев, и работают, как ключики, вставляемые в нужные замочки. Другие поверхностные белки действуют как ферменты, они растворяют поверхностный слой клетки-хозяина и таким образом помогают проникновению нуклеиновой кислоты вируса в клетку-хозяина.
Вирусные популяции используют механизмы и метаболизм клетки-хозяина, чтобы произвести множество своих копий, которые собираются в клетке, пока не «выжмут из нее все соки», а затем выходят из погибшей клетки. Это наиболее частый сценарий, но не единственный.
Жизненный цикл вирусов сильно отличается у разных видов, но существует шесть основных этапов жизненного цикла вирусов:
- Прикрепление
- Проникновение
- Сброс капсида («раздевание»)
- Репликация
- Сборка
- Выход из клетки
Присоединение к клетке-хозяину представляет собой специфическое связывание между вирусными капсидными белками и рецепторами на клеточной поверхности. Эта специфика определяет хозяина вируса.
Проникновение следует за прикреплением: вирионы проникают в клетку-хозяина через рецептор-опосредованный эндоцитоз или слияние мембран. Это часто называют вирусной записью.
Проникновение вирусов в клетку достигается за счет:
- Образования пор
- Слияния мембран
- Ретракции пилуса
- Выброса
- Проницаемости
- Механизмов эндоцитоза
Мембраны растительных и грибковых клеток отличаются от мембран животных клеток. Растения имеют жесткую клеточную стенку из целлюлозы, а грибы – из хитина, поэтому большинство вирусов могут проникать внутрь этих клеток только после травмы («пробивания») клеточной стенки. Бактерии, как и растения, имеют прочные клеточные стенки, которые вирус должен разрушить, чтобы заразить клетку. Учитывая, что бактериальные клеточные стенки намного тоньше стенок растительных клеток из-за их гораздо меньшего размера, некоторые вирусы выработали механизмы ввода своего генома в бактериальную клетку через клеточную стенку, оставляя вирусный капсид снаружи. У прокариот происходит слияние мембран, образование пор через прокалывающее устройство.
Видео
Здоровья Вам, мира и добра!
Вирус представляет собой микроорганизм, намного меньший, чем грибки или бактерия. Вирус может заражать все формы жизни, включая бактерии и археи, вторгаясь в живую клетку для последующей репликации.
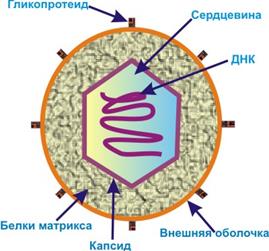
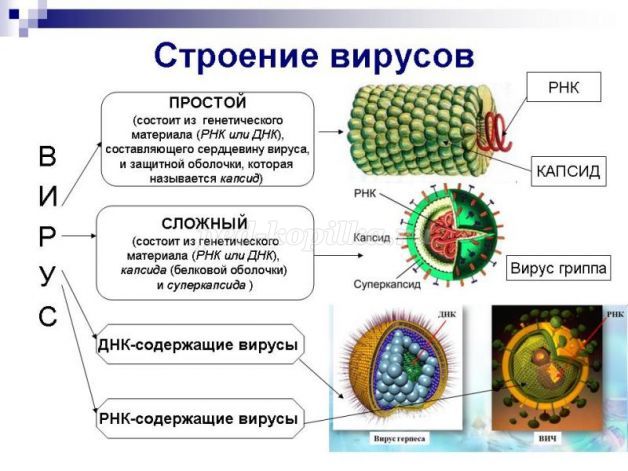
Частицы вируса (вирионы) не находятся в инфицированной клетке, они прикрепляются к клетке хоста (хозяина), входят в нее высвобождая свою ДНК или РНК. ДНК, РНК вируса – это генетический материал, содержащий информацию необходимую для копирования. Инфицированная клетка погибает, потому что вирус не позволяет ей выполнять свои обычные функции. При разрушении она выпускает новые вирионы, которые продолжают заражать другие клетки. Вирусные частицы состоят из двух или трех частей:
- Генетического материала, полученного из ДНК или РНК
- Длинных молекул несущих генетическую информацию
- Белкового покрытия — капсид
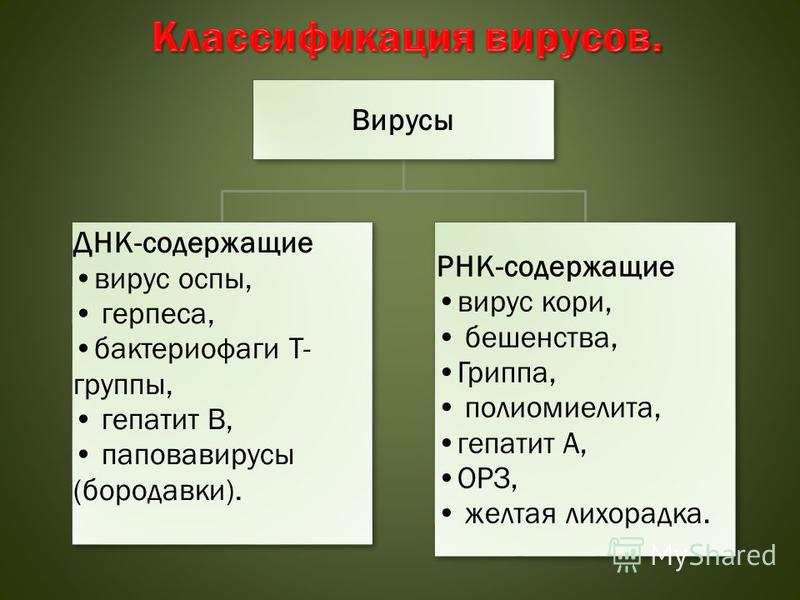
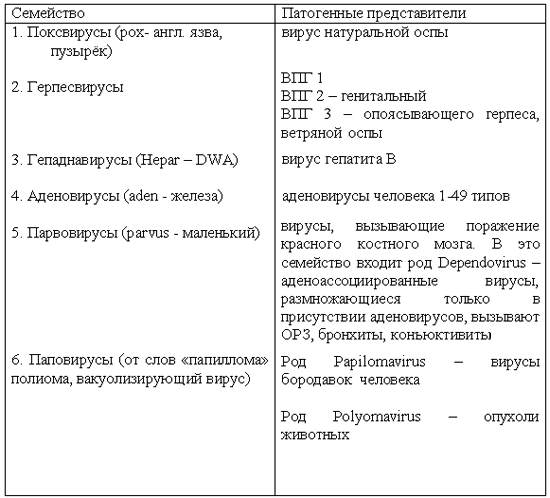
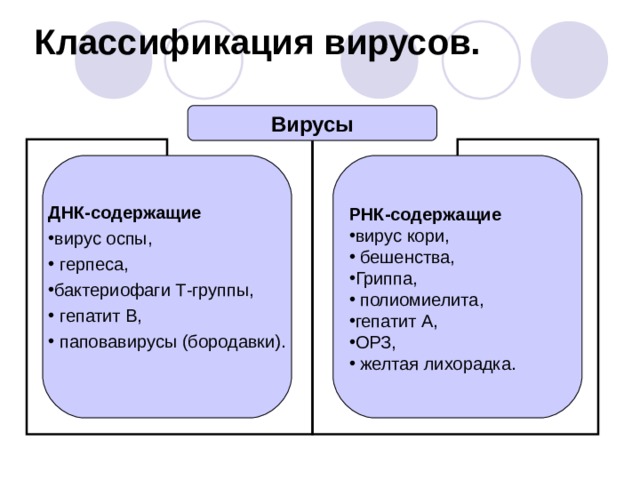
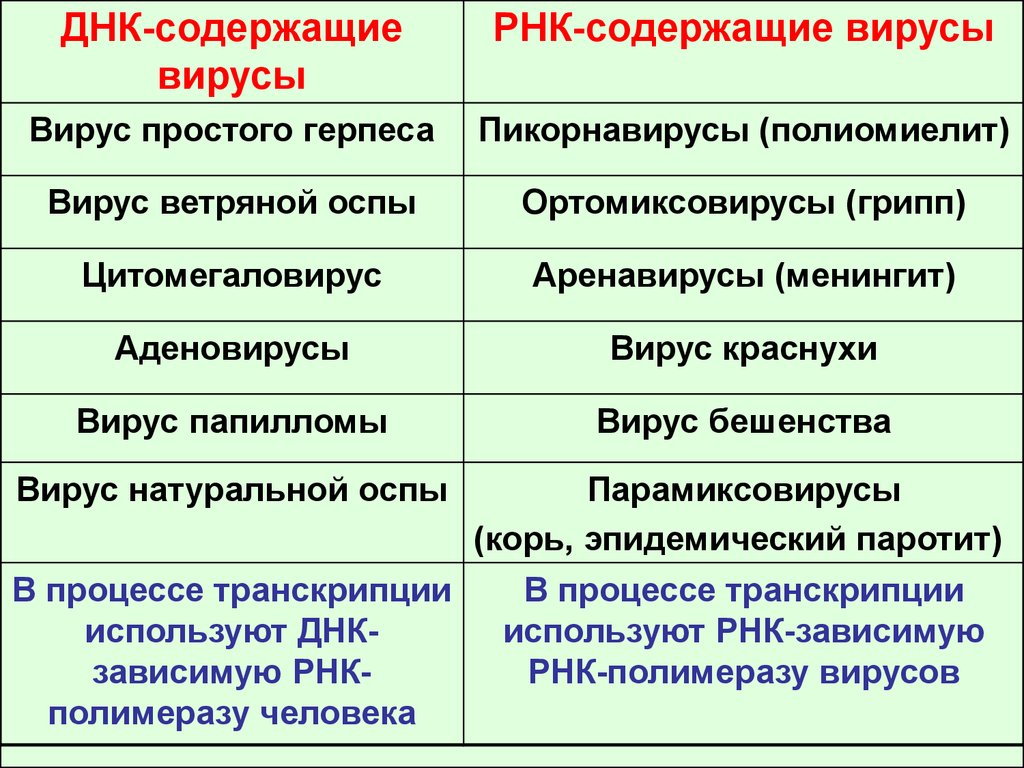
Вирусы классифицируются в зависимости от того, какую нуклеиновую кислоту используют для репликации:
- ДНК-вирусы – Репродуцируются в ядрах клеток, менее изменчивы и способны к длительной вегетации в организме хозяина. Вызывают такие заболевания как: кератит, энцефалит, герпес и др.
- РНК-вирусы – не имеют ДНК, репликация происходит в цитоплазме. Генетическая информация содержится в РНК и подвержена мутации. Включают в себя ретровирусы, такие как ВИЧ, корь, грипп, ротавирус, энтеровирус и др.
Вирионы не всегда убивают клетки, которые они заражают, а вместо этого изменяют их функции. Иногда инфицированная клетка теряет контроль над нормальным делением и становится злокачественной. Некоторые из вирусов, такие как вирусы герпеса, оставляют свой генетический материал в ядре-хозяине, где материал остается бездействующим в течение длительного времени (так называемая латентная инфекция). Когда клетка нарушена, вирионы снова начинают реплицировать, вызывая заболевание.
Вместо заключения: а могут ли вирусы приносить пользу?
Безусловно, да. Несмотря на то, что вирусы ассоциируются у большинства людей с однозначным вредом, они могут приносить и пользу — если речь идет о так называемых вирусных векторах и терапевтических подходах на их основе.
Исследователи давно научились помещать в белковую оболочку вируса интересующие их нуклеиновые кислоты, чтобы доставлять нужный ген в клетки, а также убирать те гены, которые делают вирус опасным для организма.
Это позволило сделать возможной генную терапию, помогающую бороться с заболеваниями, вызванными известными генетическими мутациями. Создание вирусных векторов — достаточно непростая задача, к тому же ограниченная свойствами самих вирусных частиц: количеством помещающейся генетической информации, местом ее вставки, стабильностью. Кроме того, вирусный вектор, используемый в медицине, не должен вызывать иммунного ответа или критично влиять на жизнедеятельность клетки. Тем не менее эти сложности решаются, поэтому уже одобрен ряд вполне успешных и безопасных генных терапий. А в качестве основы для вирусных векторов чаще всего используются ретро-, ленти-, адено- и аденоассоциированные вирусы.