Толерантность и синдром отмены
При постоянном уровне нитратов в организме коронарные артерии постепенно перестают на них реагировать, и эффект лекарств исчезает. Основной способ преодоления толерантности к нитратам – создание «безнитратного окна», то есть промежутка, когда в крови нет этого препарата. Например, обычные таблетки для этого назначают не 4 раза в день, а 2-3 раза. Важным способом профилактики толерантности является использование пролонгированных форм изосорбида-5-мононитрата.
В клинике часто используют «спорадическое» применение нитратов, когда их назначают перед планируемой физической нагрузкой.
Основной опасностью, связанной с прерывистым режимом приема, является синдром отмены. Он возникает при резком прекращении поступления нитратов. Например, после завершения внутривенного введения или отклеивания кожного пластыря возможно учащение и усиление приступов боли за грудиной.
Для профилактики синдрома отмены желательно использовать пролонгированные формы, прием которых можно назначать 1 раз в день.
Учитывая высокую эффективность этой группы лекарств, а с другой стороны – феномены привыкания и отмены, нитраты при ИБС назначают только тем больным, которые не могут без них обойтись.
Причины избегать нитраты
До сих пор ведутся споры о том, насколько опасны нитраты и нитриты для организма. Действительно необходимо избегать образования нитрозаминов. Но есть несколько причин, чтобы следить за этим и избегать нитратов и нитритов в обработанных пищевых продуктах и мясе.
1.Вред нитратов для организма человека — могут вызвать рак поджелудочной железы
Отмечалось выше, что нитрозамины действительно являются проблемой. Поскольку, когда они образуются в организме, они могут вызвать рак. Исследования показали, что может быть связь между нитратами, обнаруженными в консервированном мясе, и раком. Это имеет смысл, поскольку мы знаем, что рак связан с питанием.
Исследования были проведены, чтобы лучше понять связь между употреблением обработанных пищевых продуктов и раком поджелудочной железы. В исследованиях, опубликованных в журнале Национального института рака и Американских онкологических центров, выяснилось, что
«Самая сильная связь была с теми, кто ежедневно потребляет переработанное мясо. Эти субъекты имели повышенный риск от 50% до 68%. В то время как не было «связи риска рака поджелудочной железы с потреблением птицы, рыбы, молочных продуктов и яиц».
Гарвард недавно сообщил, что Всемирная Организация Здравоохранения заявляет
«Обработка мяса, такая как отверждение, добавление нитратов или нитритов или копчение, может привести к образованию потенциально вызывающих рак (канцерогенных) химических веществ. Таких как N-нитрозосоединения (NOC) и полициклические ароматические углеводороды (PAH)»
В докладе также говорится, что более 34 000 смертей от рака ежегодно вызываются высоким потреблением переработанного мяса.
Однако сообщалось, что среднесуточное потребление «летучих нитрозаминов» из пищевых продуктов составляет около одного микрограмма на человека. Это, вероятно, недостаточно для нанесения серьезного вреда.
Хотя необходимы дополнительные исследования, похоже, существует связь с повышенным риском различных видов рака. Институт Линуса Полинга утверждает, что нитраты могут быть связаны с развитием опухолей головного мозга, лейкемии и опухолей носа и горла. Экологическая рабочая группа (EWG) сообщает, что это, наряду с другими пищевыми добавками, может быть связано с раком желудка.
Возможно, что нитраты, образуя нитрозамины, могут влиять на здоровье мозга, способствуя развитию болезни Альцгеймера. Добавление продуктов с высоким содержанием жиров ухудшает ситуацию.
Были проведены эксперименты, показывающие, что нитрозамины могут вызывать диабет, а также жировые заболевания печени и ожирение. Эти исследования показывают, что дефицит двигательной функции, пространственного обучения и развития резистентности к инсулину были очевидны. В исследовании сделан вывод о том, что воздействие нитрозаминов на окружающую среду и пищевые продукты может привести к дегенеративной функции мозга. А также резистентности к инсулину. Это позволяет предположить, что благодаря лучшему обнаружению воздействия нитрозаминов на человека можно снизить риск развития болезни Альцгеймера и диабета.
3.Вред нитратов для организма человека — может навредить вашему ребенку
Слишком много нитратов или нитритов может вызвать состояние, известное как метгемоглобинемия или «синдром голубого ребенка». Метгемоглобинемия — это заболевание крови, при котором в организме вырабатывается аномальное количество метгемоглобина, который является формой гемоглобина. Это белок, обнаруживаемый в эритроцитах, который переносит и распределяет кислород по всему организму. Для любого, у кого есть метгемоглобинемия, гемоглобину трудно выполнять свою работу по эффективному выделению кислорода.
Дети могут получить это состояние из загрязненной питьевой воды. А также продуктов с высоким содержанием нитратов, таких как шпинат, свекла и морковь. Согласно статье, опубликованной Национальной медицинской библиотекой США, детям в возрасте до 6 лет лучше избегать этих продуктов.
Младенцы могут получить это состояние от загрязненной питьевой воды, а также продуктов с высоким содержанием нитратов, таких как шпинат, свекла и морковь. Согласно статье, опубликованной Национальной медицинской библиотекой США, детям в возрасте до 6 лет лучше избегать этих продуктов.
Какая еще работа проделана в этой области?
SCF и JECFA пересмотрели отношение к нитритам и нитратам, добавляемым в пищу, что привело к установлению текущих суточных норм
В 2010 году дискуссионная группа опубликовала заявление о нитритах в мясных продуктах, принимая во внимание данные Дании, которые не подтолкнули EFSA к пересмотру существующей допустимой суточной нормы. Экспертная группа EFSA по загрязняющим веществам в пищевой цепи (CONTAM) пришла к трём следующим выводам, относящимся к нитритам и нитратам, ни один из которых не предполагал пересмотр объявленных ранее установок SCF и JECFA:
— В 2008 году группа CONTAM провела оценку плюсов и минусов использования нитратов в овощах. Она пришла к выводу, что преимущества перевешивают потенциальные риски от воздействия нитратов в овощах, и что средний потребитель не превышает допустимой суточной дозы.
— В своём заключении 2009 года по нитритам как нежелательным веществам в кормах для животных группа пришла к выводу, что низкий уровень нитритов в свежих продуктах животного происхождения не вызывает беспокойства за здоровье человека.
— В 2010 году было вынесено ещё одно заключение о потенциальных рисках для здоровья младенцев и детей младшего возраста из-за нитратов естественного происхождения в листовых овощах. Группа заключила, что уровни нитратов в этих овощах не представляют опасности для здоровья большинства детей.
Международное агентство по изучению рака (МАИР) пересмотрело имеющиеся в 2010 году данные по нитритам и нитратам, но не прокомментировало допустимые суточные дозы, установленные ранее другими организациями. Оценка МАИР включает в себя рассмотрение последствий воздействия нитратов на животных и людей в ходе эпидемиологического исследования.
В 2015 году МАИР классифицировало переработанное мясо как канцероген (Группа 1), упомянув, что образование нитрозаминов также вносит вклад в этот результат. В то время как МАИР оценивает канцерогенные свойства, EFSA в своих оценках рисков также определяет вероятность и уровень воздействия веществ, то есть потенциальную опасность, которую они представляют для различных групп населения.
Перевод: Вероника Семёнова
Пятница, 23.11.2018
Источники нитратов и нитритов
Минеральные удобрения
Одним из важнейших источников нитратов являются минеральные удобрения. Дело в том, что в сельском хозяйстве для выращивания растений используются различные удобрения, а нитраты являются легко усваиваемым источником азота.
Было замечено, что не только нитратные удобрения вызывают накопление нитратов в растениях, из-за реакций в почве аммонийные удобрения (это те которые содержат NH4+) тоже могут стать источником нитратов.
Некоторые виды минеральных удобрений — не совместимы с органическими удобрениями, а их совместное применение может снизить производство сельскохозяйственной продукции.
В ЕС и США, объёмы использованных удобрений NPK (Азот-Фосфор-Калий) превышают 100 кг на 1 га, в то время как в Российской Федерации количество удобрений не превышает 50 кг/га. Лидерами в этом направлении являются Китай (488 кг/га), Республика Корея (389 кг/га) и Беларусь (288 кг/га). 2
С одной стороны увеличение количество вносимых удобрений повышает урожай, с другой стороны если удобрения не были использованы правильно (период внесения, вид удобрений, вид почвы) то может ухудшиться качество продуктов питания (например, накопление нитратов в арбузах).
Из-за специфичной физиологии растений, больше всего они нуждаются в азоте, так что больше всего в почву вносятся азотные удобрения.
Аммоний
Из-за высокого содержания азота, в развитых странах, большое количество азота использованного для удобрений происходит из аммония. 3 У химических соединений на базе аммония — очень хорошая растворимость в воде.
Сульфат аммония ((NH4)2SO4)
Сульфат аммония — важный вид азотных удобрений, который получают в волоконной промышленности, а также в производстве стали.
В случае затопления участка земли, сульфат (SO42-) переходит в сероводород, который является токсичным для растений.
Аммиачная селитра (NH4NO3)
Аммиачная селитра (нитрат аммония) содержит до 33-34 % азота, а растворимость в воде этого химического соединения — 190 г на 100 мл при 20 оС.
Эффективность этого вида удобрения повышается со снижением гумуса в почве.
Вода
Знаете ли вы, что питьевая вода содержит нитраты? Больше 20 % всех нитратов, которые попадают в наш организм, происходят из воды.
Так как растения используют воду для их жизнедеятельности, были замеченные такие явления у растений связанных с нитратами:
- продолжительное воздействие солнечных лучей на растения снижает концентрацию нитратов в них (вот почему овощи, полученные в теплицах, содержат больше нитратов);
- летом уровень нитратов в овощах снижается, потому что растения используют их для производства белков;
- зимой растения накапливают больше нитратов из-за меньшей активности Солнца, что снижает производства белка;
- утром уровень нитратов — более высокий в овощах по сравнению с вечерним периодом;
- больше всего нитратов содержится в стебле и листьях растений.
Колбаса и мясные изделия
Нитриты (E249 — Нитрит калия, Е250 — нитрит натрия) и нитраты (E251 — Нитрат натрия, E252 — Нитрат калия) добавляются в мясных изделиях. Многие думают, что для красивой окраски, но это не так. Оказывается, нитриты и нитраты добавляется в качестве консервантов.
Дело в том, что добавление нитритов уменьшило случаи заражения «колбасной палочкой», которая вызывает болезнь ботулизм.
Это, конечно же, хорошо, ведь ботулизм — очень опасное заболевание.
Фармакологические свойства нитрата серебра
Это вещество обладает следующими свойствами, благодаря которым широко используется в медицине:
- Антисептическими.
- Бактериальными.
- Противовоспалительными.
- Прижигающими.
- Вяжущими.
- Противомикробными.
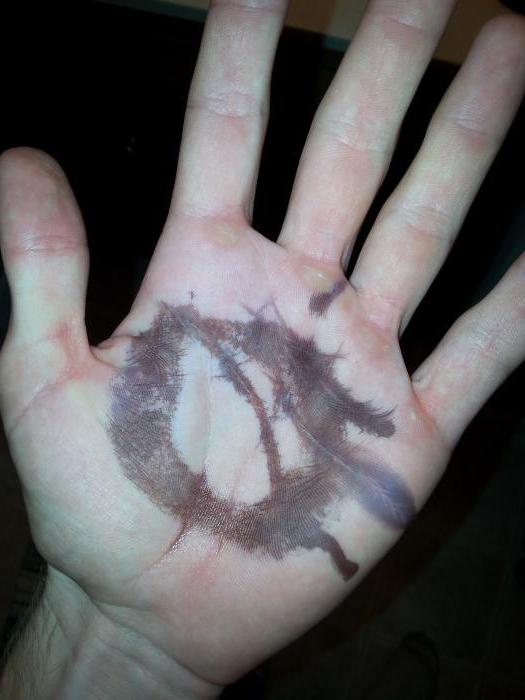
Нитрат идет на изготовление ляписа. При соприкосновении с кожей на ней появляются пятна черного цвета, а при длительном по времени контакте – ожоги большой глубины. Ляписом в медицине прижигают мелкие раны, трещины, папилломы, наросты, родинки, угри, бородавки. Широкое применение нитрат нашел в стоматологии, гомеопатии и других областях для лечения различных заболеваний.
Общие химические свойства
Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли. Практически все нитраты хорошо растворимы в воде.
Нитраты являются достаточно сильными окислителями в твёрдом состоянии (обычно в виде расплава), но практически не обладают окислительными свойствами в растворе, в отличие от азотной кислоты.
Нитраты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200—600 °C), зачастую с разложением.
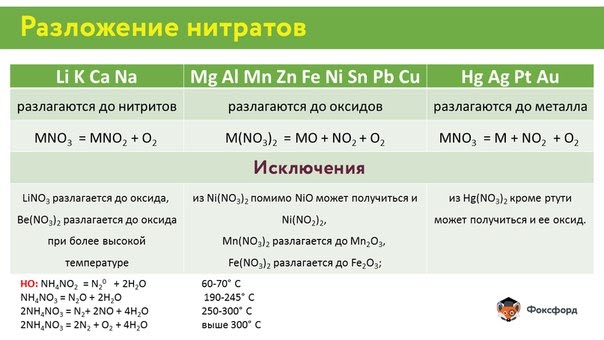
Разложение нитратов
Соли азотной кислоты при нагревании разлагаются, причём продукты разложения зависят от положения солеобразующего металла в ряду стандартных электродных потенциалов:
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Zn→Cr→Fe→Cd→Co→Ni→Sn→Pb→(H)→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
Нитраты металлов, расположенных левее магния Mg, (за исключением лития) при разложении образуют нитриты и кислород, например, нитрат натрия разлагается при температуре 300 °С:
- 2NaNO3⟶ 2NaNO2+O2↑{\displaystyle {\mathsf {\ 2NaNO_{3}\longrightarrow \ 2NaNO_{2}+O_{2}\uparrow }}}
Нитраты металлов, расположенные в ряду стандартных электродных потенциалов от Mg до Cu, а также Li дают при разложении оксид металла, NO2 и кислород. Например, нитрат меди(II) при нагревании разлагается с образованием оксида меди(II), диоксида азота и кислорода:
- 2 Cu(NO3)2→>170∘C2 CuO+4 NO2+ O2{\displaystyle {\mathsf {2\ Cu(NO_{3})_{2}{\xrightarrow {>170^{\circ }C}}2\ CuO+4\ NO_{2}+\ O_{2}}}}
Нитраты металлов, расположенных в данном ряду после Cu образуют свободный металл, NO2 и кислород. Например, нитрат серебра разлагается при температуре 170 °С, образуя свободный металл, диоксид азота и кислород.
- 2 AgNO3→>170∘C2 Ag+2 NO2+ O2{\displaystyle {\mathsf {2\ AgNO_{3}{\xrightarrow {>170^{\circ }C}}2\ Ag+2\ NO_{2}+\ O_{2}}}}
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
- Температура ниже 270°C:
- Температура выше 270 °C, или детонация:
Применение нитратов в медицине
Наиболее часто препараты Н. используются для лечения ишемической болезни сердца.
Механизм антиангинального действия Н., несмотря на то, что они применяются очень давно, недостаточно ясен. В прошлом предлагались разные объяснения. Наиболее аргументированным является представление о непосредственном миотропном (спазмолитическом) действии нитратов на коронарные сосуды, вследствие чего увеличивается приток крови к сердечной мышце и улучшается снабжение ее кислородом. Эта точка зрения не потеряла своего значения и до сих пор.
Механизм действия Н. обусловлен двумя факторами. Обладая миотропным спазмолитическим действием, Н. расширяют периферические сосуды и уменьшают венозный возврат крови к сердцу, а также понижают периферическое сопротивление сосудов. В результате этого происходит разгрузка миокарда и уменьшается его работа по преодолению сопротивления выброса крови. Энергетические затраты сердца понижаются, одновременно снижается внутримио-кардиальное напряжение и уменьшается сжатие коронарных артерий, что приводит к уменьшению ишемии и улучшению кислородного баланса в сердце. Кроме того, Н. оказывают центральное действие на продолговатый мозг, подавляя болевую импульсацию от ишемического очага в сердце, высвобождают моноамины из лабильных запасов. Показано, что в угнетении симпатического тонуса под влиянием Н. основное значение принадлежит активации свободными моноаминами процессов нисходящего торможения из продолговатого мозга.
Препараты Н. различают по скорости наступления и продолжительности антиангинального эффекта: препаратом быстрого, но короткого действия является нитроглицерин (см.), продолжительного — эринит (см.), нитросорбид (см.), а также депо-препараты (сустак и др.). Эффект после приема нитроглицерина наступает через 1 — 2 мин. и продолжается до 15—20 мин., в течение 45 мин. препарат полностью выводится из организма. Наряду с антиан-гинальным действием нитроглицерин обладает способностью расширять сосуды внутренних органов, головного мозга, сетчатки глаза. Депо-препараты представляют собой таблетки нитроглицерина, состоящие из двух частей: наружной, содержащей порцию быстровсасываю-щегося нитроглицерина (действие наступает через 10 мин.), и внутренней, содержащей фракцию нитроглицерина, медленно всасывающуюся в кишечнике (эффект проявляется в течение нескольких часов). Таблетки депо-препаратов принимают внутрь, а не под язык, Н. с медленным и продолжительным действием назначают для предупреждения приступов стенокардии и систематической терапии ишемической болезни сердца. Действие эринита проявляется через 30—45 мин. и продолжается в течение 4—5 час, а нитросорбида при приеме внутрь наступает через 5—15 мин. и длится 3—5 час. Действие нитросорбида в отличие от эринита развивается более постепенно, что обусловлено прочным связыванием препарата белками плазмы крови. Эринит хорошо переносится и хорошо всасывается в жел.-киш. тракте. Побочные явления, возникающие при применении нитроглицерина (головная боль, головокружение, шум в ушах), при назначении эринита и нитросорбида развиваются редко и менее выражены. Нитросорбид назначают также при заболеваниях, сопровождающихся спазмами периферических сосудов.
Противопоказанием для применения Н. является повышение внутриглазного давления, низкое артериальное давление.
Библиография: Вредные вещества в промышленности, под ред. Н. В. Лазарева и И. Д. Гадаскиной, т. 3, с. 110, Л., 1977; Ершов В. П. Гигиена труда в производстве минеральных удобрений, с. 38, М., 1974; Каверина Н. В., Розонов Ю. Б. и Чичканов Г. Г. Современные аспекты фармакологии анти-ангинальных средств, М., 1980; Клиническая фармакология, под ред. В. В. Заку-сова, с. 188, М., 1978; Марзеев А. М. и Жаботинский В. М. Коммунальная гигиена, М., 1979; Петухов Н. И. и др. О водно-нитратной метгемоглобинемия у детей и взрослых, Гиг. и сан., № 3, с. 14, 1972; Субботин Ф. Н. Нитраты питьевой воды и их влияние на образование метгемоглобина, там же, № 2, с. 13, 1961; Фармакология моноаминергических процессов, под ред. В. В. Закусова и Н. В. Кавериной, М., 1971; The pharmacological basis of therapeutics, ed. by L. S. Goodman a. A. Gilman, p. 806, N. Y. a. o., 1975; S o 1 1 m a n n T. A manual of pharmacology and its applications to therapeutics and toxicology, Philadelphia — L., 1957.
Как понизить концентрацию нитрата в аквариуме?
Ниже способы выведения нитрата из аквариума, их можно применять вместе и по отдельности.
СПОСОБ 1: Ежедневная смена воды по 10%. Этот способ наиболее актуален при запуске аквариума, когда к 3 недели NO3 могут свирепствовать.
 График становления азотного цикла в аквариуме после запуска
График становления азотного цикла в аквариуме после запуска
Если вы видите, что есть серьезные отклонения от графика. Действуйте указанным способом. Подменивая немного воды, вы снижаете концентрацию ядов, но в тоже время не сбиваете настройку азотного цикла в молодом аквариуме.
Обратим ваше внимание, что при аммиачной вспышке нельзя делать глубокие подмены воды (не слушаете всяких блаженных из Инета). Во-первых, вы можете сбить биологическое равновесие и азотный цикл
А во-вторых, крайне не рекомендуется резко выводить рыбок из занитрифицированного состояния. От этого они тоже могут уйти в страну вечного и вкусного мотыля.
СПОСОБ 2: Применение цеолита. Подробно о цеолите написано в нашей статье – здесь. Суть в двух словах, цеолит – ионообменник, который забирает на себя катионы NH3+|NH4+. Отметим, что цеолит действует плавно и в этом его достоинство, он мягонько так «всасывает аммиак», не нарушая дальнейшее течение дел в аквариуме.
Смысл применения цеолита при нитратной вспышке в том, что он не забирает ионы нитрата, но глушит аммиак/аммоний, которые являются первородными для NO2 и далее для NO3.


СПОСОБ 3: Применение препаратов – блокаторов нитритов. Например, Sera toxivec. Такие препараты именно блокируют, а не удаляют из воды азотистые, они просто переводят их в безопасную для гидробионтов форуму, грубо говоря, препарат дает шанс рыбам не отравиться до тех пор, пока аквариумист наладит биобаланс: подменами воды, усилением фильтрации, аэрации, рассадкой рыбы и т.д.
В тоже время азотный цикл на то и цикл, выпадение одного звена влечет за собой сбой во всей цепочке. Мы рекомендуем использовать подобные препараты аккуратно, ну и когда в аквариум просто полный треш по аммиаку и нитриту. Отметим, что Сера токсивек не блокирует нитрат. Он глушит NH4\NH3 и NO2… а без них не будет и NO3.
СПОСОБ 4: Снижение температуры и кислотности воды. Это даже не способ, а метода, но проговорить его стоит. Азотистые более «забористые» в теплой и щелочной воде. Поэтому, если вы снизите температуру с 27 до 22 градусов – это уже облегчит жизнь гидробионтам. Тоже самое и с pH, желательно, чтобы среда в аквариуме была с pH 7 и ниже.
СПОСОБ 5: Аквариумный уголь. Сам по себе уголь не забирает на себя нитрит. Но он адсорбирует «мертвую органику», которая является первоисточником возникновения NH3/NH4, далее NO2, и далее NO3.
СПОСОБ 6: Применение стартовых препаратов. Стереотипно эти препараты почему-то называют «аквариумной химией». Самое смешное, что 99% подобных препаратов – это чистая биология. Химия – это Sera toxivec. Стартовые же препараты – это концентраты полезных бактерий нитрификаторов, которые расщепляют азотистые и/или способствуют развитию этих полезных колоний бактерий.

К таким препаратам можно отнести, например, Tetra SafeStart, Tetra FilterActive, Tetra Bacrozym и т.д.
Проблему этих препаратов, по отношению к аммиачной вспышке, можно выразить фразой: «хороша ложка к обеду» или «поздно пить боржоми, когда почки отказали». Свое отношение к стартовым препаратам мы подробно изложили в статье «Быстрый запуск аквариума». Здесь скажем, только то, что если у вас уже случился полный абзац с NO2, то поздно применять «стартовые» препараты» на «финише». Их применение имеет место быть при запуске аквариума, тогда они действительно сглаживают азотистые вспышки. То есть они не действуют здесь и сейчас – прямо вот сразу.
Отметим, что также хорошо удерживают нитраты такие фишечки, как Тетра нитрат минус перлс и Тетра Баланс болс пролайн.
Вот такие способы удаления нитрата из аквариума мы расписали для вас. Наиболее эффективная схема на наш взгляд – совокупность способа 1, 2 и 5. В этом случае, мы достаточно быстро и мягко уберем яды.
Помните, что важную роль в становлении и удержании азотного цикла играет качественная фильтрация и аэрация аквариума. А также хороший грунт (легкий, пористы, покаты) уложенный слоем в 5-7 см. Ведь именно в грунте протекает львиная доля всех процессов нитрификации.
Подписывайтесь на нашYouTube-канал, чтобы ничего не пропустить
Категория: Аквариумные статьи / Полезные советы по содержанию рыбок | Просмотров: 20 520 | Дата: 7-05-2018, 15:47 |
Рекомендуем так же почитать:
- — Нитриты в аквариуме Ядъ!
- — Аммиак в аквариуме Ядъ!
- — Видео-обзор фильтра LAGUNA 1408
- — Сомики коридорасы виды
- — Барбосы
НИТРАТЫ НУЖНЫ?[править | править код]
Источник Muscle and Fitness №3
Нитраты могут быть полезны организму
Вам, наверняка, доводилось читать, что нитраты — это злейшие враги здоровья человека. Наука определила минимальные нормы содержания нитратов в продуктах питания, однако сами по себе такие нормы не являются гарантией от напастей. Все зависит от того, сколько пищи, содержащей нитраты, вы съедаете. Ну а нитраты есть во всех продуктах питания от колбас до овощей. Причем, согласно статистике около 70% нитратов человек получает с овощами, которых призывают есть больше. Откуда они там берутся? Дело в том, что элемент азот остро нужен растениям для образования хлорофилла, без которого они и вовсе не могут жить. Обычно растения берут азот из почвы. Если дополнительно удобрять почву азо-тосодержащими нитратами, урожайность растений резко увеличивается. Плоды растений, которые удобрялись нитратами, накапливают в себе эти соединения сверх всякой меры. Что же касается колбасных изделий, то здесь нитраты применяются в качестве консервирующего средства. Проще говоря, как яды против микроорганизмов. К тому же без нитратов колбаса имела бы неприглядный бледно-коричневый оттенок, ну а нитраты делают ее ярко-красной.
Избыток нитратов, бесспорно, является для человека токсичным. Дело в том, что нитраты взаимодействуют с гемоглобином крови и «переделывают» его в т.н. метгемоглобин, который уже не способен переносить кислород. В итоге образуется гипоксия — нехватка дыхания. Как раз по этой причине толстяки, плотно подсевшие на колбасу и копчености, страдают хронической одышкой.
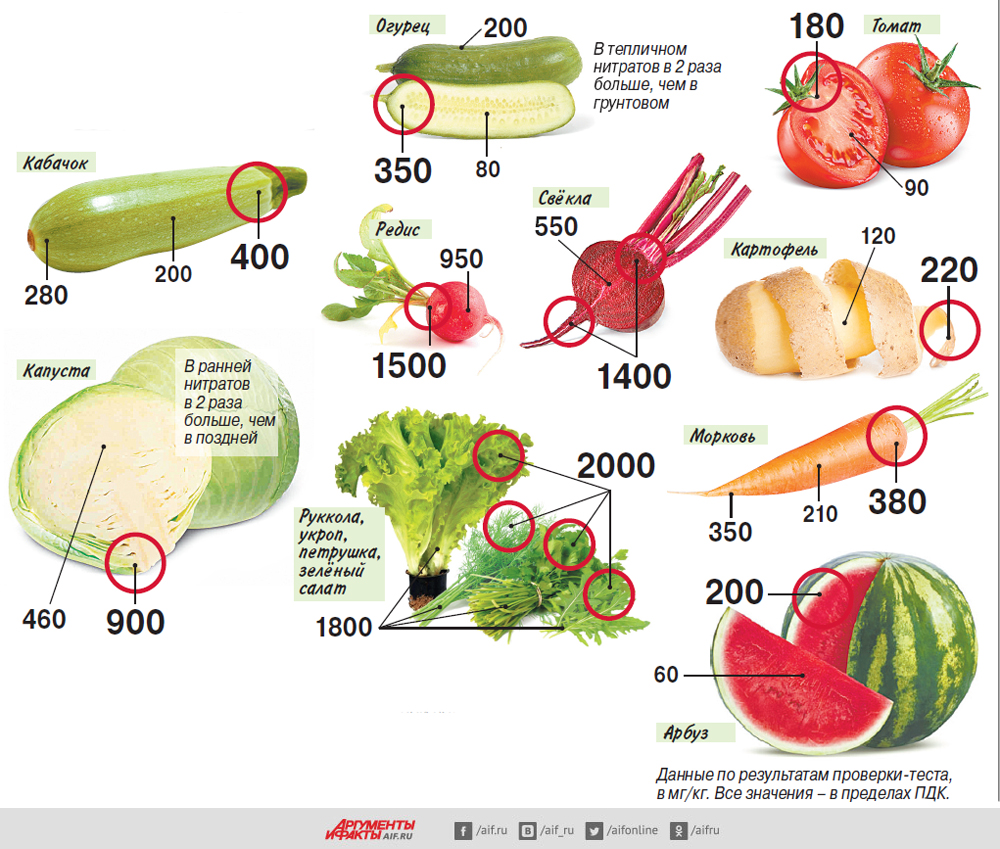
Предельно допустимая норма приема нитратов для человек составляет 5 мг на килограмм веса тела, причем, 500 мг нитратов в сутки считаются предельно допустимым количеством, а 600 мг — откровенно токсичным. При этом нужно сказать, что в промышленно развитых странах, где массово применяются минеральные удобрения, даже колодезная вода обычно содержит до 100 мг нитратов на литр. (Вода из водопровода — 20 мг/л). В колбасе обычно бывает до 500 мг/кг нитратов, хотя пищевые стандарты предполагают не больше 50-150 мг/кг. Впрочем, подлинными чемпионами по содержанию нитратов (до 5000 мг/кг) являются те овощи, которые объявлены самыми полезными: листовые салаты, шпинат, редис, свежий укроп, зеленый лук, арбузы и дыни. Средним содержанием нитратов (300-600 мг/кг) отличаются огурцы, морковь, цветная и белокачанная капуста, кабачки, тыква, репа, редька и хрен. Ну, и совсем уж мало нитратов во фруктах, ягодах, картофеле, помидорах, горохе, фасоли, брюссельской капусте, щавеле и репчатом луке (8-10 мг/кг).
Американская ассоциация по борьбе с высоким давлением обследовала слои населения, которые превышают норму потребления нитратов минимум в 5 раз и обнаружила, казалось бы, странный факт. Среди таких людей было куда меньше сердечников. И все потому, что избыток нитратов снижал кровяное давление. Впрочем, а как иначе, если нитраты широко применяются для расширения просвета сосудов у сердечных больных. Достаточно вспомнить популярный нитроглицерин, который есть в кармане у каждого, кто страдает гипертонией.
Действие нитратов объясняется просто. Они стимулируют производство известной каждому культуристу окиси азота. Причем, маленькая таблетка действует куда сильнее самой объемной порции любого новомодного донатора окиси азота.
Побочных эффектов от приема терапевтической дозы нитратов 3-4 раза в неделю (по числу тренировок), практически, не наблюдается. Это побудило компанию VPX выпустить принципиально новый продукт Power Shock, где к аминокислотам добавлены нитраты. Мощное расширение сосудов под действием азотосодержащих соединений привело к усилению кровотока и на порядок повысило усвоение аминокислот, особенно, аминокислот ВСАА. Возможно, мы стоим на пороге нового поколения более эффективных пищевых добавок, которые не только поставляют организму полезные питательные вещества, но и гарантируют их глубокое усвоение, благодаря содержанию нитратов.
Как нитраты влияют на кровяное давление и здоровье сердца
При некоторых обстоятельствах нитрит теряет атом кислорода. Затем он превращается в оксид азота, важную молекулу.
Оксид азота (NO) выполняет различные функции в организме. Он может быть токсичным в больших количествах, но также может помочь защитить организм ().
Самое главное, это сигнальная молекула. Она проходит через стенки артерий и посылает сигналы к крошечным мышечным клеткам вокруг артерий, приказывая им расслабиться ().
Когда эти клетки расслабляются, кровеносные сосуды расширяются, и кровяное давление понижается.
Нитроглицерин – это препарат, который содержит нитраты. Врачи используют его для лечения сердечной недостаточности и других состояний ().
Нитроглицерин может предотвратить или обратить вспять стенокардию – тип боли в груди, которая возникает, когда сердечная мышца не получает достаточно кислорода из-за плохого кровотока.
Содержащиеся в продуктах питания нитраты и нитриты также могут превращаться в оксид азота, расширять кровеносные сосуды и понижать кровяное давление ().
Исследования показали, что продукты с высоким содержанием нитратов и нитритов, такие как свёкла или свекольный сок, могут снизить кровяное давление. В одном исследовании артериальное давление снизилось на 4–10 мм/рт в течение нескольких часов (, , ).
Высокое кровяное давление является ключевым фактором риска развития сердечно-сосудистых заболеваний и инсульта, которые могут быть опасными для жизни.
Что такое нитраты?

На самом деле существуют нитраты и нитриты. Какая между ними разница? Чтобы это понять, придется немного вспомнить химию. Молекула каждого из этих веществ состоит из одного атома азота и нескольких атомов кислорода. Выглядит это следующим образом:
- Нитраты: 1 атом азота, 3 атома кислорода. Химическая формула: NO3-
- Нитриты: 1 атом азота, 2 атома кислорода. Химическая формула: NO2-
Так что же дает разное количество атомов кислорода в молекуле? По сути, нитраты безвредны, но когда они превращаются в нитриты, все становится сложнее. Когда нитраты попадают в организм, ферменты и бактерии в ротовой полости превращают их в нитриты. Нитриты могут быть безвредными, если они образуют оксид азота. Но при образовании нитрозаминов они могут оказывать негативное воздействие на организм человека и способствовать росту раковых клеток.
Так что потребление нитритов может быть даже полезным, так как они препятствуют формированию бактерий, вызывающих листериоз и ботулизм. Но слишком большое количество полезных веществ тоже может стать проблемой. В конце концов, нитриты применяются для придания мясу привлекательного розового или красного цвета, так как иначе оно стало бы коричневым, и вы бы его не купили. Нитриты преобразуются в оксид азота, который в свою очередь вступает в химическую реакцию с белками мяса, в результате чего изменяется его цвет.
Эта информация может казаться немного запутанной. Но давайте продолжим и узнаем еще больше о нитратах. Нитраты производятся естественным путем во фруктах, овощах и зерновых культурах. Этот процесс препятствует образованию вредных нитрозаминов. Нитрозамины используются при производстве косметических средств, пестицидов, табачных продуктов и резиновых изделий, таких как воздушные шары и презервативы. Нитрозамины также образуются при попадании нитритов в кислую среду желудка. Высокие температуры и обжаривание увеличивает вероятность образования нитрозаминов.
Нитраты также представляют собой соли азотной кислоты. Как было отмечено выше, они добавляются в такие продукты, как салями, пепперони и бекон для придания цвета и препятствования росту вредных микроорганизмов. Но вопрос безопасности по-прежнему не разрешен. Если нитраты образуются естественных путем в некоторых пищевых продуктах, то все не может быть очень плохо, не так ли? Что ж, в некоторых случаях это верно. Фрукты, овощи и зерновые культуры, богатые нитратами, могут обеспечить множество преимуществ для здоровья, в том числе расслабление кровеносных сосудов и улучшение кровотока
На самом деле очень важно, чтобы наши тела производили нитриты. Природные нитраты безвредны для человека, так как витамин С в овощах и фруктах предотвращает формирование нитрозаминов
По данным Центра Контроля и Профилактики Заболеваний, копчености поставляют в наш организм лишь около 6% всех нитратов. Остальные поставляются водой и овощами. Все растения содержат нитраты, но больше всего их в таких овощах, как сельдерей, зелень, свекла, петрушка, лук-порей, цикорий, капуста и укроп.
Нитраты иногда назначаются людям, страдающим от проблем с сердцем, так как они помогают расслабить кровеносные сосуды и облегчить боли в грудной клетке. В Национальном Институте Сердца, Легких и Крови утверждают, что нитроглицерин является наиболее часто употребляемым нитратом для таких целей.
Общие химические свойства
Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли. Практически все нитраты хорошо растворимы в воде.
Нитраты являются достаточно сильными окислителями в твёрдом состоянии (обычно в виде расплава), но практически не обладают окислительными свойствами в растворе, в отличие от азотной кислоты.
Нитраты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200—600 °C), зачастую с разложением.
Разложение нитратов
Соли азотной кислоты при нагревании разлагаются, причём продукты разложения зависят от положения солеобразующего металла в ряду стандартных электродных потенциалов:
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Zn→Cr→Fe→Cd→Co→Ni→Sn→Pb→(H)→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
Нитраты металлов, расположенных левее магния Mg, (за исключением лития) при разложении образуют нитриты и кислород, например, нитрат натрия разлагается при температуре 300 °С:
- 2NaNO3⟶ 2NaNO2+O2↑{\displaystyle {\mathsf {\ 2NaNO_{3}\longrightarrow \ 2NaNO_{2}+O_{2}\uparrow }}}
Нитраты металлов, расположенные в ряду стандартных электродных потенциалов от Mg до Cu, а также Li дают при разложении оксид металла, NO2 и кислород. Например, нитрат меди(II) при нагревании разлагается с образованием оксида меди(II), диоксида азота и кислорода:
- 2 Cu(NO3)2→>170∘C2 CuO+4 NO2+ O2{\displaystyle {\mathsf {2\ Cu(NO_{3})_{2}{\xrightarrow {>170^{\circ }C}}2\ CuO+4\ NO_{2}+\ O_{2}}}}
Нитраты металлов, расположенных в данном ряду после Cu образуют свободный металл, NO2 и кислород. Например, нитрат серебра разлагается при температуре 170 °С, образуя свободный металл, диоксид азота и кислород.
- 2 AgNO3→>170∘C2 Ag+2 NO2+ O2{\displaystyle {\mathsf {2\ AgNO_{3}{\xrightarrow {>170^{\circ }C}}2\ Ag+2\ NO_{2}+\ O_{2}}}}
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
- Температура ниже 270°C:
- Температура выше 270 °C, или детонация: