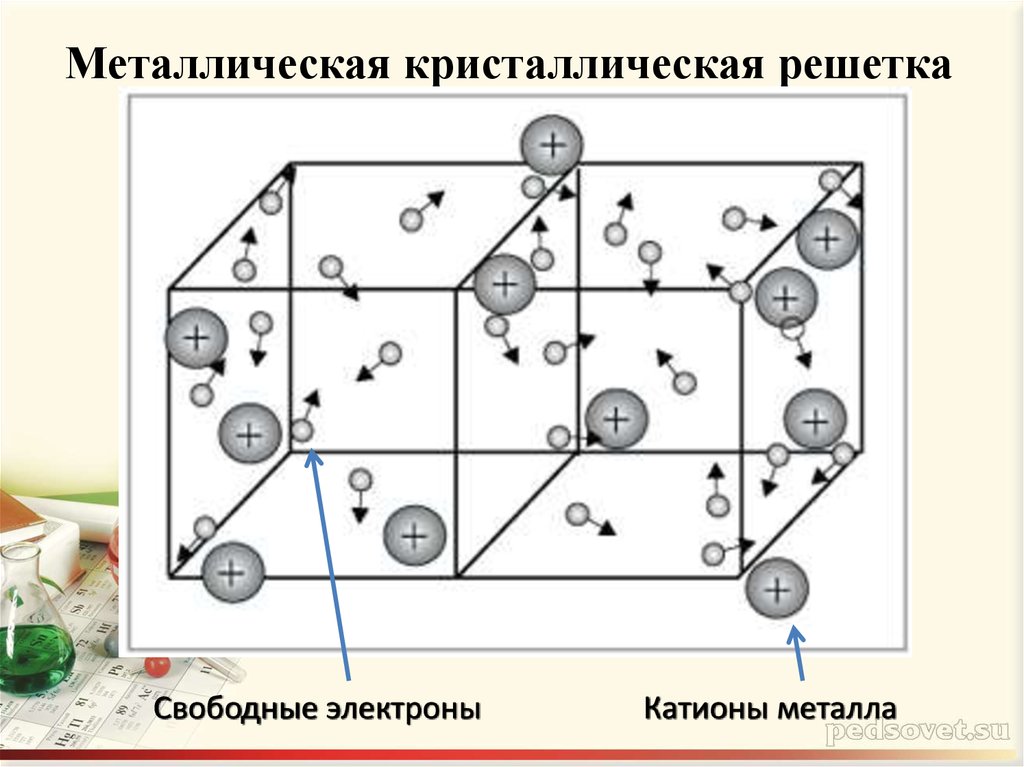
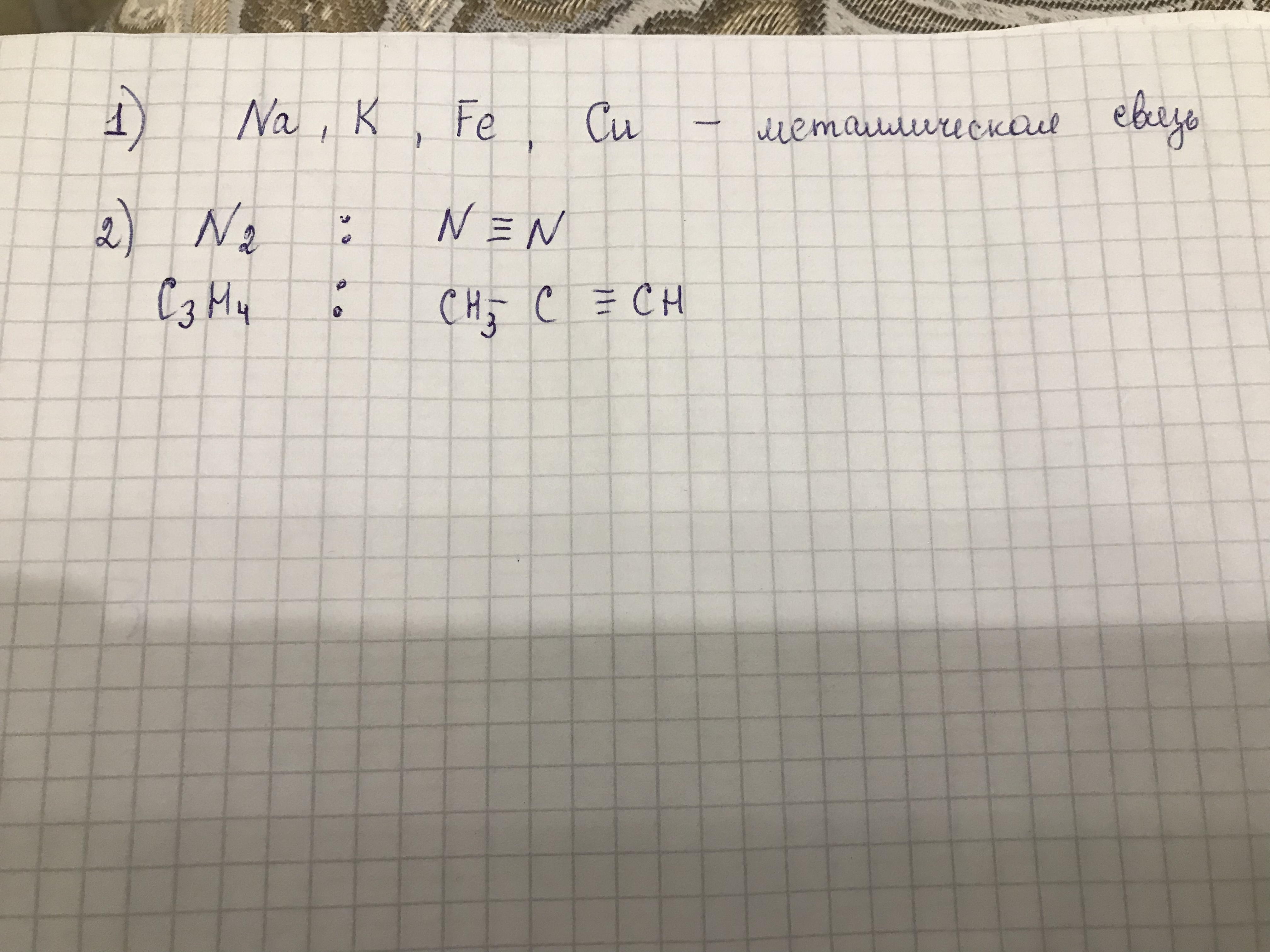Водородная связь
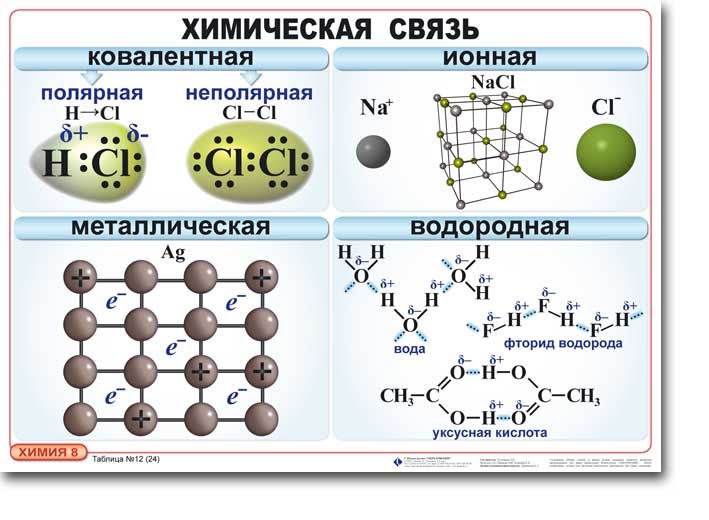
Водородная связь ― связь между электроотрицательным атомом (F, O, N) и атомом водорода, который ковалентно связан с другим электроотрицательным атомом (F, O, N).
Водородные связи влияют на физические (температуру кипения, температуру плавления) и химические (кислотно-основные) свойства соединений.
Межмолекулярные водородные связи обусловливают ассоциацию молекул, что приводит к повышению температур кипения и плавления вещества. Например, этиловый спирт C2H5OH, способный к ассоциации, кипит при +78,3°С, а диметиловый эфир СН3ОСН3, не образующий водородных связей, лишь при –24°С (молекулярная формула обоих веществ С2Н6О).
| Тип связи | Примеры |
| Ковалентная неполярная | Cl2, O2, Br2, I2, N2 и др. |
| Ковалентная полярная | HCl, H2S, HBr, H2O, SO2, SO3 и др. |
| Ионная | NaCl, KCl, CaBr2, Na2O и др. |
| Металлическая | Na, Ca, Zn, Al и др. |
| Водородная | Между молекулами:
|
Водородная химическая связь
Еще задолго до появления современной теории химических связей в ее современном виде учеными химиками было замечено, что соединения водорода с неметаллами обладают различными удивительными свойствами. Скажем, температура кипения воды и вместе со фтороводородом гораздо выше, чем это могло бы быть, вот вам готовый пример водородной химической связи.
На картинке схема образования водородной химической связи.
Природа и свойства водородной химической связи обусловлены способностью атома водорода H образовывать еще одну химическую связь, отсюда собственно и название этой связи. Причиной образования такой связи являются свойства электростатических сил. Например, общее электронное облако в молекуле фтороводорода настолько смещено в сторону фтора, что пространство вокруг атома этого вещества насыщено отрицательным электрическим полем. Вокруг атома водорода, тем более лишенного своего единственного электрона, все с точностью до наоборот, его электронное поле значительно слабее и как следствие имеет положительный заряд. А положительные и отрицательные заряды, как известно, притягиваются, таким нехитрым образом и возникает водородная связь.
Схема связи и примеры
Процесс, происходящий в металле можно записать с помощью формулы:
К — е <—> К +
Al — 3e <—> Al3+
Na — e <—> Na+
Zn — 2e <—> Zn2+
Fe — 3e <—> Fe3+
Если описывать более подробно, металлическую связь, как образуется этот тип связи, необходимо рассматривать строение внешних энергетических уровней элемента.
В качестве примера можно рассмотреть натрий. Имеющийся на внешнем уровне единственный валентный 3s электрон может свободно перемещаться по свободным орбиталям третьего энергетического уровня. При сближении атомов натрия, происходит перекрывание орбиталей. Теперь уже все электроны могут перемещаться между атом-ионами в пределах всех пререкрывшихся орбиталей.
У цинка на 2 валентных электрона приходится целых 15 свободных орбиталей на четвёртом энергетическом уровне. При взаимодействии атомов эти свободные орбитали будут перекрываться, как бы обобществляя электроны, которые по ним перемещаются.
У атомов хрома валентных электронов 6 и все они будут участвовать в образовании электронного газа и связывать атом-ионы.
Характерные кристаллические решётки
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt, Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Примеры образования связи в металлах
Рассмотрим несколько конкретных вариантов, которые иллюстрируют, как образуется металлическая связь. Примеры веществ следующие:
- цинк;
- алюминий;
- калий;
- хром.
Образование металлической связи между атомами цинка: Zn — 2e- Zn2+. Атом цинка имеет четыре энергетических уровня. Свободных орбиталей, исходя из электронного строения, у него 15 — 3 на р-орбитали, 5 на 4 d и 7 на 4f. Электронное строение следующее: 1s22s22p63s23p64s23d104p4d4f, всего в атоме 30 электронов. То есть две свободные валентные отрицательные частицы способны перемещаться в пределах 15 просторных и никем не занятых орбиталей. И так у каждого атома. В итоге — огромное общее пространство, состоящее из пустующих орбиталей, и небольшое количество электронов, связывающих всю структуру воедино.
Металлическая связь между атомами алюминия: AL — e- AL3+ . Тринадцать электронов атома алюминия располагаются на трех энергетических уровнях, которых им явно хватает с избытком. Электронное строение: 1s22s22p63s23p13d. Свободных орбиталей — 7 штук. Очевидно, что электронное облако будет небольшим по сравнению с общим внутренним свободным пространством в кристалле.

Металлическая связь хрома. Данный элемент особый по своему электронному строению. Ведь для стабилизации системы происходит провал электрона с 4s на 3d орбиталь: 1s22s22p63s23p64s13d54p4d4f. Всего 24 электрона, из которых валентных получается шесть. Именно они уходят в общее электронное пространство на образование химической связи. Свободных орбиталей 15, то есть все равно намного больше, чем требуется для заполнения. Поэтому хром — также типичный пример металла с соответствующей связью в молекуле.
Одним из самых активных металлов, реагирующих даже с обычной водой с возгоранием, является калий. Чем объясняются такие свойства? Опять же во многом — металлическим типом связи. Электронов у этого элемента всего 19, но вот располагаются они аж на 4 энергетических уровнях. То есть на 30 орбиталях разных подуровней. Электронное строение: 1s22s22p63s23p64s13d4p4d4f. Всего два валентных электрона, с очень низкой энергией ионизации. Свободно отрываются и уходят в общее электронное пространство. Орбиталей для перемещения на один атом 22 штуки, то есть очень обширное свободное пространство для «электронного газа».
Механизм металлической связи
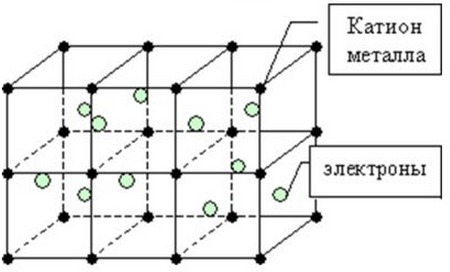
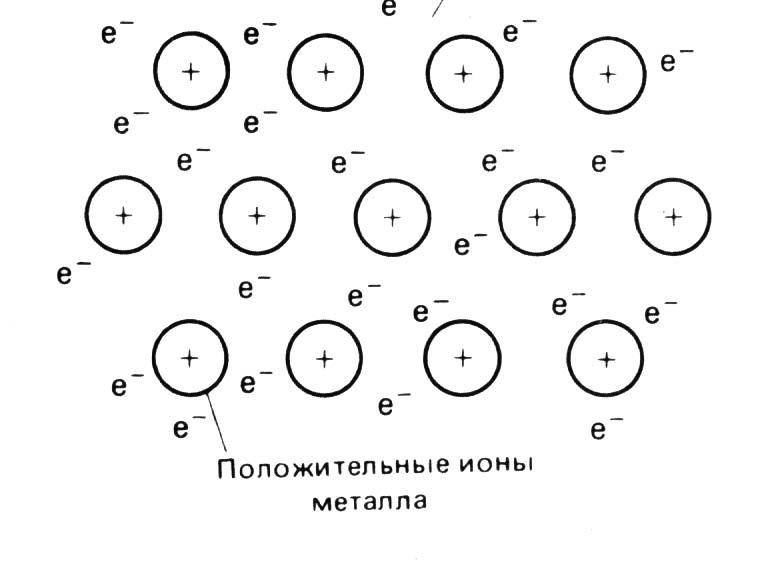
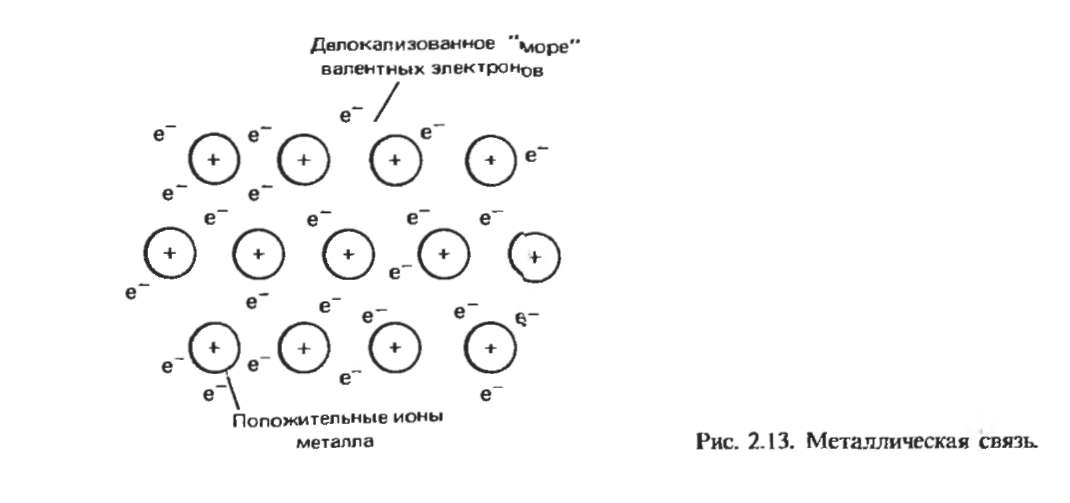
В узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа, движутся электроны проводимости, происходящие из атомов металлов при образовании ионов. Эти электроны играют роль «цемента», удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Силы связи не локализованы и не направлены. В металлах в большинстве случаев проявляются высокие координационные числа (например, 12 или 8).
Рис.1. Расположение ионов в кристалле щелочного металла
Рис.2. Связывающее звено кристаллической решётки щелочного металла
Так, щелочные металлы кристаллизуются в кубической объёмно-центрированной решётке, и каждый положительно заряженный ион щелочного металла имеет в кристалле по восемь ближайших соседей — положительно заряженных ионов щелочного металла (рис.1). Кулоновское отталкивание одноимённо-заряженных частиц (ионов) компенсируется электростатическим притяжением к электронам связывающих звеньев, имеющих форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величине постоянной решётки aw кристалла щелочного металла (рис.2).
Связывающие электроны становятся общими для системы из шести положительных ионов щелочных металлов и удерживают последние от кулоновского отталкивания.
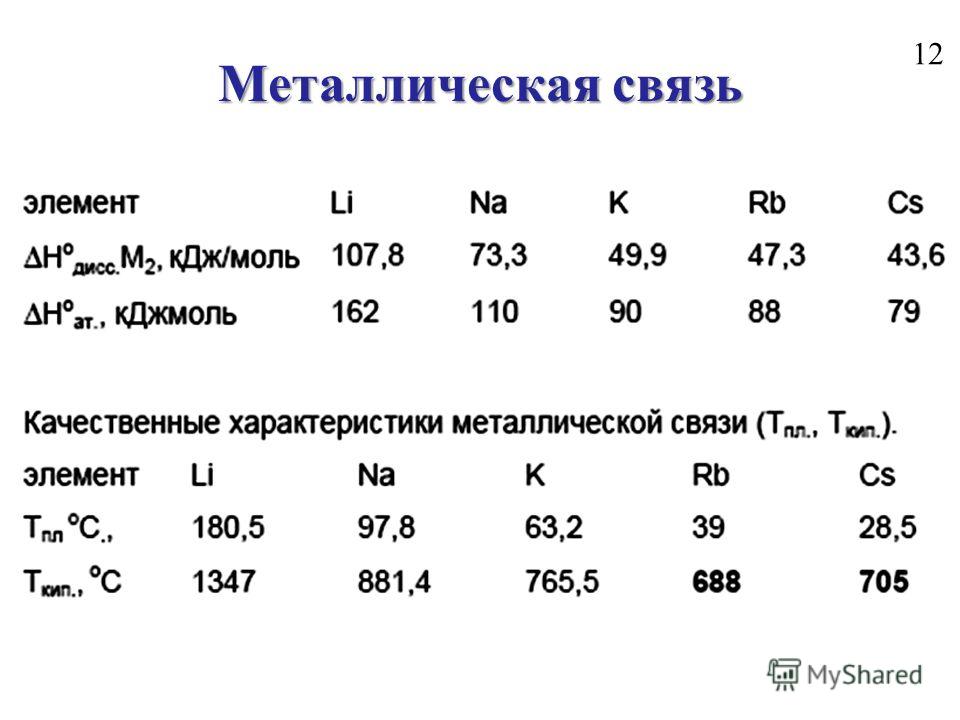
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щёлочный металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётки aw, Å | 3,502 | 4,282 | 5,247 | 5,690 | 6,084 |
| Длина ковалентной связи для Me2, Å | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место в k-пространстве, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток. Таким образом, электрический ток в металлах — это движение сорванных с орбитального радиуса электронов в поле положительно заряженных ионов, находящихся в узлах кристаллической решётки металла. Выход и вход свободных электронов в связывающее звено кристалла осуществляется через точки «0», равноудалённые от положительных ионов атомов (рис.2).
Свободное движение электронов в металле подтверждено в 1916 году опытом Толмена и Стюарта по резкому торможению быстро вращающейся катушки с проводом — свободные электроны продолжали двигаться по инерции, в результате чего гальванометр регистрировал импульс электрического тока. Свободное движение электронов в металле обусловливает высокую теплопроводность металла и склонность металлов к термоэлектронной эмиссии, происходящей при умеренной температуре.
Колебание ионов кристаллической решётки создаёт сопротивление движению электронов по металлу, сопровождающееся разогревом металла. В настоящее время важнейшим признаком металлов считается положительный температурный коэффициент электрической проводимости, то есть понижение проводимости с ростом температуры. С понижением температуры электросопротивление металлов уменьшается, вследствие уменьшения колебаний ионов в кристаллической решётке. В процессе исследования свойств материи при низких температурах Камерлинг-Оннес открывает явление сверхпроводимости. В 1911 году ему удаётся обнаружить уменьшение электросопротивления ртути при температуре кипения жидкого гелия (4,2 К) до нуля. В 1913 году Камерлинг-Оннесу присуждается Нобелевская премия по физике со следующей формулировкой: «За исследование свойств веществ при низких температурах, которые привели к производству жидкого гелия.»
Однако теория сверхпроводимости была создана позднее. В её основе лежит концепция куперовской электронной пары — коррелированного состояния связывающих электронов с противоположными спинамии и импульсами, и, следовательно, сверхпроводимость можно рассматривать как сверхтекучесть электронного газа, состоящего из куперовских пар электронов, через ионную кристаллическую решётку. В 1972 году авторам теории БКШ — Бардину, Куперу и Шрифферу присуждена Нобелевская премия по физике «За создание теории сверхпроводимости, обычно называемой БКШ-теорией».
Металлы и их физические свойства
Металлы находятся в подавляющем большинстве среди всех химических элементов. Это объясняется их особыми свойствами. Значительная часть из них была получена человеком ядерными реакциями в лабораторных условиях, они являются радиоактивными с небольшим периодом полураспада.
Однако большинство — это природные элементы, которые формируют целые горные породы и руды, входят в состав большинства важных соединений. Именно из них люди научились отливать сплавы и изготавливать массу прекрасных и важных изделий. Это такие, как медь, железо, алюминий, серебро, золото, хром, марганец, никель, цинк, свинец и многие другие.
Для всех металлов можно выделить общие физические свойства, которые объясняет схема образования металлической связи. Какие же это свойства?
- Ковкость и пластичность. Известно, что многие металлы можно прокатать даже до состояния фольги (золото, алюминий). Из других получают проволоку, металлические гибкие листы, изделия, способные деформироваться при физическом воздействии, но тут же восстанавливать форму после прекращения его. Именно эти качества металлов и называют ковкостью и пластичностью. Причина этой особенности — металлический тип связи. Ионы и электроны в кристалле скользят относительно друг друга без разрыва, что и позволяет сохранять целостность всей структуры.
- Металлический блеск. Это также объясняет металлическая связь, механизм образования, характеристики ее и особенности. Так, не все частицы способны поглощать или отражать световые волны одинаковой длины. Атомы большинства металлов отражают коротковолновые лучи и приобретают практически одинаковую окраску серебристого, белого, бледно-голубоватого оттенка. Исключениями являются медь и золото, их окраска рыже-красная и желтая соответственно. Они способны отражать более длинноволновое излучение.
- Тепло- и электропроводность. Данные свойства также объясняются строением кристаллической решетки и тем, что в ее образовании реализуется металлический тип связи. За счет «электронного газа», движущегося внутри кристалла, электрический ток и тепло мгновенно и равномерно распределяются между всеми атомами и ионами и проводятся через металл.
- Твердое агрегатное состояние при обычных условиях. Здесь исключением является лишь ртуть. Все остальные металлы — это обязательно прочные, твердые соединения, равно как и их сплавы. Это также результат того, что в металлах присутствует металлическая связь. Механизм образования такого типа связывания частиц полностью подтверждает свойства.
Это основные физические характеристики для металлов, которые объясняет и определяет именно схема образования металлической связи. Актуален такой способ соединения атомов именно для элементов металлов, их сплавов. То есть для них в твердом и жидком состоянии.

А: + B= А:В
При этом один из атомов предоставляет неподеленную электронную пару (донор), а другой атом предоставляет вакантную орбиталь для этой пары (акцептор). В результате образования связи оба энергия электронов уменьшается, т.е. это выгодно для атомов.
Ковалентная связь, образованная по донорно-акцепторному механизму, не отличается по свойствам от других ковалентных связей, образованных по обменному механизму. Образование ковалентной связи по донорно-акцепторному механизму характерно для атомов либо с большим числом электронов на внешнем энергетическом уровне (доноры электронов), либо наоборот, с очень малым числом электронов (акцепторы электронов). Более подробно валентные возможности атомов рассмотрены в соответствующей статье.
Ковалентная связь по донорно-акцепторному механизму образуется:
– в молекуле угарного газа CO (связь в молекуле – тройная, 2 связи образованы по обменному механизму, одна – по донорно-акцепторному): C≡O;
– в ионе аммония NH4+, в ионах органических аминов, например, в ионе метиламмония CH3-NH2+;
– в комплексных соединениях, химическая связь между центральным атомом и группами лигандов, например, в тетрагидроксоалюминате натрия Na[Al(OH)4] связь между алюминием и гидроксид-ионами;
– в азотной кислоте и ее солях — нитратах: HNO3, NaNO3, в некоторых других соединениях азота;
– в молекуле озона O3.
Основные характеристики ковалентной связи
Ковалентная связь, как правило, образуется между атомами неметаллов. Основными характеристиками ковалентной связи являются длина, энергия, кратность и направленность.
Кратность химической связи
Кратность химической связи — это число общих электронных пар между двумя атомами в соединении. Кратность связи достаточно легко можно определить из значения валентности атомов, образующих молекулу.
Например, в молекуле водорода H2 кратность связи равна 1, т.к. у каждого водорода только 1 неспаренный электрон на внешнем энергетическом уровне, следовательно, образуется одна общая электронная пара.
В молекуле кислорода O2 кратность связи равна 2, т.к. у каждого атома на внешнем энергетическом уровне есть по 2 неспаренных электрона: O=O.
В молекуле азота N2 кратность связи равна 3, т.к. между у каждого атома по 3 неспаренных электрона на внешнем энергетическом уровне, и атомы образуют 3 общие электронные пары N≡N.
Длина ковалентной связи
Длина химической связи – это расстояние между центрами ядер атомов, образующих связь. Ее определяют экспериментальными физическими методами. Оценить величину длины связи можно примерно, по правилу аддитивности, согласно которому длина связи в молекуле АВ приблизительно равна полусумме длин связей в молекулах А2 и В2:
Длину химической связи можно примерно оценить по радиусам атомов, образующих связь, или по кратности связи, если радиусы атомов не сильно отличаются.
При увеличении радиусов атомов, образующих связь, длина связи увеличится.
Например. В ряду: C–C, C=C, C≡C длина связи уменьшается.
| Связь |
Длина связи, нм |
| H-F | 0,092 |
| H-Cl | 0,128 |
| H-Br | 0,142 |
| H-I | 0,162 |
При увеличении кратности связи между атомами (атомные радиусы которых не отличаются, либо отличаются незначительно) длина связи уменьшится.
Например. В ряду: C–C, C=C, C≡C длина связи уменьшается.
| Связь |
Длина связи, нм |
| С–С | 0,154 |
| С=С | 0,133 |
| С≡С | 0,120 |
Энергия связи
Мерой прочности химической связи является энергия связи. Энергия связи определяется энергией, необходимой для разрыва связи и удаления атомов, образующих эту связь, на бесконечно большое расстояние друг от друга.
Ковалентная связь является очень прочной. Ее энергия составляет от нескольких десятков до нескольких сотен кДж/моль. Чем больше энергия связи, тем больше прочность связи, и наоборот.
Прочность химической связи зависит от длины связи, полярности связи и кратности связи. Чем длиннее химическая связь, тем легче ее разорвать, и тем меньше энергия связи, тем ниже ее прочность. Чем короче химическая связь, тем она прочнее, и тем больше энергия связи.
Например, в ряду соединений HF, HCl, HBr слева направо прочность химической связи уменьшается, т.к. увеличивается длина связи.
Примеры образования связи в металлах
Рассмотрим несколько конкретных вариантов, которые иллюстрируют, как образуется металлическая связь. Примеры веществ следующие:
- цинк;
- алюминий;
- калий;
- хром.
Образование металлической связи между атомами цинка: Zn — 2e- Zn2+. Атом цинка имеет четыре энергетических уровня. Свободных орбиталей, исходя из электронного строения, у него 15 — 3 на р-орбитали, 5 на 4 d и 7 на 4f. Электронное строение следующее: 1s22s22p63s23p64s23d104p4d4f, всего в атоме 30 электронов. То есть две свободные валентные отрицательные частицы способны перемещаться в пределах 15 просторных и никем не занятых орбиталей. И так у каждого атома. В итоге — огромное общее пространство, состоящее из пустующих орбиталей, и небольшое количество электронов, связывающих всю структуру воедино.
Металлическая связь между атомами алюминия: AL — e- AL3+ . Тринадцать электронов атома алюминия располагаются на трех энергетических уровнях, которых им явно хватает с избытком. Электронное строение: 1s22s22p63s23p13d. Свободных орбиталей — 7 штук. Очевидно, что электронное облако будет небольшим по сравнению с общим внутренним свободным пространством в кристалле.

Металлическая связь хрома. Данный элемент особый по своему электронному строению. Ведь для стабилизации системы происходит провал электрона с 4s на 3d орбиталь: 1s22s22p63s23p64s13d54p4d4f. Всего 24 электрона, из которых валентных получается шесть. Именно они уходят в общее электронное пространство на образование химической связи. Свободных орбиталей 15, то есть все равно намного больше, чем требуется для заполнения. Поэтому хром — также типичный пример металла с соответствующей связью в молекуле.
Одним из самых активных металлов, реагирующих даже с обычной водой с возгоранием, является калий. Чем объясняются такие свойства? Опять же во многом — металлическим типом связи. Электронов у этого элемента всего 19, но вот располагаются они аж на 4 энергетических уровнях. То есть на 30 орбиталях разных подуровней. Электронное строение: 1s22s22p63s23p64s13d4p4d4f. Всего два валентных электрона, с очень низкой энергией ионизации. Свободно отрываются и уходят в общее электронное пространство. Орбиталей для перемещения на один атом 22 штуки, то есть очень обширное свободное пространство для «электронного газа».
Характерные кристаллические решётки
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt, Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Насыщаемость
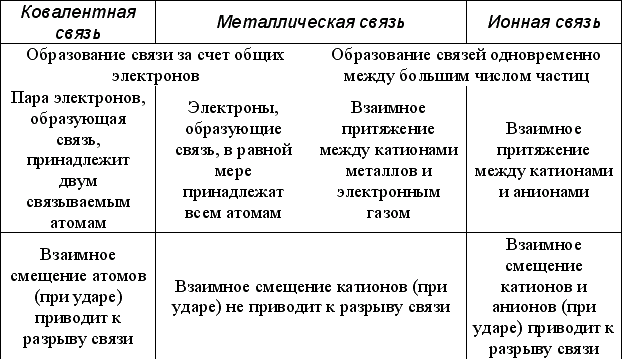
Данная характеристика отражает способность атомов к ограниченному или неограниченному взаимодействию с другими. Так, ковалентная и металлическая связь по этому показателю опять же являются противоположностями.
Первая является насыщаемой. Атомы, принимающие участие в ее образовании, имеют строго определенное количество валентных внешних электронов, принимающих непосредственное участие в образовании соединения. Больше, чем есть, у него электронов не будет. Поэтому и количество формируемых связей ограничено валентностью. Отсюда насыщаемость связи. Благодаря данной характеристике большинство соединений имеет постоянный химический состав.
Металлическая и водородная связи, напротив, ненасыщаемые. Это объясняется наличием многочисленных свободных электронов и орбиталей внутри кристалла. Также роль играют ионы в узлах кристаллической решетки, каждый из которых может стать атомом и снова ионом в любой момент времени.
Еще одна характеристика металлической связи — делокализация внутреннего электронного облака. Она проявляется в способности небольшого количества общих электронов связывать между собой множество атомных ядер металлов. То есть плотность как бы делокализуется, распределяется равномерно между всеми звеньями кристалла.
Характеристики связи: ненаправленность
Ковалентная и металлическая связь имеют одну очень ярко выраженную отличительную черту. В отличие от первой, металлическая связь не является направленной. Что это значит? То есть электронное облако внутри кристалла движется совершенно свободно в его пределах в разных направлениях, каждый из электронов способен присоединяться к абсолютно любому иону в узлах структуры. То есть взаимодействие осуществляется по разным направлениям. Отсюда и говорят о том, что металлическая связь — ненаправленная.
Механизм ковалентной связи подразумевает образование общих электронных пар, то есть облаков перекрывания атомов. Причем происходит оно строго по определенной линии, соединяющей их центры. Поэтому говорят о направленности такой связи.
Металлическая химическая связь
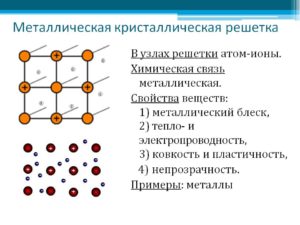
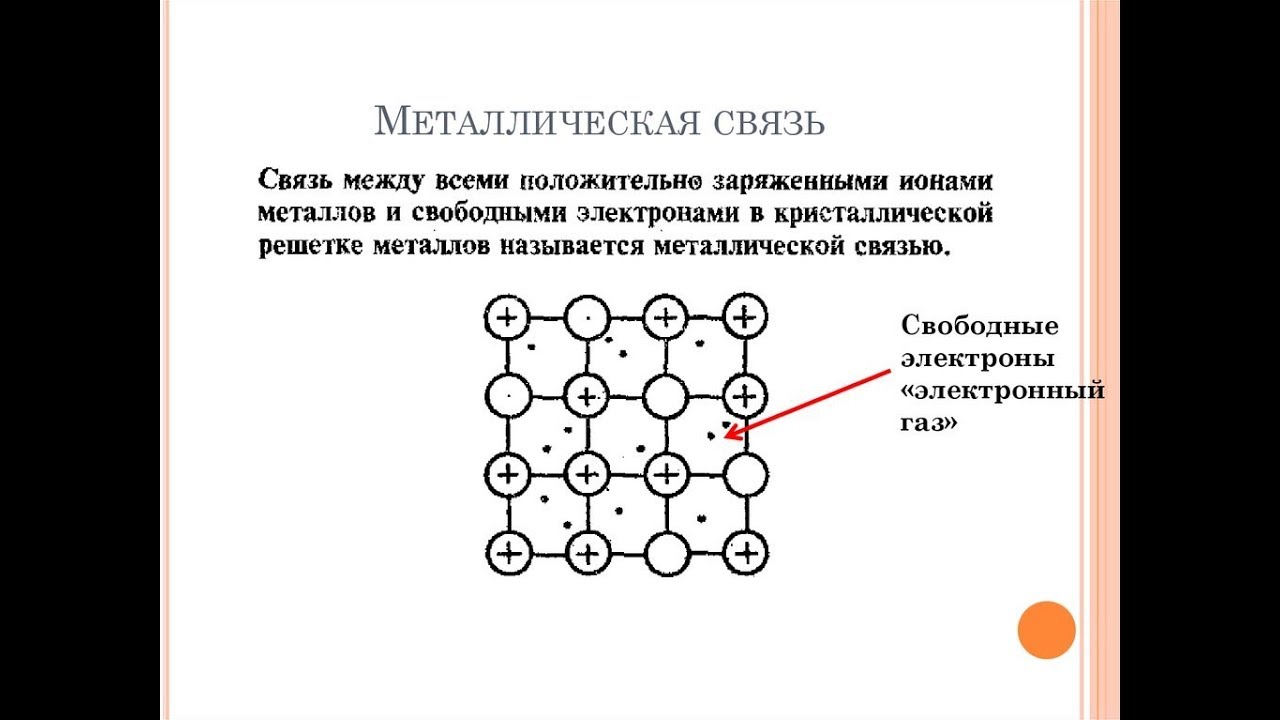
Металлическая связь — это связь, которую образуют относительно свободные электроны между ионами металлов, образующих кристаллическую решетку.
У атомов металлов на внешнем энергетическом уровне обычно расположены от одного до трех электронов. Радиусы у атомов металлов, как правило, большие — следовательно, атомы металлов, в отличие от неметаллов, достаточно легко отдают наружные электроны, т.е. являются сильными восстановителями.
Отдавая электроны, атомы металлов превращаются в положительно заряженные ионы. Оторвавшиеся электроны относительно свободно перемещаются между положительно заряженными ионами металлов. Между этими частицами возникает связь, т.к. общие электроны удерживают катионы металлов, расположенные слоями, вместе, создавая таким образом достаточно прочную металлическую кристаллическую решетку. При этом электроны непрерывно хаотично двигаются, т.е. постоянно возникают новые нейтральные атомы и новые катионы.
Межмолекулярные взаимо-действия
Отдельно стоит рассмотреть взаимодействия, возникающие между отдельными молекулами в веществе — межмолекулярные взаимодействия. Межмолекулярные взаимодействия — это такой вид взаимодействия между нейтральными атомами, при котором не появляеются новые ковалентные связи. Силы взаимодействия между молекулами обнаружены Ван-дер Ваальсом в 1869 году, и названы в честь него Ван-дар-Ваальсовыми силами. Силы Ван-дер-Ваальса делятся на ориентационные, индукционные и дисперсионные. Энергия межмолекулярных взаимодейстий намного меньше энергии химической связи.
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Особый вид межмолекулярного взаимодействия — водородные связи. Водородные связи — это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O или H-N. Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения.
Механизм образования водородной связи частично электростатический, а частично — донорно–акцепторный. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором — атомы водорода, соединенные с этими атомами. Для водородной связи характерны направленность в пространстве и насыщаемость.
Водородную связь можно обозначать точками: Н ··· O. Чем больше электроотрицательность атома, соединенного с водородом, и чем меньше его размеры, тем крепче водородная связь. Она характерна прежде всего для соединений фтора с водородом, а также кислорода с водородом, в меньшей степени азота с водородом.
Водородные связи возникают между следующими веществами:
— фтороводород HF (газ, раствор фтороводорода в воде — плавиковая кислота), вода H2O (пар, лед, жидкая вода):
— раствор аммиака и органических аминов — между молекулами аммиака и воды;
— органические соединения, в которых связи O-H или N-H: спирты, карбоновые кислоты, амины, аминокислоты, фенолы, анилин и его производные, белки, растворы углеводов — моносахаридов и дисахаридов.
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение тепературы кипения.
Например, как правило, при повышении молекулярной массы наблюдается повышение температуры кипения веществ. Однако в ряду веществ H2O-H2S-H2Se-H2Te мы не наблюдаем линейное изменение температур кипения.
А именно, у воды температура кипения аномально высокая — не меньше -61оС, как показывает нам прямая линия, а намного больше, +100 оС. Эта аномалия объясняется наличием водородных связей между молекулами воды. Следовательно, при обычных условиях (0-20оС) вода является жидкостью по фазовому состоянию.
Металлическая химическая связь

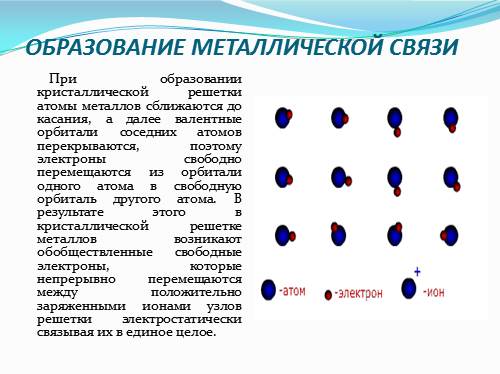
Эти электроны, свободно перемещающиеся в кристаллической решётке, называют «электронным газом».
На рисунке схематично изображено строение вещества металла.
То есть в объёме металла атомы постоянно превращаются в ионы (их называют атом-ионами) и наоборот ионы постоянно принимают электроны из «электронного газа».
Механизм образования металлической связи можно записать в виде формулы:
атом M — ne ион Mn+
Таким образом, металлы представляют собой положительные ионы, которые расположены в кристаллической решётке в определённых положениях, и электроны, которые могут достаточно свободно перемещаться между атом-ионами.
Кристаллическая решётка представляет «скелет», остов вещества, а электроны перемещаются между её узлами. Формы кристаллических решёток металлов могут быть различными, например:
- объёмно-центрическая кубическая решётка характерна для щелочных металлов;
- гранецентрическую кубическую решётку имеют, например, цинк, алюминий, медь, другие переходные элементы;
- гексагональная форма типична для щёлочноземельных элементов (исключением является барий);
- тетрагональная структура — у индия;
- ромбоэдрическая — у ртути.
Пример кристаллической решётки металла показан на картинке ниже.
Отличия от других видов

Энергия металлических связей меньше
В случае с металлической связью, нельзя говорить и о направленности, ковалентная связь строго направлена в пространстве.
Такая характеристика, как насыщаемость также не характерна для взаимодействия между атомами металлов. В то время как ковалентные связи являются насыщаемыми, то есть количество атомов, с которыми может произойти взаимодействие, строго ограничено количеством валентных электронов.