Применение графита

Как известно такой материал, как графит обладает большим количеством уникальных качеств. Именно они обуславливают сферы его применения. Благодаря тому. что данный материал обладает устойчивостью к высоким температурам его применяют для производства футеровочных плит.
Применение графита используется и в сфере ядерной промышленности. Там он играет важную роль при замедлении нейтронов.
Получение алмаза из графита тоже возможно. В современном мире есть возможность получать синтетический алмаз, который по своим качествам и внешнему виду будет напоминать природный материал.
Пиролитический графит представляет собой особую форму такого элемента, как графит. Данная его разновидность нашла широкое применение в сфере микроскопических исследований. Его применяют в качестве калибровочного материала. Чаще всего его используют в сканирующей туннельной микроскопии и в атомно-силовой микроскопии. Данная разновидность графита относится к разряду синтетических. Его получение возможно при нагревании кокса и пека.
Благодаря графиту можно получать активные металлы с химической точки зрения путем электролиза. Данный метод использования элемента объясняется тем, что у графита достаточно хорошая электропроводность.
При производстве пластмассовых изделий графит тоже нашел свое применение. Его используют для наполнения пластмассы.
Самым известным методом использования графита является производство стержней для обычных простых карандашей, к которым так привыкли люди.
Оптические свойства
Среди свойств графита следует выделить еще и оптические. Коэффициент светопоглощения остается постоянным для всего спектра. На него не влияет температура лучеиспускания тела. Если рассматривать тонкие графитовые нити, то коэффициент светопоглощения будет равен 0,77. Этот параметр уменьшается до 0,55 с увеличением кристаллов графита.
Рассматривая чистый материал, вы отметите, что он обладает незначительным коэффициентом поглощения нейтронов и наивысшим коэффициентом замедления. Благодаря этому появилась возможность использования в атомных реакторах. Без графитовых электродов невозможно было бы развитие цветной и черной химической промышленности.

Областью применения графита является еще и футеровка электролизеров для получения алюминия. Материалы с высоким содержанием углерода используются для строительства электропечей и других тепловых агрегатов. Графит ложится в основу тиглей и лодочек для сверхтвердых сплавов.
Растворение — графит
Растворение графита в у-фазе является важным процессом при нормализации ( а также и при закалке) чугуна с ферритной или феррито-перлитной структурой. Этот процесс подобен цементации стали; разница в том, что при цементации происходит насыщение поверхностного слоя стальной детали углеродом из внешней среды, а при нагреве чугунной отливки карбюризатором являются многочисленные включения графита, расположенные в металлической основе, и насыщение углеродом происходит во всем объеме отливки. На растворение углерода в аустените чугунной отливки влияет температура: с повышением температуры нагрева растворимость углерода в у-фазе резко увеличивается. В результате нормализации чугуна с исходной структурой основной массы феррит или феррит и перлит получается структура перлита или сорбитообразного перлита с повышенной твердостью и прочностью.
Процесс растворения графита достаточно быстро происходит лишь при высоких температурах.
По мере растворения графита на холодном контакте и повышения концентрации углерода в расплаве зона, где СГ ( ТХ) СА ( ТХ), расширяется в сторону высоких температур и более низких пересыщений.
Термодинамические данные для растворения графита пока еще скудны и нередко разноречивы. Не вполне ясен вопрос об энтальпии процесса.
При нагреве происходит растворение графита в аустените, в связи с чем, несмотря на различную исходную структуру чугуна, превращению при охлаждении подвергается аустенит с эвтектоид-ной или заэвтектоидной концентрацией углерода.
Обра-1 зующиеся при растворении графита и обезуглероживании чугуна поры частично или полностью заполняются окислами. Наряду с железом окисляются кремний и марганец, образующие с кислородом стойкие соединения. Как и на поверхности, окисленный слой в объеме отливок имеет гетерогенное строение.
Возможность образования пор при растворении графита следует из данных дилатометрического анализа. Если бы процесс растворения графита был обратим, размеры образцов при выделении и растворении графита изменялись бы на одну и ту же величину, но противоположную по знаку.
Установлено, что при растворении графита в жидком железе величина Д) / с имеет положительное значение на всем интервале концентраций и при NG 0 1 близка к 5000 кал / моль. Изменение энтропии ДЛ с превышает значения, отвечающие идеальным растворам; при повышении концентрации углерода фактические значения ДЛ с убывают быстрее по сравнению с соответствующими величинами, отвечающими идеальным растворам.
Таким образом, основным механизмом растворения графита является, по-видимому, прямая контактная диффузия. В этом случае науглероживание железа может быть результатом диффузии углерода по поверхности поры до тех участков, где контакт с матрицей сохранился, и в дальнейшем путем граничной и объемной диффузии. Большого различия в науглероживании по контуру включения не наблюдается, что может реализоваться в том случае, если поверхностная диффузия значительно преобладает над объемной. Во многих диффузионных парах такое соотношение скоростей диффузии в действительности имеет место, однако, в какой мере это может оказаться справедливым для Fe — Si — С-сплавов, неизвестно.
Исходя из рассмотренной выше микроскопической картины растворения графита, нетрудно объяснить эффект температуры аустенитизации и поверхностно-активных примесей. При нагреве растворимость углерода в аустените возрастает, так что уменьшение когезии графита сопровождается увеличением адгезии графита к матрице. Вследствие этого восстановление контакта двух фаз путем разрушения графита реализуется чаще. Одновременно с нагревом увеличивается и роль газов. Присадка в чугун элементов, снижающих поверхностное натяжение матрицы и тем самым ослабляющих адгезию, должна препятствовать науглероживанию. Задерживать растворение могут и примеси, увеличивающие силы связи в базисных плоскостях графита.
Месторождение графита
Месторождения чешуйчатого графита локализуются в гнейсах, кварцитах, мраморах. Образуются при метаморфизме древних осадочных толщ. Форма залежей пласто- и линзообразная, выдержана по мощности и протяжённости. Графитовые чешуйки образуют рассеянную вкрапленность в породе. Содержание углерода в руде составляет в среднем 3-18%. Месторождения графита известны в CCCP (например, Тайгинское, Урал; Завальевское, УССР), Австрии, ЧССР, ФРГ, Индии, на Мадагаскаре (район Фанандрана), в Бразилии, KHP, Канаде.
Плотнокристаллический графит слагает жилы и линзы в месторождениях гидротермально-пневмалитового генезиса или гнезда, линзы и вкрапленность в контактово-реакционных месторождениях. Пневматолито-гидротермальные месторождения связаны с согласными, реже секущими пегматитовыми, кварцевыми, полевошпатовыми и кальцитовыми жилами. Контактово-реакционные месторождения приурочены к зонам контакта обогащенных углеродом карбонатных и сланцевых пород со щелочными и габброидными породами, реже гранитами. Руды сложены полевым шпатом, кварцем, реже слюдами, карбонатом; в скарновых зонах они обогащены гранатом, волластонитом, пироксеном, скаполитом, а также минералами щелочных и габброидных пород (нефелином, канкринитом, содалитом, сфеном, апатитом). Графит (от крупно- до тонкокристаллического) слагает чешуйчатые и волокнистые агрегаты. Содержание в рудах 15-40%, на некоторых месторождениях 60-90%. Разрабатывается обычно подземным способом. Известные месторождения — Богала (Шри-Ланка) и Ботогольское (CCCP).
Скрытокристаллический графит отличается несовершенной текстурой, часто содержит примесь тонкодисперсного углеродистого вещества. Слагает мощные и протяжённые пластообразные залежи, иногда переходящие в угли. Содержание углерода составляет 80-90%. Основные породообразующие минералы: кварц, полевой шпат, серицит, хлорит, кальцит. Графит образуется при метаморфизме углей, углистых и битуминозных сланцев вблизи интрузий. Залежи разрабатываются открытым и подземным способами. Основные месторождения расположены в Мексике (штат Сонора), Южной Kopee, Австрии (рудник «Кайзерсберг»), CCCP (месторождение Ногинское).
Запасы и применение
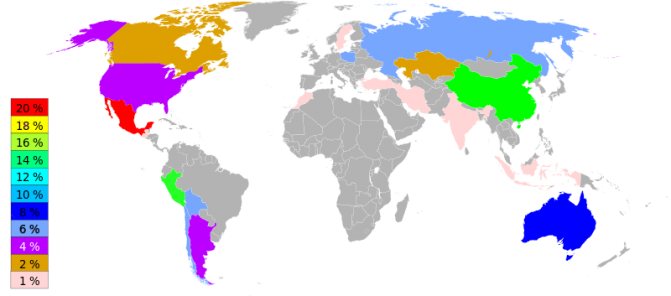
Мировые запасы графита (1978, тысяч т) в капиталистических и развивающихся странах: чешуйчатого — Южная Америка, 136; Европа, 3500; Африка, 5442; Азия, 900; плотнокристаллического — Азия, 2900; скрытокристаллического — Северная Америка (без США), 3084; Европа, 5623; Азия, 6168. О добыче графита см. в ст. графитовая промышленность.
Наряду с природным применяют искусственный графиты, который получают при охлаждении пересыщенных углеродом сплавов, термическим разложением газообразных углеводородов, нагреванием антрацита, нефтяного кокса, каменноугольного пека. Применяются графиты в металлургии (тигли, литейные формы, противопригарные краски), в химическом машиностроении (футеровочный материал, трубы и др.), в производстве коллекторов для динамо-машин, электродов, проводящих порошков, смазочных материалов, антифрикционных изделий, в ядерной технике, в производстве карандашей, красок, теплоизоляционных материалов. Искусственный кусковой графит используют в качестве эрозионностойких покрытий для сопел ракетных двигателей, камер сгорания носовых конусов.
Структура и кристаллическая решетка графита:
Графит имеет слоистую, плоскую структуру. Отдельные слои графита называются графеном. Каждый слой кристаллической решетки графита может по-разному располагаться по отношению друг к другу, образуя политипы.
В каждом слое атомы углерода расположены в гексагональной решетке на расстоянии 0,142 Нм, а расстояние между плоскостями графена составляет 0,335 Нм.
Атомы углерода, расположенные в одной плоскости слоя, связаны между собой ковалентной связью. Углерод имеет четыре свободных электрона. Однако в ковалентной связи задействованы только три электрона из четырех, поэтому каждый атом углерода связан только с тремя атомами углерода. Четвертый электрон свободно мигрирует в плоскости, делая графит электропроводящим в направлении, параллельном плоскости. Электропроводность графита в направлении перпендикулярно плоскости слоя, наоборот, в сотни раз меньше.
Между собой слои графена в графите скреплены слабыми Вандерваальсовыми силами, которые позволяют слоям графита легко быть отделенными друг от друга.
Известны две формы графита: альфа-графит (имеет гексагональную структуру и кристаллическую решетку) и бета-графит (имеет ромбоэдрическую структуру и кристаллическую решетку). Обе формы графита имеют очень схожие физические свойства, за исключением того, что слои графена у каждой формы графита укладываются несколько по-разному.

Рис. 1. Альфа-графит
У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника, а у β-графита каждый четвёртый слой повторяет первый.
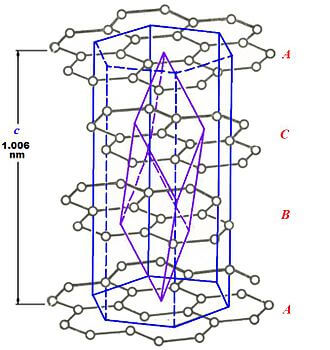
Рис. 2. Бета-графит
Альфа-графит может быть преобразован в бета-форму с помощью механической обработки. Бета-форма переходит в альфа-форму при нагревании графита свыше 1300 °C.
Получение графита
Основной метод обогащения скрытокристаллических руд — рудоразборка, плотнокристаллических и чешуйчатых — флотация. На качество концентратов накладываются ограничения по содержанию золы и гранулометрическому составу (чешуйки графита ценятся по величине). Скрытокристаллические руды размалываются. При флотации чешуйчатых и плотнокристаллических руд используют собиратели — керосин и другие углеводороды; пенообразователи — сосновое масло, спиртовые; регуляторы — соду, щёлочь; депрессоры — крахмал, реагенты на основе декстрина. Для улучшения селекции подаётся жидкое стекло. После флотации следуют мокрая классификация, сушка, воздушная классификация и гидрометаллургические операции, включающие спекание с содой, кипячение огарка, выщелачивание серной кислотой, отмывку, кипячение в содовом растворе, отмывку, сушку и сухую магнитную сепарацию с получением графита в немагнитном продукте. При доводке чешуйчатого доменного графита используется электросепарация.
Физические свойства
Хорошо проводит электрический ток. Обладает низкой твёрдостью (1 по шкале Мооса). Относительно мягкий. После воздействия высоких температур становится немного более твёрдым и очень хрупким. Плотность 2,08—2,23 г/см³. Цвет тёмно-серый, блеск металлический. Неплавкий, устойчив при нагревании в отсутствие воздуха. Жирный (скользкий) на ощупь. Природный графит содержит 10—12 % примесей глин и окислов железа. При трении расслаивается на отдельные чешуйки (это свойство используется в карандашах).
Теплопроводность графита от 100 до 354,1 Вт/(м·К), зависит от марки графита, от направления относительно базисных плоскостей и от температуры.
Электрическая проводимость монокристаллов графита анизотропна, в направлении, параллельном базисной плоскости, близка к металлической, в перпендикулярном — в сотни раз меньше. Минимальное значение проводимости наблюдается в интервале 300—1300 К, причём положение минимума смещается в область низких температур для совершенных кристаллических структур. Наивысшую электрическую проводимость имеет рекристаллизованный графит.
Коэффициент теплового расширения графита до 700 К отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение с повышением температуры уменьшается. Выше 700 К коэффициент теплового расширения становится положительным. В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положителен, практически не зависит от температуры и более чем в 20 раз выше среднего абсолютного значения для базисных плоскостей.
Теплоёмкость графита в диапазоне температур 300÷3000 К хорошо согласуется с дебаевской моделью. В высокотемпературной области после Т>3500K наблюдается аномальное поведение теплоёмкости графита аналогично алмазу: экспериментальные данные по теплоёмкости резко отклоняются вверх от нормальной (дебаевской) кривой и аппроксимируются экспоненциальной функцией, что обуславливается больцмановской компонентой поглощения тепла кристаллической решеткой.
Пределы температуры плавления — 3845—3890 °C, кипение начинается при 4200 °C[источник не указан 414 дней]. Во время сжигания 1 кг графита выделяется 7832 ккал тепла.
Монокристаллы графита диамагнитны, магнитная восприимчивость незначительна в базисной плоскости и велика в ортогональных базисным плоскостях. Коэффициента Холла меняется с положительного на отрицательный при 2400 К.
Типы и марки графита:
В соответствии с ГОСТ 17022-81 «Графит. Типы, марки и общие технические требования» выделяют следующие минералогические типы графита:
– кристаллический,
– скрытокристаллический.
Этим же ГОСТом предусмотрены следующие марки графита: ГСМ-1, ГСМ-2, ГАК-1, ГАК-2, ГАК-3, ГК-1, ГК-2, ГК-3, ГС-1, ГС-2, ГС-3, ГС-4, П, ЭУЗ-М, ЭУЗ-II, ЭУЗ-III, ЭУТ-I, ЭУТ-II, ЭУТ-III, ГТ-1, ГТ-2, ГТ-3, ГЭ-1, ГЭ-2, ГЭ-3, ГЭ-4, ГЛ-1, ГЛ-2, ГЛ-3, ЭУН, ГЛС-1, ГЛС-2, ГЛС-3, ГЛС-4.
Им соответствуют следующие виды использования (потребления) графита:
– графит специальный малозольный,
– графит аккумуляторный,
– графит карандашный,
– графит смазочный,
– графит кристаллический электроугольный,
– графит тигельный,
– графит элементный,
– графит кристаллический литейный,
– графит скрытокристаллический электроугольный,
– графит скрытокристаллический литейный.
Графит: описание и происхождение
Наряду с образованием карбонатов и углеводородов в природных условиях углерод существует в самородном виде, образуя 2 полиморфные формы – графит и алмаз. Эти одинаковые по составу минералы различаются структурой и физическими свойствами.

Графитовая горная порода известна с давних времен, однако исходной информации о ее применении нет. Отсутствие ранних исторических сведений объясняется тем, что по красящим свойствам графит имеют сходство со многими другими материалами, например молибденитом. Несмотря на скудость информации об этом камне, доподлинно известно, что в археологической культуре эпохи неолита Боян, существовавшей на территории современной Молдавии, Румынии и Болгарии в 4 тысячелетии до н. э., этот материал использовался для раскрашивания глиняной посуды.
Свое название графит получил в 89 г. XVIII в. благодаря немецкому геологу Абрааму Готлобу Вернеру. Ученый, обнаружив, что этим камнем можно писать, решил присвоить ему наименование, которое происходит от греческого слова «графо», переводящегося как «пишу».

Этот минерал в некоторых источниках также называется черным или серебристым свинцом, карбидным железом. В нашей стране этот камень впервые был обнаружен в 26-м г. XIX в. в Уральских горах.
Применение натурального графита
Область применения графита не ограничивается возможностью письма на бумаге и других поверхностях. Благодаря своим уникальным качествам этот материал имеет широкую сферу использования.
Графит применяется для:
- Производства емкостей для нагрева, высушивания, сжигания, обжига и плавления различного сырья и изготовления износостойких плит. Такое применение обусловлено его устойчивостью к воздействию высоких температур при отсутствии воздуха, а также к большому количеству расплавленных металлов.
- Изготовления электрических проводников, имеющих электронную проводимость и находящихся в контакте с электролитом, а также нагревательных элементов. Данный материал в этом направлении используется благодаря высокому уровню электропроводности и устойчивости к практически всем водным растворам с агрессивными свойствами.
- Образования химически активных металлов путем электролиза расплавленных соединений. Для получения алюминия используется одновременно 2 свойства: отличная электропроводность и газообразность продукта реакции, протекающей на электроде.
- Производства твердого смазочного сырья.
- Изготовления наполнителя пластики.
- Замедления нейтронов в ядерных реакторах.
- Производства стержней для черных графитовых карандашей. В этом случае он используется совместно с каолиновым веществом.
- Синтезирования искусственных алмазов.
- Измерения длины нанометрового диапазона для калибровки сканеров сканирующих зондовых микроскопов, предназначенных для измерения рельефа проводящих поверхностей с высоким пространственным разрешением, а также сканирующих зондовых микроскопов высокого разрешения, использующихся для определения рельефа поверхности с разрешением от десятков ангстрем вплоть до атомарного.
- Производства контактных элементов для различных электромашин, транспорта, работающего от электричества, и мостовых подъемных кранов с троллейным питанием, реостатов повышенной мощности и других устройств, которые требуют надежного подвижного электрического контакта.
- Изготовления тепловой защиты носовой области элементов поражения ракетного оружия и возвращаемых космических аппаратов.
- Производства элементов, проводящих ток в высокоомных токопроводящих склеивающих материалах.
Основные свойства природного графита
Минералы и горные породы / Описание минерала Графит

Графиты — вещества серого цвета с металлическим блеском, аморфного, кристаллического, или волокнистого сложения, жирные на ощупь, удельный вес от 1,9 до 2,6. По внешнему виду графит, имеет металлический свинцово-серый цвет, колеблющейся от серебристого до черного, с характерным жирным блеском.Поэтому потребители зачастую называют явнокристаллические графиты серебристыми, а скрытокристаллические — черными.
На ощупь графит жирен и отлично пачкается. На поверхностях он легко дает черту от серебристого до черной, блестящей. Графит отличается способностью прилипать к твердым поверхностям, что позволяет создавать тонкие пленки при натирании им поверхностей твердых тел.
Графит представляет собой алоторопную форму углерода, которая характеризуется определенной кристаллической структурой, имеющей своеобразное строение.
В зависимости от структурного строения графиты делятся на:
- явнокристаллические,
- скрытокристаллические,
- графитоиды,
- высокодисперсные графитовые материалы, обычно называемые углями.В свою очередь, явнокристаллические графиты по величине и структуре кристаллов делятся на:
- плотнокристаллические (Боготольское месторождение графита),
- чешуйчатые (Тайгинское месторождение графита).
В чешуйчатых графитах кристаллы имеют форму пластинок или листочков. Чешуйки их жирные, пластичные и имеют металлический блеск.
Практическое применение
Графит имеет очень разнообразное применение, основанное на его «жирности», кислотоупорности, огнестойкости, электропроводности. Идет на изготовление тиглей для плавки стали и цветных металлов (около 65—70% общего потребления), широко применяется в электротехнике (для изготовления электродов), как смазочный материал, при производстве красок, карандашей и др. Наиболее ценным считается кристаллический графит; скрытокристаллические разности употребляются лишь в литейном деле, как наиболее дешевое сырье.
Мировая добыча природного графита осуществляется в немногих странах и приближается к 600 тыс. т/год. Почти половина ее приходится на КНР и Россию, разрабатываю щ ие месторождения кристаллического и аморфного графита. Крупными продуцентами кристаллического графита являются Чехия, Германия, Малагасийская Республика, Норвегия, Шри-Ланка, а аморфного — Индия,
Мексика, КНДР , Южная Корея, Австрия. Мировое производств0 синтетического графита составляет около 1,5 млн т и осуществляется в промышленно развитых странах, не обладающих существенными природными запасами этого сырья: США, Канаде, Японии, странах Западной Европы.
Физические методы исследования
Что такое графит
Графит представлен веществом серого цвета с металлическим отблеском. Минерал очень распространен в природе, он образует крупные скопления кристаллов. Часто его можно найти выраженным кристаллическими включениями в другие горные породы: гнейсы, слюду, известняк и гранит.
Особенности минерала обусловлены скольжением структурных слоев относительно друг друга. Он обладает высокой теплопроводностью, что ценится в промышленности.
В натуральной среде минерал имеет несколько модификаций и разновидностей. Он подразделен по структурному признаку на гексагональный и ромбоэдрический тип.
Для ромбоэдрической модификации первому идентичен каждый четвертый слой. Такой тип графита встречается преимущественно в качестве примесей. В гексагональном варианте характерна кристаллическая решетка, у которой половина атомов смещена к центру шестиугольника.
Разновидности минерала
Природный графит является аллотропным соединением из углерода с содержанием примесей. В зависимости от состава его можно классифицировать:
По сферам применения и содержанию примесей:
- Пиролитический – искусственно воспроизведенный минерал применяется в инструментах для микроскопических исследований.
- Коллоидный – технический графит, используемый в промышленности, преобразованный из чистейшего искусственного камня в порошок.
- Силицированный – устойчивое к эрозиям и коррозиям вещество, полученное искусственным методом с добавлением жидкого кремния при изготовлении.
| По структуре | По цвету |
| Чешуйчатый | Серебристый серый |
| Графитовый сланец | Белый |
| Волокнистый | Матовый светлый |
| Плотнокристаллический | Черный |